Se comunican 43 casos de insuficiencia renal aguda (IRA) por picadura múltiple de abejas africanizadas (AA) recopilados entre 1982 y 2007 en la Sección de Nefrología de la Universidad de Antioquía y el Hospital San Vicente de Paúl, de Medellín, Colombia. No se realizó ninguna intervención diferente a responder la interconsulta a nefrología y a ordenar los procedimientos de diálisis. Los datos obtenidos de las historias clínicas incluyeron datos demográficos; presentación clínica; exámenes de laboratorio realizados en el momento del ingreso; evolución de función renal para documentar la mejoría y la curación de la IRA; intervalos entre picaduras y desenlaces; número de sesiones de diálisis; duración del seguimiento y la hospitalización; supervivencia, y mortalidad. Los datos no fueron completos en los 43 casos; por ello se expone el número exacto de observaciones cuando corresponde. Edad promedio: 56 ± 26 años (rango, 2-96); 37 (86%) fueron hombres; 38 (de 41 con datos) procedían del área rural (91%); 22 de 39 fueron agricultores (56,4%); 33 de 41 provinieron de la ciudad de Medellín o el departamento de Antioquía (80,5%). Número de picaduras por paciente: aproximadamente 900. Intervalo entre picadura múltiple e IRA <48 horas: 31 casos (72,1%; promedio 2,6 ± 2,6 días; rango, 1-12); 37 de 43 requirieron diálisis (86%); promedio de sesiones: 4,7 ± 3,3 (rango, 1-12). Supervivencia: ocurrió en 36 casos (83,7%); mortalidad: en siete, todos >60 años (16,3%). La mejoría de la función renal se produjo en 36 casos (83,7%) y la normalización en 15 de los 36 casos (41,7%). El intervalo hasta el inicio de la diuresis fue de 10,6 ± 6,8 días (rango, 1-25). La duración de la hospitalización fue de 16,9 ± 8,7 días (rango, 1-39). El seguimiento fue de 25,2 ± 18,3 días (rango, 1-75). Hematuria y oliguria se produjeron antes de 24 horas de las picaduras; hubo elevación de CPK en el 90%, de ALT en el 96%, de AST en el 89%, de láctico-deshidrogenasa en el 95%, y de BUN y creatinina en el 100%. Basándonos en nuestros hallazgos y en la revisión de la información de la que disponemos, postulamos que este tipo de IRA se produce como resultado de rabdomiólisis con mioglobinuria subsiguiente, lo que desencadena una necrosis tubular aguda nefrotóxica; probablemente influye, además, algún grado de nefrotoxicidad directa no cuantificable con los métodos diagnósticos actuales. Un mayor conocimiento de esta entidad por parte de la comunidad médica puede ayudar a mejorar el tratamiento y el pronóstico de los pacientes que la presentan.
Acute renal failure due to multiple stings by Africanized bees. Report on 43 cases. This study reports on acute renal failure (ARF) due to multiple stings by Africanized bees (AB) occurring in 43 cases collected between 1982 and 2007 (at the Nephrology Section, University of Antioquia School of Medicine and San Vicente de Paul University Hospital, Medellin, Colombia). No intervention on patient care was performed except for responding the Nephrology consult and prescribing dialysis. Data obtained from the medical records included demography; clinical presentation; laboratory results on admission; evolution of renal function to document improvement and normalization; intervals between stings and outcomes; number of dialysis sessions; length of follow-up and hospitalization; survival; and mortality. Not all patients had complete data and therefore, the number of observations is included where required. Mean age was 56 ± 26 yr (range 2–96); 37 (86%) were men; 38 (of 41 cases) came from rural areas (91%); 22 (of 39) were farmers (56.4%); 33 (of 41) lived in Medellin or in the department of Antioquia (80.5%). Number of stings per patient: ~ 900. Interval between stings and ARF < 48 hours: in 31 cases (72.1%; mean 2.6 ± 2.6 days; range 1–12); 37 (of 43) required dialysis (86%); mean number of sessions: 4.7 ± 3.3 (range 1–12). Survival occurred in 36 cases (83.7%) and mortality, in 7, all > 60 yr (16.3%). At last follow-up, renal function improvement was documented in 36 (83.7%) and normalization in 15 of them (41.7%). Interval until initiation of diuresis: 10.6 ± 6.8 days (range 1–25). Duration of hospitalization: 16.9 ± 8.7 days (range 1–39). Follow-up: 25.2 ± 18.3 days (range 1–75). Hematuria and oliguria occurred before 24 hours; there was an increase of CPK in 90%, of ALT in 96%, of AST in 89%, of DHL in 95%, and of BUN and creatinine in 100%. Based on our findings and on the review of the available information, we propose that this type of ARF occurs as a result of rhabdomyolysis with subsequent myoglobinuria, which lead to nephrotoxic acute tubular necrosis; a variable degree of direct nephrotoxicity, not quantifiable with current diagnostic methods, is also probably involved. A better knowledge of this entity by the medical community could improve care and prognosis of the patients who develop it.
INTRODUCCIÓN
En 1986, el Grupo de Nefrología de la Facultad de Medicina de la Universidad de Antioquía y el Hospital Universitario San Vicente de Paúl de Medellín, Colombia publicaron los datos de los primeros 5 casos de insuficiencia renal aguda (IRA) producida por picadura múltiple de abejas africanizadas (AA)1 que se acompañaba de un "Editorial" sobre el tema en la misma revista2. Nuestro primer paciente fue atendido en 1982 y desde entonces hemos seguido recopilando todos los que fueron referidos a este hospital por presentar IRA como complicación de picadura múltiple de AA. Durante las últimas tres décadas se han publicado numerosos casos aislados o pequeñas series sobre esta forma de alteración de la función renal3-16, pero la nuestra, que recopila 43 casos, es la más extensa de la bibliografía científica.
En este estudio descriptivo se comunican los hallazgos sobre su presentación clínica, su historia natural y su pronóstico; asimismo, se discuten sus posibles mecanismos fisiopatológicos, que tanto la bibliografía médica existente como nuestro análisis, indican que se debe a rabdomiólisis causada por el veneno de las abejas. El objetivo es ilustrar a la comunidad médica sobre las características de la IRA como complicación de la picadura múltiple de AA para poder, de esta forma, mejorar su tratamiento y el pronóstico de quienes la presentan.
MATERIALES Y MÉTODOS
Entre enero de 1982 y diciembre de 2007 se realizó una recopilación longitudinal sobre la información clínica de 43 casos de pacientes con diagnóstico de picadura múltiple de AA complicada con alteración de la función renal, pero no se participó en el cuidado médico directo de los pacientes en los servicios de urgencias, cuidados intensivos, medicina interna o pediatría donde estuvieron hospitalizados los pacientes (39 casos fueron remitidos al Hospital Universitario San Vicente de Paúl y cuatro fueron comunicados por otras instituciones). No se dispuso de todos los datos clínicos, de laboratorio o de la evolución en el total de los pacientes, por lo cual en algunas variables el número sobre el que se extraen los promedios no es de 43; cuando esto ocurre, se consigna el número de observaciones correspondiente.
En la recogida de los datos a partir de las historias clínicas se mantuvo el anonimato sobre la identidad de los pacientes; por esta razón, no se solicitó consentimiento informado y el estudio se clasificó como sin riesgo para los sujetos cuya información se recopiló.
Datos demográficos
De cada caso se obtuvieron (de acuerdo con la disponibilidad, como ya se ha mencionado) los datos de edad, género, procedencia de área urbana o rural, ubicación geográfica donde ocurrió la picadura, oficio o profesión.
Datos clínicos
Se documentaron presencia o no de hematuria, hipotensión u oliguria/anuria al momento de la remisión del paciente; estimación del número de picaduras; intervalo entre picadura y remisión al hospital; duración de la oliguria; número de sesiones de hemodiálisis (o de diálisis peritoneal en los pocos casos en los que ésta se empleó); documentación de mejoría (iniciación de la diuresis y/o disminución de cifras de creatinina, BUN y/o potasio, suficientes para no requerir diálisis a juicio de los médicos que trataban a los pacientes) o curación (normalización de la función renal); duración de la hospitalización y del seguimiento hasta la última consulta documentada; mortalidad, causa de la muerte cuando ésta ocurrió y supervivencia.
El seguimiento continuó hasta que los pacientes fueron dados de alta del hospital o de la interconsulta por el servicio de nefrología (esto último generalmente tuvo lugar cuando dejaron de tener criterios para tratamiento con diálisis y/o se inició la diuresis), o hasta la última revisión ambulatoria.
Datos de laboratorio
Se registraron los resultados de las pruebas en el momento del ingreso, los de la evolución durante la permanencia en el centro asistencial y los posteriores a la salida del hospital en la pequeña parte de los pacientes en los que pudo continuarse su seguimiento en la consulta ambulatoria. Las pruebas registradas fueron: hemoglobina, hematocrito, plaquetas, leucocitos, neutrófilos, creatinina, BUN, sodio, potasio, aspartato (AST) y alanino-aminotransferasas (ALT), creatina-fosfokinasa (CPK), lactico-deshidrogenasa (DHL), bilirrubinas total y directa, glucemia, hematuria y proteinuria en muestra de orina ocasional. Los métodos utilizados para realizar las pruebas fueron los que sistemáticamente empleaba el laboratorio clínico del hospital.
Se consignan sólo los resultados de los exámenes de laboratorio en el momento del ingreso que fueron los que permitieron llevar a cabo los diagnósticos; las pruebas durante el seguimiento en la hospitalización no se incluyen en el análisis debido a la variabilidad de tiempos y frecuencias con las que se les ordenaron y registraron. Las pruebas de función renal durante la evolución se evaluaron para documentar su mejoría o normalización.
Análisis estadístico
Los datos se expresan en número (± desviación estándar [DE]) y en porcentajes del total, aplicables a los 43 pacientes o al número exacto en el que el dato estuvo disponible; se incluyen, asimismo, los promedios y los rangos.
RESULTADOS
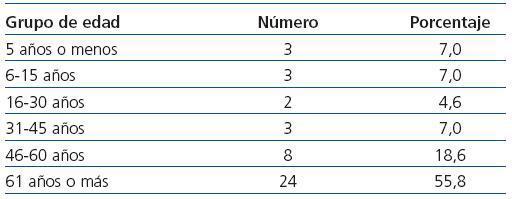
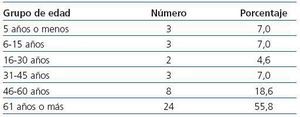
En los 25 años se recopilaron 43 casos de IRA causada por picadura múltiple de AA. La edad promedio fue de 56 ± 26 años (rango, 2-96). La distribución por grupos de edad se expone en la tabla 1.
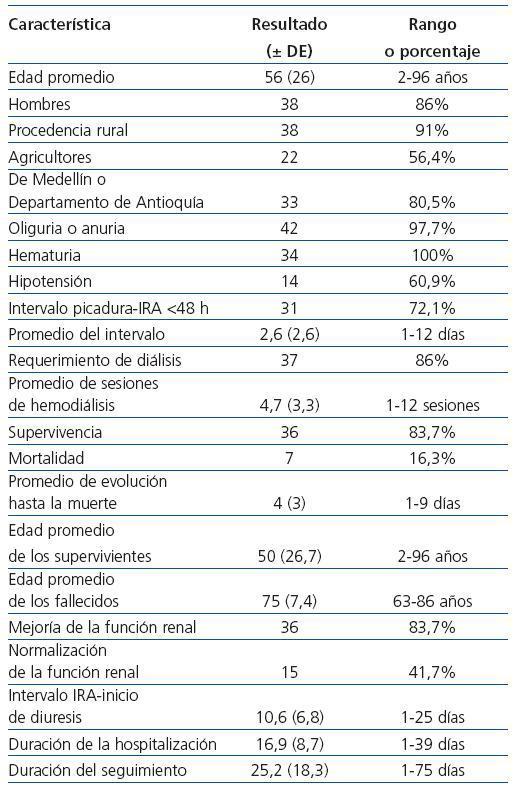
La gran mayoría (37 casos, 86%) pertenecía al sexo masculino y sólo 6 pacientes (14%) eran mujeres. La procedencia (n = 41) fue del área rural en 38 (91%) y de la urbana en 3 casos (7%). El oficio o profesión (n = 39) fue agricultor en 22 casos (56,4%); en 3 casos cada uno (7,7%) fueron jubilados, estudiantes, amas de casa y niños en edad preescolar, y en un caso cada uno fueron médico, tractorista, zapatero, oficinista y retrasado mental sin ocupación. Las procedencias geográficas (n = 41) fueron de la ciudad de Medellín y/o el departamento de Antioquia en 33 casos (80,5%) y de otros departamentos de Colombia en ocho (19,5%) (tabla 2).
La presentación clínica incluyó oliguria o anuria en 42 de los 43 casos (97,7%). Hematuria macroscópica o microscópica se encontró en 34 (100%, n = 34), e hipotensión, en 14 casos (60,9%, n = 23). Estos signos clínicos aparecieron en las primeras 24 horas de la picadura múltiple. La mayoría de los pacientes recibió atención primaria en el centro de salud o en el hospital local, que incluyó esquemas variables de prescripción de adrenalina, corticosteroides, antihistamínicos, antibióticos y líquidos intravenosos, durante períodos inferiores a 24 horas que precedieron a su remisión al centro médico de referencia.
El intervalo entre la picadura múltiple y la IRA (n = 43) fue menor de 48 horas en 31 casos (72,1%) y mayor de 2 días en 12 casos; el promedio fue de 2,6 ± 2,6 días (rango, 1-12). De los 43 casos, 37 requirieron tratamiento con diálisis (86%), en 2 casos se llevó a cabo solamente diálisis peritoneal y en otros dos, una sesión de diálisis peritoneal y otras de hemodiálisis. Cuatro pacientes mejoraron sin diálisis (14%); en los 34 que recibieron solamente hemodiálisis, el promedio de sesiones fue de 4,7 ± 3,3 (rango, 1-12).
La estimación del número de picaduras se realizó en los primeros casos y se encontraron aproximadamente 900 lesiones; no se continuó dado lo dispendioso del procedimiento y porque clínicamente era evidente la afectación masiva en todas las superficies descubiertas del cuerpo y en aquellas cubiertas con ropa ligera. Hubo un caso de picadura en la córnea que requirió posteriormente la realización de un trasplante; en 2 casos se produjo una picadura en la glotis que obligó a una intervención urgente para garantizar la permeabilidad de la vía aérea.
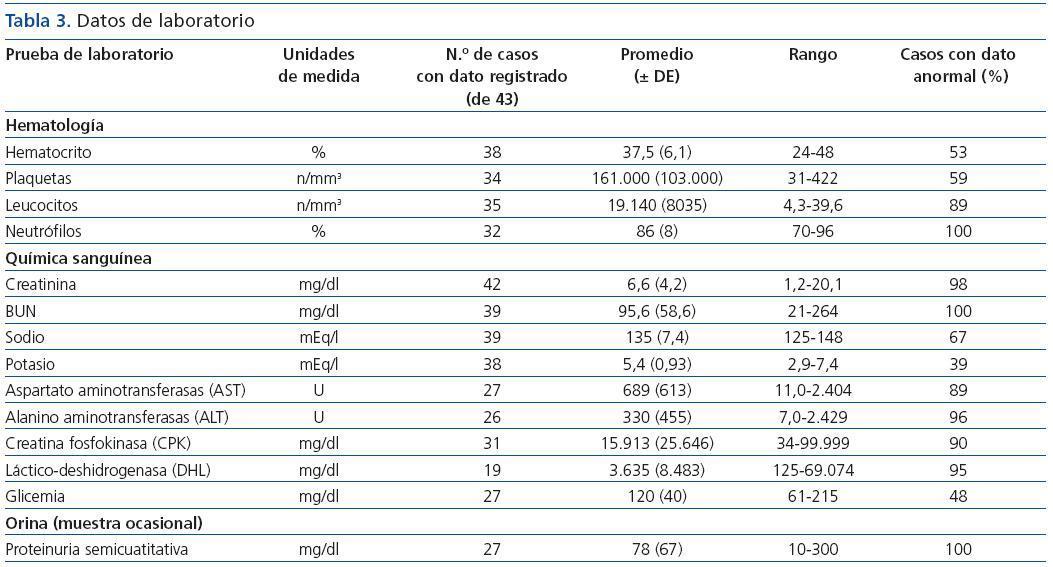
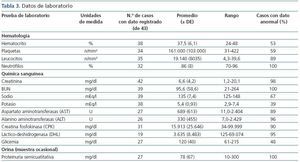
El día del ingreso se documentaron los siguientes hallazgos: elevación de BUN en el 100% y de creatinina en el 98% de los casos (en el único de ellos que no la tuvo al inicio, se le elevó al segundo día); anemia en el 53%, leucocitosis en el 89%, neutrofilia en el 100%, trombocitopenia en el 59%, hiponatremia en el 67%, hiperpotasemia en el 39%, elevación de AST en el 89%, de ALT en el 96%, de CPK en el 90%, de DHL en el 95%, de bilirrubina total en el 38%, de bilirrubina directa en el 29%, de glucemia en el 48% y de proteinuria en muestra de orina ocasional en el 100%. La tabla 3 incluye el número de casos con dato registrado, así como los promedios y las desviaciones estándar para cada prueba de laboratorio, los rangos y los porcentajes en los que se presentó un hallazgo anormal.
Siete de los pacientes fallecieron (mortalidad del 16,3%) y 36 sobrevivieron (83,7%). Las causas de muerte consignadas en la historia clínica fueron paro cardiorrespiratorio en dos, y sindrome de distrés respiratorio, shock séptico, acidosis grave, desequilibrio hidroelectrolítico y no aclarado, en uno cada uno.
En 36 casos se produjo una mejoría de la función renal (83,7%); los 7 casos (16,3%) en quienes no la hubo, fueron los que fallecieron. El promedio de edad de quienes sobrevivieron fue de 50 ± 26,7 años (rango, 2-96) y el de quienes fallecieron, de 75 ± 7,4 años (rango, 63-86). En 15 de los supervivientes se documentó la normalización de la función renal (41,7%). Los pacientes que fallecieron lo hicieron tempranamente en la evolución de la IRA, sin tener tiempo para alcanzar a manifestar alguna recuperación de la lesión renal y sólo en uno de ellos hubo mejoría de la oliguria, pero no de la función. El período de tiempo promedio para la iniciación de la diuresis fue de 10,6 ± 6,8 días (n = 35; rango, 1-25) (tabla 2).
La duración promedio de la hospitalización (hasta el alta o hasta que se registró seguimiento) fue de 16,9 ± 8,7 días (rango, 1-39). El intervalo promedio entre la admisión y el último seguimiento hospitalario o ambulatorio (incluidos el día en el que se documentó la normalización de la función renal y el de la muerte en quienes fallecieron), fue de 25,2 ± 18,3 días (rango, 1-75). La muerte se produjo, como media, a los 4 ± 3 días de la hospitalización (rango, 1- 9) (tabla 2).
DISCUSIÓN
En 1957 se escaparon de un apiario de AA en la ciudad de Río Claro, estado de Sao Paulo, Brasil, 26 enjambres con sus reinas. De inmediato se previó que habría una mezcla de estas abejas con las especies nativas y nadie especuló con que de este accidente, aparentemente banal, pudieran derivarse riesgos para la población. Se presumió que su diseminación completa por el hábitat compatible con su supervivencia dentro del continente americano se demoraría varios años17,18; no obstante, para 1992 ya habían llegado a diferentes zonas de Norte y Suramérica ubicadas en latitudes por encima o por debajo de las cuales, las estaciones no les permiten sobrevivir18-20. Simultáneamente comenzaron a aparecer publicaciones que comunicaban casos aislados o pequeñas series sobre esta forma de IRA3-16.
En estas comunicaciones de casos se postula que la fisiopatología de la IRA puede estar asociada con rabdomiólisis, hemólisis, hipotensión, shock anafiláctico y acción directa tóxica del veneno (el inóculo masivo ocurre al recibir aproximadamente 1.000 picaduras; con cada picadura, la abeja inyecta un máximo de 90 μg del veneno que es lo que puede contener el saco del insecto adulto20, pero hay que tener en cuenta que no todas las abejas tienen el mismo volumen de veneno ni logran inyectar la totalidad de éste). La mayoría de estas publicaciones establece como causa del fallo renal la rabdomiólisis3,5,7-9,11,13-16; en muchas de ellas se postula también la hemólisis como mecanismo asociado3,5,9,11,13-15. Dos artículos proponen la toxicidad directa como mecanismo, asociado a rabdomiólisis y/o a hemólisis11,14 y solo uno la atribuye a shock anafiláctico6.
Independientemente del mecanismo fisiopatológico que explique la necrosis tubular aguda (NTA), la mayoría de los casos referidos en estas series se concentró en los extremos de la vida (niños y adultos mayores); en ellos se requirió tratamiento con diálisis, excepto en uno que no fue sometido a diálisis y que falleció por hiperpotasemia7; en casi todos se realizó hemodiálisis y en unos pocos, diálisis peritoneal, siempre según la disponibilidad del recurso terapéutico.
Entre los posibles factores de riesgo para el desarrollo de la IRA se encuentran que la mayoría de nuestros pacientes (56%) eran mayores de 60 años, hecho que concuerda con su menor capacidad para escapar del ataque de los enjambres, y que la mortalidad se concentró en este grupo de edad (100%), lo que hace de la mayor edad un factor pronóstico negativo. Una alteración previa de la función renal sería otro factor, pero desconocemos esta información; no obstante, la reducción normal de la RFG causada por la edad en los >60 años, probablemente la favorece. En nuestra serie, la rabdomiólisis por sí misma puede considerarse como factor de alto riesgo para el desarrollo de NTA oligúrica, pero el número de casos limita la utilidad potencial de estratificarlo según niveles de CPK o de otras enzimas.
En los casos de IRA por picadura múltiple de AA que estamos analizando en este artículo, observamos que habitualmente la hematuria y la oliguria tuvieron lugar dentro de las primeras 24 horas; hubo una elevación temprana, rápida y progresiva tanto de las enzimas de origen muscular (CPK en el 90% de los casos, ALT en el 96%, AST en el 89%, DHL en el 95%), como de las pruebas de función renal (BUN y creatinina en el 100%). Simultáneamente, hubo trombocitopenia en el 59%, leucocitosis en el 89%, neutrofilia en el 100%, hiponatremia en el 67% e hiperpotasemia en el 39% de los casos. Por estas razones, en nuestra opinión, los mecanismos que causan la IRA no tienen ninguna relación con las reacciones anafilácticas que se presentan al recibir una sola picadura.
En relación con el análisis de la fisiopatología, la hemólisis podría desempeñar algún papel dadas las propiedades vasoactivas, citolíticas y hemolíticas de varios de los componentes del veneno. Sin embargo, en nuestra serie sólo hubo 2 casos con hallazgos compatibles con hemólisis, en quienes hubo ictericia; se encontró elevación de la bilirrubina total en un 38% (importante sólo en un caso) y de la directa en un 29%; ninguno de los casos presentó otras manifestaciones clínicas de hemólisis.
Los hallazgos hematológicos pueden relacionarse con los efectos tóxicos hemolíticos y proinflamatorios del veneno21. Desde el punto de vista de los electrolitos, los casos de hiponatremia podrían deberse a dilución causada por la hidratación recibida por la mayoría de los pacientes y la poca frecuencia de hiperpotasemia, a la iniciación temprana de la terapia de reemplazo renal.
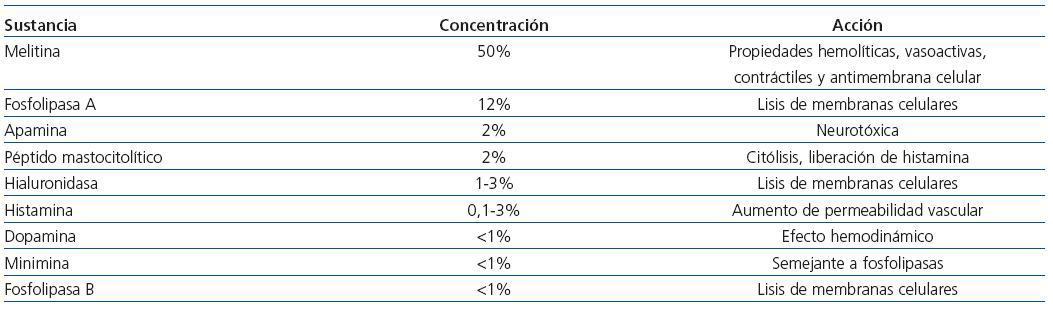
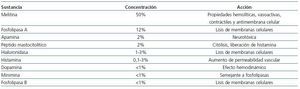
El veneno contiene un 35-50% de melitina y un 12% de fosfolipasa A, que ejercen efectos citolíticos al actuar sobre la membrana fosfolipídica de células sanguíneas y endotelio vascular; la fosfolipasa, a su vez, produce rabdomiólisis de músculo esquelético y cardíaco, lesión hepatocelular y formación de sustancias proinflamatorias; tiene, además, un 2-3% de hialuronidasa, un 2% de apamina, un 2% de péptido mastocitolítico, un 1% de fosfatasa ácida y cantidades menores de otras sustancias como histamina, todos los cuales contribuyen a la fisiopatología de la lesión20,21. En la tabla 4 se presentan la composición del veneno y las acciones principales de cada componente.
Los estudios experimentales realizados durante las 2 o 3 últimas décadas, aunque no son muy abundantes, sí parecen ser suficientes para apoyar el papel de la rabdomiólisis como principal mecanismo fisiopatológico en esta entidad. En una de estas investigaciones, la inyección experimental de veneno de AA a ratas Wistar adultas produjo rabdomionecrosis demostrada indirectamente por la elevación de las enzimas musculares y directamente por necrosis e inflamación del músculo esquelético en la microscopia de luz22.
Otro estudio con el mismo modelo de inyección i.v. del veneno en los mismos animales evaluó la función renal después del inóculo, encontrando disminución de la RFG y aumento de la FENa y la FEK (como reflejo de cambios tubulares proximales). En la histología de muestras obtenidas después de 30 horas de observación, se identificaron NTA y formación de cilindros en los túbulos distales y colectores. Los hallazgos permitieron a los autores llegar a la conclusión de que la IRA se debía a los múltiples efectos del veneno: alteraciones hemodinámicas por vasodilatación sistémica, mioglobinuria y nefrotoxicidad directa sobre las células tubulares23.
Estudios inmunohistoquímicos realizados posteriormente por este mismo grupo de investigadores en el mismo modelo experimental observaron que había mioglobina y actina muscular en los cilindros tubulares. En el examen de los especímenes renales con microscopio electrónico encontraron vacuolización intracitoplasmática en los segmentos tubulares proximales con atenuación del borde “en cepillo” de las células, así como muerte celular y apoptosis con denudación de la membrana basal tubular. Basándose en ello, postularon que la NTA se debía a los efectos de la melitina y las fosfolipasas sobre las membranas biológicas, asociados con toxicidad directa, con mioglobinuria y posiblemente con algún grado de isquemia24.
En otra comunicación de casos se evalúa el mecanismo de lesión renal mediante la inyección i.v. experimental de veneno a ratas; se demostró una reducción de RFG, de flujo sanguíneo renal y de depuración de inulina, junto con aumento de CK, DHL y AST, todo sin modificación en la presión arterial sistémica. En la histología de los especímenes obtenidos después de 24 horas de la inyección, se hallaron lesión tubular aguda y depósitos masivos de mioglobinuria en los túbulos. En una segunda fase del experimento, se agregó veneno a una suspensión aislada de túbulos proximales que fue sometida a normoxia y después a hipoxia-reoxigenación, con el fin de evaluar la nefrotoxicidad directa; se encontró un incremento altamente significativo de liberación de DHL. Los autores llegaron a la conclusión de que la vasoconstricción, la nefrotoxicidad directa y la rabdomiólisis son importantes en la IRA inducida por el veneno, y que estos efectos se presentan en ausencia de hipotensión o hemólisis25.
En nuestra opinión, estos estudios presentan la limitación de que, al menos en teoría, la inyección i.v. del veneno no replica la forma subcutánea como ocurre la inoculación en los humanos que son víctimas de la picadura múltiple de AA. La inoculación masiva de una dosis del veneno por vía i.v. favorece el desarrollo de los efectos hemodinámicos de los componentes vasodilatadores e inflamatorios y de los hemolíticos, así como la acción tóxica sobre las superficies endoteliales de capilares y túbulos.
Para investigar la hipótesis de la acción directa del veneno en las células, se ha evaluado su efecto y el de su principal componente, la melitina, sobre los mecanismos transportadores apicales de membrana de las células tubulares proximales. La aplicación de veneno seco y de melitina a cultivos aislados de dichas células (de conejos), produjo tanto reducción de la viabilidad celular como inhibición de la actividad de estos transportadores renales (efectos que son dependientes de la dosis) e incremento en la captación de Ca2+. Estos cambios se inhibieron con mepacrina (sustancia bloqueadora de los transportadores) y con bloqueadores de canales de calcio, respectivamente. Los resultados de los experimentos tanto con veneno completo como con melitina fueron iguales, lo que demostró que esta última sustancia es la responsable de los efectos mencionados26.
Debido a la mezcla compleja de enzimas y proteínas que contiene el veneno, este mismo grupo evaluó diferentes fracciones del veneno sobre los transportadores apicales en su modelo experimental de cultivo de células del túbulo proximal. Según su solubilidad se encontraron tres fracciones y de ellas la BVA (Bee Venom A), produjo reducción de la viabilidad de las células. Ésta se separó posteriormente en 3 subfracciones según su peso molecular (BF1 [Pm >20 kD]; BF2 [Pm 10–20 kD], y BF3 [Pm <10 kD]). De éstas, la BF3 fue la más efectiva en producir los efectos experimentales; además, estos cambios se asociaron con la actividad de la cascada de estrés oxidativo dependiente de fosfolipasa A2 y de Ca2+ 27.
Tomados en conjunto, los estudios experimentales mencionados apoyan tanto la rabdomiólisis como la toxicidad directa del veneno sobre las células tubulares renales, como explicación fisiopatológica de la IRA producida por el veneno de AA.
La revisión sobre el impacto que pueda tener este problema en las áreas geográficas del mundo donde es posible que se presente permite predecir que los casos continuarán ocurriendo y siendo comunicados con una frecuencia creciente. Para tratar de prevenir sus consecuencias, se están desarrollando vacunas para profilaxis en personas que tengan incremento en el riesgo de sufrir la picadura masiva, pero su efectividad es aún pobre28.
Existe controversia sobre si la remoción de los aguijones previene mayor inoculación de veneno; un artículo afirma que no existe fundamento para hacerlo pues pasados 20 segundos de la picadura toda la carga que la abeja podía inyectar ya ha pasado al sujeto picado29; sin embargo, otra publicación hace hincapié en que deben removerse para evitar un mayor envenenamiento, sin que importe si esta remoción se realiza “afeitando” los aguijones o extrayéndolos30.
Es de esperar también, que en el futuro, con el advenimiento de los biomarcadores séricos y urinarios de lesión tubular aguda como cistatina C, Neutrophil Gelatinase-Associated Lypocalin (NGAL), Kidney Injury Molecule-1 (KIM-1), interleukina 18 (IL-18) y otros, se pueda llegar a esclarecer en forma precisa el mecanismo de esta lesión en la enfermedad humana31.
Es importante que la comunidad médica en general sea consciente de que los pacientes con picaduras múltiples de AA requieren una remisión rápida a centros asistenciales de alta complejidad, pues la lesión renal forma parte de su historia natural, y de que el tratamiento con hemodiálisis debe iniciarse tempranamente para prevenir complicaciones y reducir la mortalidad28-30.
En conclusión, de acuerdo con nuestro análisis y con la revisión de la información de la que disponemos, creemos que la alteración de la función renal se debe a un efecto tóxico directo del veneno sobre la masa muscular, lo que desencadena rabdomiólisis con necrosis tubular aguda de tipo nefrotóxico subsiguiente, causada por la mioglobinuria. Además, es muy posible que intervenga algún grado de nefrotoxicidad directa no cuantificable con las pruebas diagnósticas existentes hoy día. Sobre las bases discutidas, sugerimos que la picadura múltiple de AA se añada a la lista de causas de rabdomiólisis y de IRA de tipo nefrotóxico. El esclarecimiento adecuado de los mecanismos fisiopatológicos implicados en este trastorno podrá conducir a diseñar intervenciones terapéuticas para prevenir o reducir el desarrollo de la lesión tisular producida por el veneno.
AGRADECIMIENTOS
Damos las gracias a los colegas nefrólogos y a los estudiantes de posgrado de medicina interna y de nefrología que contribuyeron a detectar los casos, nos los comunicaron y colaboraron en la recogida de los datos a partir de los registros médicos.
Tabla 1. Distribución de los casos por grupos de edad
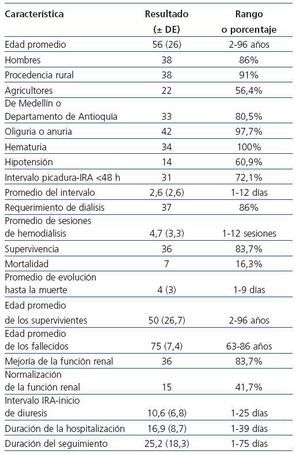
Tabla 2. Características demográficas
Tabla 3. Datos de laboratorio
Tabla 4. Composición del veneno de las abejas africanizadas (refs. 20,21)