La enfermedad renal crónica tiene una alta prevalencia y coste, así como un mayor riesgo de ingreso. Disponemos de registros públicos y obligatorios, pero no hay referencias recientes para estimar el impacto que el tratamiento sustitutivo renal (TSR) tiene en la actividad hospitalaria.
MétodosTras las autorizaciones pertinentes, hemos integrado las bases de datos REMER (2013-2014) y CMBDH (2013-2015) para analizar la actividad hospitalaria durante el primer año de TSR.
ResultadosUn total de 767 pacientes iniciaron TSR en los 7 hospitales de tercer nivel de la Comunidad de Madrid. Más de una tercera parte lo hicieron de forma no programada durante un ingreso. Este inicio es más frecuente en HD que en DP, pero existen diferencias clínicas relevantes en edad y en comorbilidad. Descartando este primer episodio, casi el 60% de pacientes ingresan durante el primer año. La tasa de ingreso es de 1,2 ingresos/paciente, más alta en HD que en TX y DP; la estancia media es de 8,6días. El coste agregado de los ingresos del primer año es de 12.006€/paciente. Nuestro análisis asegura la inclusión exhaustiva de todos los episodios y la estimación precisa de costes.
ConclusionesEl impacto del TSR en la actividad hospitalaria ha sido infraestimado y es una parte importante del coste global del TSR. Los resultados de la literatura internacional no pueden extrapolarse a nuestro país por las diferencias en el modelo sanitario y perfil de paciente. La integración de bases de datos clínicas es técnicamente viable y podría abrir una vía inmensa de información que solo requiere apoyo institucional para su desarrollo.
Chronic kidney disease has a high prevalence and economic impact, and an increased risk of hospitalization. Although there are public regional and country registries, we have not found references to estimate the impact of renal replacement therapy (RRT) on hospital admissions.
MethodsWe obtained authorization from the ethics committee and health authorities to integrate the REMER [Madrid Kidney Disease Registry] (2013-2014) and Minimum Basic Data Set (2013-2015) databases and to analyze the admissions during the first year of RRT.
Results767 patients started RRT in all the hospitals of our region across all RRT modalities. More than a third of the patients start dialysis during a hospital admission. This unplanned start, more common in HD than PD, shows relevant differences in patient profile or admission characteristics.
Without considering this initial episode, almost 60% of patients were admitted during their first year. The hospitalization rate was 1.2admissions/patient, higher in HD than in TX or PD; the mean length of stay was 8.6days.
The estimated cost of admissions during the first year is €12,006/patient. Our analysis ensures the exhaustive inclusion of all episodes and accurate estimation based on the discharge form.
ConclusionThe impact of RRT on hospitals has been underestimated and is very relevant when calculating the total cost of RRT. Results from other countries cannot be extrapolated due to differences in the health system and patient profile. The integration of clinical databases could open up an opportunity that needs only institutional support for its development.
La enfermedad renal crónica (ERC) es una enfermedad de alta prevalencia, elevada mortalidad e impacto personal, con un alto coste organizativo y económico1. Según datos del estudio EPIRCE2, el 9,24% de la población adulta tiene algún grado de ERC y el 6,83% se encontraría en estadios3 a 5. Las tasas de incidencia en tratamiento sustitutivo renal (TSR) en España son similares al promedio de países europeos, aunque mantenemos una mayor prevalencia3. En los últimos años la incidencia en TSR en la Comunidad de Madrid (CM) ha aumentado progresivamente, pasando de 123,9 por millón de población (pmp) en 2013 a 129,1 en 20144, siendo incluso más alta en el conjunto del país, de 133,6 pmp y de 156,6 pmp en población adulta5.
La ERC tiene además un elevado coste sanitario, pues se estima que consume el 2,5% del presupuesto del Sistema Nacional de Salud y más del 4% de atención especializada: unos 800 millones de euros por año1. Aproximadamente el 73% de los costes del TSR incidente son de pacientes en hemodiálisis (HD), el 21% de pacientes trasplantados renales (TX) y solo un 6% se debe a pacientes en diálisis peritoneal (DP)6. Algunos estudios estiman menores costes para el trasplante (TX) a partir del segundo año, que es más elevado durante el primer año por el peso de la cirugía, de los ingresos y del tratamiento inmunosupresor inicial7.
Los pacientes en diálisis tienen un alto riesgo de ingreso comparado con otras patologías crónicas, y las complicaciones más frecuentes durante el primer año son las relacionadas con el acceso vascular, las infecciones y la insuficiencia cardiaca congestiva8,9.
Una mayor tasa de hospitalización por infecciones o relacionadas con el acceso vascular se correlaciona con un riesgo aumentado de mortalidad precoz8. En los últimos años el ingreso debido a procesos cardiovasculares ha aumentado entre un 20 y un 30% durante los primeros meses en diálisis, mientras que los ingresos por infección se han incrementado casi un 200% en los dos primeros meses.
La mayor parte de la información disponible sobre la hospitalización en TSR procede de otros países y no puede extrapolarse al nuestro por las diferencias en el modelo sanitario, perfil de riesgo, prevalencia relativa de las técnicas de TSR e incluso por factores culturales.
En nuestro país disponemos de un registro obligatorio de TSR en todas las comunidades autónomas, cuya memoria se publica anualmente agrupada en el registro nacional (REER). Por otro lado, el Conjunto Mínimo Básico de Datos de Hospitalización (CMBDH), impulsado por el Consejo Interterritorial de Sistema Nacional de la Salud en 1987 (Acuerdo número 30) y obligatorio desde 1999 (Real Decreto 89/1999), recoge los datos demográficos y clínicos de todos los ingresos en instituciones sanitarias del Estado español10.
Pese a ello, no hemos encontrado ninguna referencia reciente, de ámbito nacional o autonómico, suficientemente amplia y directamente enfocada a analizar el impacto que el TSR tiene sobre la actividad especializada hospitalaria.
El objetivo del presente proyecto es integrar estas bases de datos, demostrando su utilidad para estimar el impacto que tiene el primer año en TSR en todos los hospitales de tercer nivel de una comunidad autónoma. El objetivo principal es calcular la tasa de ingreso durante el primer año de TSR, describir las características principales de los mismos y estimar los costes que generan. Al realizar este análisis incluyendo las bases de datos oficiales, de cumplimentación obligatoria en los hospitales con cartera de servicios completa, podemos garantizar su exhaustividad, precisión y validez.
Material y métodosEste proyecto ha sido evaluado favorablemente por el Comité de Ética de la Investigación de referencia, aprobado por el Comité Técnico del Registro Madrileño de Enfermos Renales (REMER) y autorizado por la Consejería de Sanidad de la Comunidad de Madrid, que han considerado que el análisis planteado se alinea con los objetivos establecidos en la fundación del REMER4. El informe de la Oficina de Seguridad de Sistemas de Información Sanitaria (OSSI) garantiza que este estudio cumple con la Ley Orgánica de Protección de Datos (LOPD) mediante la implantación de un estricto protocolo que controla la ubicación y el acceso a las bases de datos y la anonimización de los registros de los pacientes mediante la disociación irreversible de sus datos personales y sus datos clínicos en fase previa a cualquier análisis o tratamiento estadístico.
Con el fin de asegurar la inclusión de todos los ingresos de un paciente dado, se analizan los 7 hospitales de la CM con cartera de servicios completa en TSR. Estos 7 hospitales atienden un área sanitaria de casi 3 millones de habitantes4 y el total de los TX realizados en la comunidad. Se han excluido para el análisis los TX realizados a pacientes de otras comunidades.
Se selecciona una cohorte de todos los pacientes incidentes en TSR durante los años 2013 y 2014. De acuerdo con los criterios REMER, definimos como paciente incidente el residente en la CM que comienza su primer TSR durante el periodo de estudio. No se descarta ningún paciente con mortalidad precoz. De esta cohorte seleccionamos a partir del CMBDH los ingresos realizados durante su primer año de TSR con independencia del motivo, del servicio de referencia y de la duración. Por tanto, disponemos de un seguimiento de un año desde la fecha de inicio del TSR, salvo que haya habido un evento previo (muerte o cambio de técnica TSR).
Si la diálisis (HD/DP) se inicia de forma no programada durante una hospitalización, este ingreso se analiza de forma independiente y no se incluye en los cálculos de tasas ni coste agregado, ya que es un ingreso previo a su primera diálisis ambulante. Tampoco se incluye en estos cálculos el ingreso para recibir un TX renal.
El CMBDH es una base de datos clínico-administrativa que registra todas las altas hospitalarias; para su análisis solo se tienen en cuenta los ingresos con estancias iguales o superior a un día. Tampoco se incluyen los episodios de atención en el servicio de urgencias que no generan un ingreso en planta.
Todos los diagnósticos y procedimientos del CMBDH están codificados según la Clasificación Internacional de Enfermedades, 9.ª Revisión, Modificación Clínica (CIE-9-MC). Todos los episodios se han agrupado con la versión 32.0 del sistema de clasificación de pacientes APR-GRD (all patients refined-Grupos Relacionados por el Diagnóstico [GRD]). El cambio del sistema de codificación (versión CIE-10) a partir del 1de enero de 2016 contribuye a justificar el límite temporal de cierre.
Del REMER se seleccionan las variables demográficas, de hospital, etiología y TSR de inicio. De la base de datos del CMBDH, por defecto, se integran todos los datos asociados al episodio de ingreso (fecha de ingreso y de alta, servicio de ingreso/alta, diagnostico principal, diagnósticos secundarios, procedimientos, categoría diagnóstica mayor [CDM], GRD, grado de severidad y riesgo de mortalidad del ingreso y los diagnósticos Present on Admission (POA), cualidad que establece si un diagnóstico estaba presente o no en el paciente al ingreso en el hospital. Si se produce un traslado interno entre dos servicios, consideramos como servicio de referencia el de alta.
El grado de severidad y riesgo de mortalidad se calcula a partir de la clasificación y agrupación de pacientes con APR-GRD. Esta novedosa clasificación permite comparar el riesgo de muerte esperable (por la gravedad) con la tasa de mortalidad real. Este tipo de análisis se está implantando progresivamente como un elemento más en el control de la calidad asistencial.
El índice de Charlson en el momento del ingreso se ha calculado a partir del CMBDH. Para ello utilizamos la modificación de Deyo sobre los diagnósticos recogidos en el CMBDH y los datos demográficos; se aplica una rutina del programa en Stata (charlson.ado) diseñado para registros médicos basados en la CIE-9-MC11. Sin embargo, la base de datos del REMER no incluye este índice de Charlson, por lo que no podemos realizar comparaciones con los pacientes que no hayan ingresado.
Para estimar la tasa de ingreso por enfermedad cardiovascular previa, se han considerado los diagnósticos POA agrupados bajo los siguientes códigos CIE9-MC: Cardiopatía isquémica (410-414), Otras formas de enfermedad cardiaca (420-429), Enfermedad cerebrovascular (430-438) y Enfermedades de las arterias, arteriolas y capilares (440-449).
EstadísticaLos resultados, en caso de variables de tipo cuantitativo, se expresan como media y desviación estándar (DE) o mediana y rangos intercuartílicos (RIC) si no sigue una distribución normal, o como porcentajes en caso de variables de tipo categórico. Las comparaciones entre variables cuantitativas se realizan con una t de Student si los datos siguen una distribución normal o con la U de Mann Whitney en caso de que no lo sean; diferencias entre variables categóricas se contrastan con una χ2 (chi-cuadrado). El tiempo de seguimiento se ha calculado como la diferencia entre fecha de inicio y fecha de fin de tratamiento (o 31dec2015 si el dato está censurado), excepto en el caso del trasplante, que se considera como inicio de TSR el día que se va de alta tras la cirugía para el trasplante. La tasa de ingreso se ha estimado como número de ingresos por paciente, y la tasa de ingreso por motivos cardiovasculares, como número de ingresos por paciente y año.
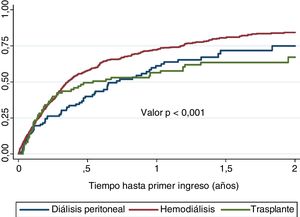
El tiempo hasta el primer ingreso se ha estimado mediante Kaplan-Meier, y las diferencias entre modalidades se han establecido con el test log-rank.
La base de datos del CMBDH imputa un coste para cada GRD al alta. Este coste es el valor medio más aproximado que considera todos los elementos de: hospitalización, personal, fármacos, procedimientos, diálisis ingresada y otras intervenciones. A partir de aquí realizamos las estimaciones de coste medio por ingreso, y por primer año de seguimiento en un paciente incidente en TSR. El coste por primer año se calcula dividiendo el coste de todos los ingresos por el número de pacientes que han iniciado TSR, con independencia de que hayan ingresado o no y de que hayan fallecido antes de completar su año de seguimiento.
Todos los análisis han sido realizados con Stata14 (StataCorp2015. Stata Statistical Software: Release 14. College Station, TX: StataCorp LP.X).
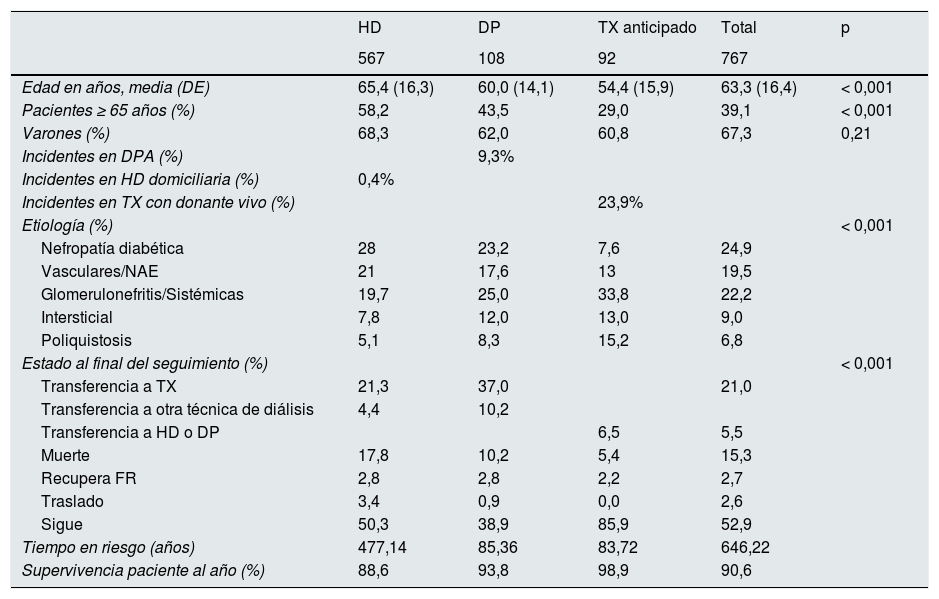
ResultadosDescripción de la cohorteDurante el periodo 2013-14 inician TSR un total de 767 pacientes, con la siguiente distribución por tratamiento: 108 en DP (14,1%), 567 en HD (73,9%) y 92 en TX (12,0%). La edad media es de 63,3años (DE: 16,42), siendo más jóvenes los que reciben un TX en prediálisis que los que inician por DP o HD (54,4 vs 60,0 vs 65,4años; p<0,001; tabla 1). La principal causa de ERC es la diabetes mellitus (DM; 24,9%), seguida por la nefroangioesclerosis (NAE)/vascular (19,5%) y las glomerulonefritis (16,7%).
Descriptivo de los pacientes incidentes en tratamiento sustitutivo renal
| HD | DP | TX anticipado | Total | p | |
|---|---|---|---|---|---|
| 567 | 108 | 92 | 767 | ||
| Edad en años, media (DE) | 65,4 (16,3) | 60,0 (14,1) | 54,4 (15,9) | 63,3 (16,4) | < 0,001 |
| Pacientes ≥ 65 años (%) | 58,2 | 43,5 | 29,0 | 39,1 | < 0,001 |
| Varones (%) | 68,3 | 62,0 | 60,8 | 67,3 | 0,21 |
| Incidentes en DPA (%) | 9,3% | ||||
| Incidentes en HD domiciliaria (%) | 0,4% | ||||
| Incidentes en TX con donante vivo (%) | 23,9% | ||||
| Etiología (%) | < 0,001 | ||||
| Nefropatía diabética | 28 | 23,2 | 7,6 | 24,9 | |
| Vasculares/NAE | 21 | 17,6 | 13 | 19,5 | |
| Glomerulonefritis/Sistémicas | 19,7 | 25,0 | 33,8 | 22,2 | |
| Intersticial | 7,8 | 12,0 | 13,0 | 9,0 | |
| Poliquistosis | 5,1 | 8,3 | 15,2 | 6,8 | |
| Estado al final del seguimiento (%) | < 0,001 | ||||
| Transferencia a TX | 21,3 | 37,0 | 21,0 | ||
| Transferencia a otra técnica de diálisis | 4,4 | 10,2 | |||
| Transferencia a HD o DP | 6,5 | 5,5 | |||
| Muerte | 17,8 | 10,2 | 5,4 | 15,3 | |
| Recupera FR | 2,8 | 2,8 | 2,2 | 2,7 | |
| Traslado | 3,4 | 0,9 | 0,0 | 2,6 | |
| Sigue | 50,3 | 38,9 | 85,9 | 52,9 | |
| Tiempo en riesgo (años) | 477,14 | 85,36 | 83,72 | 646,22 | |
| Supervivencia paciente al año (%) | 88,6 | 93,8 | 98,9 | 90,6 |
DE: desviación estándar; DP: diálisis peritoneal; DPA: diálisis peritoneal con cicladora; FR: función renal; HD: hemodiálisis; NAE: nefroangioesclerosis; TX: trasplante renal.
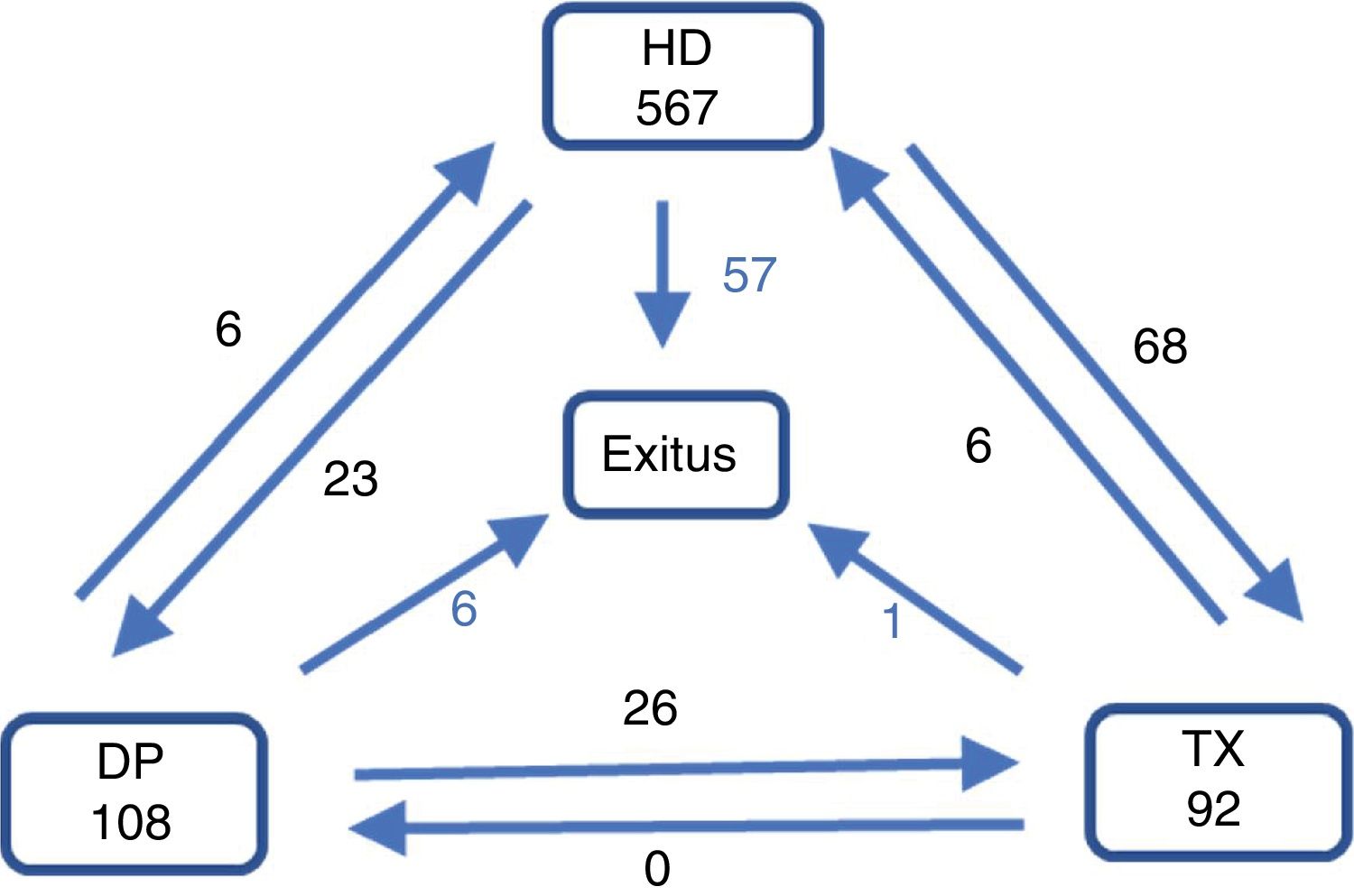
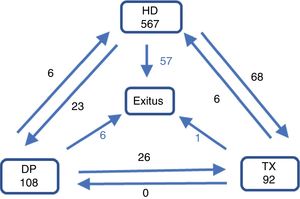
Al final del primer año, el 71,1% siguen en el mismo tratamiento, el 16,8% han cambiado (el 12,3% han sido TX), el 8,3% han fallecido, el 2,2% han recuperado función renal y del 1,6% se pierde seguimiento (fig. 1). El seguimiento acumulado es de 646,22años (0,8años/paciente).
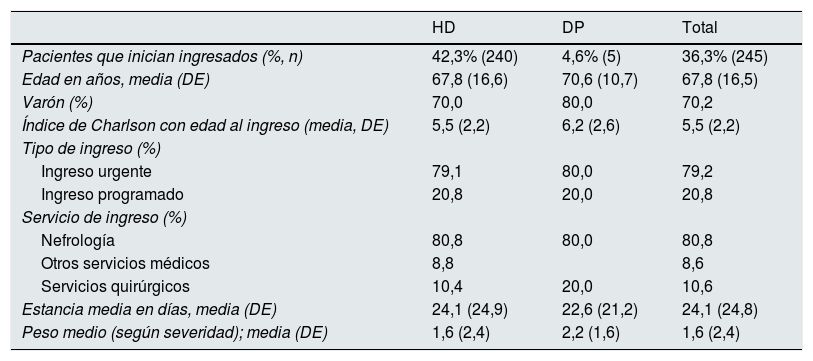
Ingresos para inicio en diálisisEl 36,3% de los incidentes en diálisis inician su TSR durante un ingreso hospitalario. Estos pacientes son mayores y con más comorbilidad, sobre todo en los que inician en DP. Hay un menor porcentaje de pacientes con poliquistosis renal (1,6 vs 6,8%) y más pacientes con enfermedad NAE/vascular como causa de su TSR (24,1 vs 19,5%) que en la cohorte incidente; el 37,6% son DM y el 60% tienen algún diagnóstico previo de enfermedad cardiovascular (tabla 2).
Descripción de las características de los pacientes que inician diálisis ingresados
| HD | DP | Total | |
|---|---|---|---|
| Pacientes que inician ingresados (%, n) | 42,3% (240) | 4,6% (5) | 36,3% (245) |
| Edad en años, media (DE) | 67,8 (16,6) | 70,6 (10,7) | 67,8 (16,5) |
| Varón (%) | 70,0 | 80,0 | 70,2 |
| Índice de Charlson con edad al ingreso (media, DE) | 5,5 (2,2) | 6,2 (2,6) | 5,5 (2,2) |
| Tipo de ingreso (%) | |||
| Ingreso urgente | 79,1 | 80,0 | 79,2 |
| Ingreso programado | 20,8 | 20,0 | 20,8 |
| Servicio de ingreso (%) | |||
| Nefrología | 80,8 | 80,0 | 80,8 |
| Otros servicios médicos | 8,8 | 8,6 | |
| Servicios quirúrgicos | 10,4 | 20,0 | 10,6 |
| Estancia media en días, media (DE) | 24,1 (24,9) | 22,6 (21,2) | 24,1 (24,8) |
| Peso medio (según severidad); media (DE) | 1,6 (2,4) | 2,2 (1,6) | 1,6 (2,4) |
DE: desviación estándar; DP: diálisis peritoneal; HD: hemodiálisis.
La estancia media (EM) de este primer ingreso es de 24,1días (DE: 24,8) y la EM ajustada por técnica es de 19,1días (DE: 11,7), sin diferencias entre DP y HD (p=0,6). La complejidad del ingreso calculada por peso medio es de 1,65 (DE: 2,39), más alto en DP que en HD (2,15 vs 1,64), y más de dos tercios de los ingresos son de severidad grave o muy grave.
La mayoría de los ingresos para inicio de TSR se realizan desde urgencias (79,2%) y solo un 20,8% son programados, con porcentajes muy similares en ambas técnicas (HD/DP). Son dados de alta por nefrología en un 80,8% y el motivo de ingreso está relacionado con enfermedades del aparato circulatorio (38,8%) o del sistema genitourinario (33,9%).
El 13,5% de los pacientes que inician TSR ingresados fallecen durante el primer año. La principal causa de mortalidad es de tipo infeccioso (42,4%), seguida por los motivos cardiovasculares (27,3%) y por cáncer (12,2%).
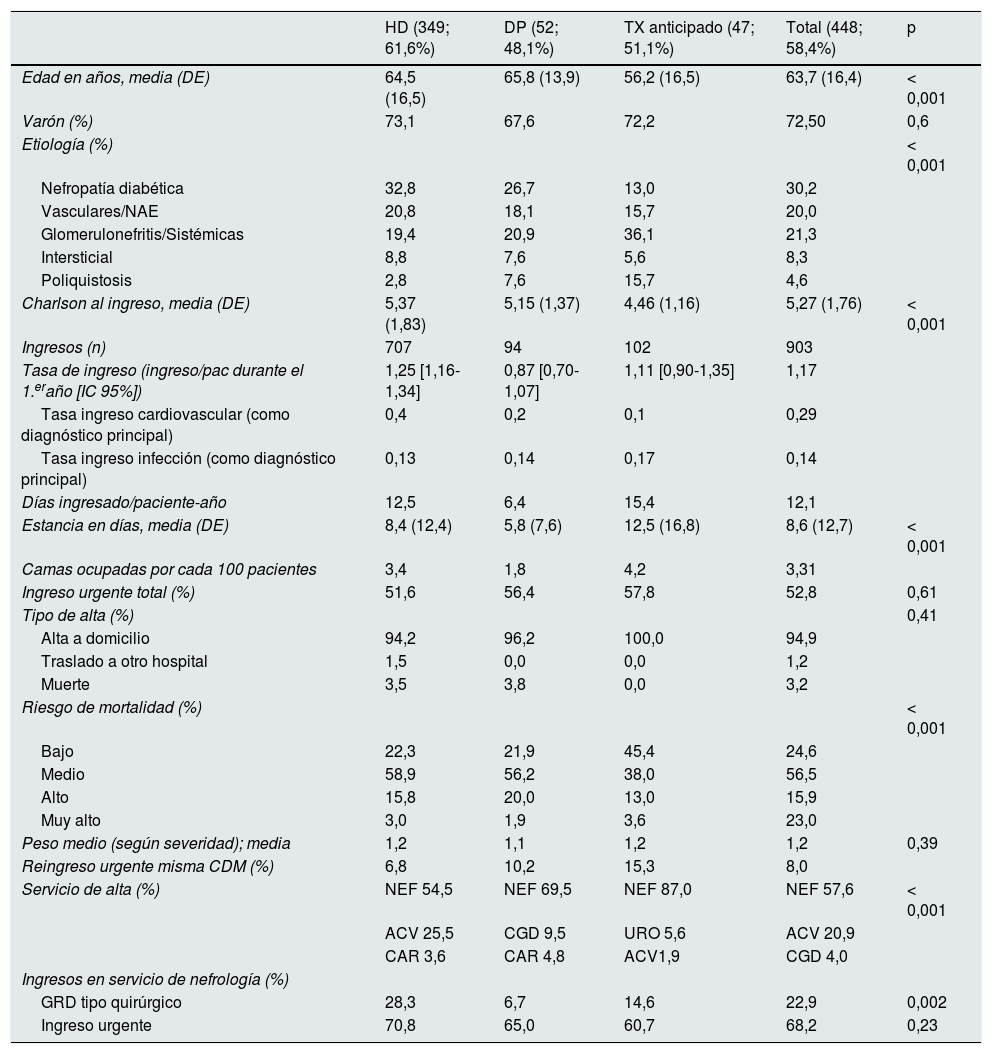
Ingresos durante el primer año en tratamiento sustitutivo renalDescartado tanto el ingreso para inicio como el ingreso para recibir un TX renal, durante el primer año de TSR ingresan el 58,4% de los pacientes. Se registran 903 ingresos: el 10,0% de pacientes en DP, el 78,0% de HD y el 11,0% de TX. La tasa de ingreso durante el primer año es de 1,18ingresos por paciente, y el número de días ingresado, estimado por paciente y año de seguimiento, es de 12,05días. La EM es de 8,6 días (DE: 12,7), más corta en incidentes en DP. Casi la mitad de los ingresos son urgentes y solo un 3,2% fallecen durante un ingreso (tabla 3).
Descripción de las características de los ingresos durante el primer año en tratamiento sustitutivo renal. Se excluye el ingreso para inicio de TSR
| HD (349; 61,6%) | DP (52; 48,1%) | TX anticipado (47; 51,1%) | Total (448; 58,4%) | p | |
|---|---|---|---|---|---|
| Edad en años, media (DE) | 64,5 (16,5) | 65,8 (13,9) | 56,2 (16,5) | 63,7 (16,4) | < 0,001 |
| Varón (%) | 73,1 | 67,6 | 72,2 | 72,50 | 0,6 |
| Etiología (%) | < 0,001 | ||||
| Nefropatía diabética | 32,8 | 26,7 | 13,0 | 30,2 | |
| Vasculares/NAE | 20,8 | 18,1 | 15,7 | 20,0 | |
| Glomerulonefritis/Sistémicas | 19,4 | 20,9 | 36,1 | 21,3 | |
| Intersticial | 8,8 | 7,6 | 5,6 | 8,3 | |
| Poliquistosis | 2,8 | 7,6 | 15,7 | 4,6 | |
| Charlson al ingreso, media (DE) | 5,37 (1,83) | 5,15 (1,37) | 4,46 (1,16) | 5,27 (1,76) | < 0,001 |
| Ingresos (n) | 707 | 94 | 102 | 903 | |
| Tasa de ingreso (ingreso/pac durante el 1.eraño [IC 95%]) | 1,25 [1,16-1,34] | 0,87 [0,70-1,07] | 1,11 [0,90-1,35] | 1,17 | |
| Tasa ingreso cardiovascular (como diagnóstico principal) | 0,4 | 0,2 | 0,1 | 0,29 | |
| Tasa ingreso infección (como diagnóstico principal) | 0,13 | 0,14 | 0,17 | 0,14 | |
| Días ingresado/paciente-año | 12,5 | 6,4 | 15,4 | 12,1 | |
| Estancia en días, media (DE) | 8,4 (12,4) | 5,8 (7,6) | 12,5 (16,8) | 8,6 (12,7) | < 0,001 |
| Camas ocupadas por cada 100 pacientes | 3,4 | 1,8 | 4,2 | 3,31 | |
| Ingreso urgente total (%) | 51,6 | 56,4 | 57,8 | 52,8 | 0,61 |
| Tipo de alta (%) | 0,41 | ||||
| Alta a domicilio | 94,2 | 96,2 | 100,0 | 94,9 | |
| Traslado a otro hospital | 1,5 | 0,0 | 0,0 | 1,2 | |
| Muerte | 3,5 | 3,8 | 0,0 | 3,2 | |
| Riesgo de mortalidad (%) | < 0,001 | ||||
| Bajo | 22,3 | 21,9 | 45,4 | 24,6 | |
| Medio | 58,9 | 56,2 | 38,0 | 56,5 | |
| Alto | 15,8 | 20,0 | 13,0 | 15,9 | |
| Muy alto | 3,0 | 1,9 | 3,6 | 23,0 | |
| Peso medio (según severidad); media | 1,2 | 1,1 | 1,2 | 1,2 | 0,39 |
| Reingreso urgente misma CDM (%) | 6,8 | 10,2 | 15,3 | 8,0 | |
| Servicio de alta (%) | NEF 54,5 | NEF 69,5 | NEF 87,0 | NEF 57,6 | < 0,001 |
| ACV 25,5 | CGD 9,5 | URO 5,6 | ACV 20,9 | ||
| CAR 3,6 | CAR 4,8 | ACV1,9 | CGD 4,0 | ||
| Ingresos en servicio de nefrología (%) | |||||
| GRD tipo quirúrgico | 28,3 | 6,7 | 14,6 | 22,9 | 0,002 |
| Ingreso urgente | 70,8 | 65,0 | 60,7 | 68,2 | 0,23 |
CDM: categoría diagnóstica mayor; DE: desviación estándar; DP: diálisis peritoneal; GRD: grupos relacionados por el diagnóstico; HD: hemodiálisis; IC: intervalo de confianza; NAE: nefroangioesclerosis; TSR: tratamiento sustitutivo renal; TX: trasplante renal.
La edad media de los ingresados es de 63,7años (DE: 16,4), con un Índice de Charlson de 5,3 (DE: 1,8). Los trasplantados son más jóvenes que los que inician por diálisis (p<0,001) y tienen un menor Índice de Charlson (tabla 3). Un tercio de los ingresos son de pacientes con diagnóstico de DM (30,2%), seguidos por los diagnosticados de NAE/vascular (20%) o glomerulonefritis (15,3%).
La tasa de ingreso por motivos cardiovasculares es de 0,29ingresos/paciente-año, más baja en los TX renales que en pacientes en diálisis (HD/DP). La tasa de ingreso por infección de cualquier origen es de 0,14ingresos/paciente-año. y por infección peritoneal en DP, de 0,13ingresos/paciente-año. Los 11 casos de ingreso por peritonitis tienen una EM de 4,6días (DE: 3,2), con un rango de 1-10días, todos con nivel de severidad 3-4, pero sin ningún fallecimiento. En los pacientes en HD la tasa de ingreso por infección es 0,14ingresos/paciente-año; la distribución es: 28,3% infección respiratoria, 19,8% infección del acceso vascular y 10,4% infección urinaria. Ninguna de ellas fue causa de fallecimiento.
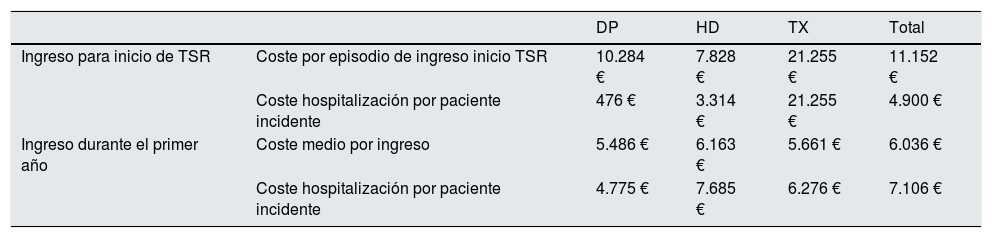
El coste medio de los ingresos el primer año (tabla 4), estimado en paciente incidente y según el GRD y el nivel de severidad, es de 5.251€ en DP, 10.999€ en HD y 27.531€ en TX (incluyendo los 21.255€ por realizar el trasplante).
Coste de los ingresos durante el primer año
| DP | HD | TX | Total | ||
|---|---|---|---|---|---|
| Ingreso para inicio de TSR | Coste por episodio de ingreso inicio TSR | 10.284 € | 7.828 € | 21.255 € | 11.152 € |
| Coste hospitalización por paciente incidente | 476 € | 3.314 € | 21.255 € | 4.900 € | |
| Ingreso durante el primer año | Coste medio por ingreso | 5.486 € | 6.163 € | 5.661 € | 6.036 € |
| Coste hospitalización por paciente incidente | 4.775 € | 7.685 € | 6.276 € | 7.106 € |
DP: diálisis peritoneal; HD: hemodiálisis; TX: trasplante renal.
Coste por ingreso es el coste total dividido por el número de ingresos. Coste por incidente es el coste total entre el número de incidentes, ingresen o no.
El criterio de reingreso urgente y por la misma categoría diagnóstica solo representa el 8% de los ingresos (6,8% en HD vs 10,2% en DP vs 15,3% en TX). Los GRD más frecuentes en los reingresos son «malfuncionamiento, reacción o complicación de dispositivo, injerto o trasplante genitourinario» (10,0%) e «insuficiencia renal» (9,1%).
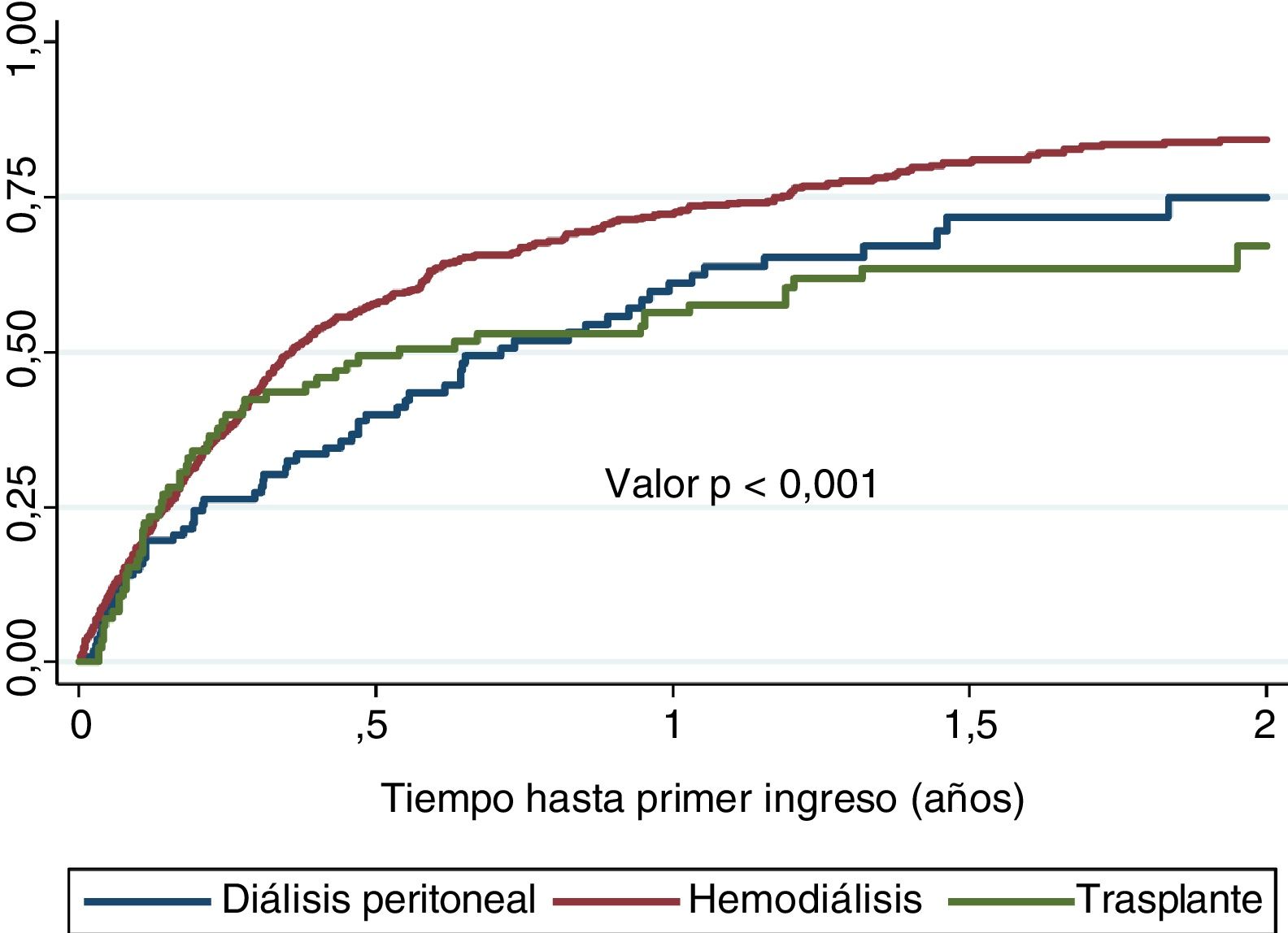
Estimamos por Kaplan-Meier el tiempo trascurrido desde el inicio de TSR hasta el primer ingreso en 147días (IC95%: 128-176). Si comparamos por técnicas, la HD tiene el ingreso más precoz: 131días en HD (IC95%: 116-151), 260 en DP (IC95%: 177-363) y 197 en TX (IC95%: 88-435) (log-rank 14,57; p<0,001) (fig. 2).
DiscusiónEste trabajo es el primero que analiza el impacto que tiene el primer año de TSR en los hospitales de tercer nivel de toda una comunidad autónoma. Se analizan de forma conjunta todos los ingresos, independientemente de la indicación, servicio u hospital en el que se realizan, agrupando bases de datos oficiales, públicas y de obligado cumplimiento en un país en el que el TSR está cubierto prácticamente al 100% por la sanidad pública. Hemos conseguido estimaciones precisas y actuales sobre las tasas de ingreso, sus características y costes, que podrían ser de gran valor en la toma de decisiones de planificación, asignación de recursos y desarrollo de vías clínicas y referencias para planes de calidad. Por la metodología empleada, no se puede conocer la carga asistencial/económica que generan las urgencias, o la atención en consultas de otras especialidades, ya que esta información no está incluida en el CMBDH.
Como el riesgo de ingreso no es constante a lo largo del tiempo en TSR, nos hemos centrado en el primer año. En nuestro estudio, más de la mitad de los pacientes ingresaron durante su primer año en TSR, con una tasa de más de 1,5ingresos/paciente (0,36para el inicio ingresado y 1,17 durante el primer año) que genera un coste anual de más de 12.000€ por paciente. Los incidentes en HD ingresan con mayor frecuencia en su mayoría por urgencias, posiblemente por su mayor edad y comorbilidad.
La tasa de ingreso descrita es mayor que la estimada por el Dialysis Outcomes and Practice Patterns Study (DOPPS) para el promedio de España y Europa12. Sin embargo, debemos considerar que el diseño es diferente, pues DOPPS solo registra datos de pacientes prevalentes en HD y desde la perspectiva del nefrólogo, con ingresos en su propio servicio y como un registro voluntario. Lo mismo sucede con las publicaciones de centros de HD concertada, donde existe una selección positiva de pacientes menos comórbidos y posiblemente un registro parcial de los ingresos13. No debemos olvidar que los estudios sobre pacientes prevalentes tienen siempre un sesgo favorable de supervivencia de aquellos con menor riesgo que no han fallecido en fases precoces del tratamiento.
Frente a ello, los datos del CMBDH incluyen la totalidad de ingresos por cualquier causa y en cualquier servicio (más de 40% fuera de nefrología), por lo que consideramos que esas publicaciones infraestiman la tasa de hospitalización14,15.
Nuestro enfoque se centra en el primer año de TSR, cuando la tasa de ingreso es potencialmente mayor14,16,17, sobre todo en los 3 primeros meses9. De hecho, algunos países excluyen de sus registros TSR los pacientes que fallecen en los 3 primeros meses (p.e., Estados Unidos de América: USRD)17. Los que son transferidos a otras técnicas o fallecen en esta fase inicial podrían ser los de mayor comorbilidad y edad, con ingresos más frecuentes, que no se contemplan en esos registros17. También se sabe que una referencia tardía a nefrología, así como el inicio no programado de la HD sin un acceso vascular definitivo, incrementaba el riesgo de hospitalización en los 3 primeros meses tras el inicio de TSR16. Aunque nuestros datos no van más allá del primer año, las técnicas domiciliarias (DP y TX) son las que tienen una tasa de ingreso más baja.
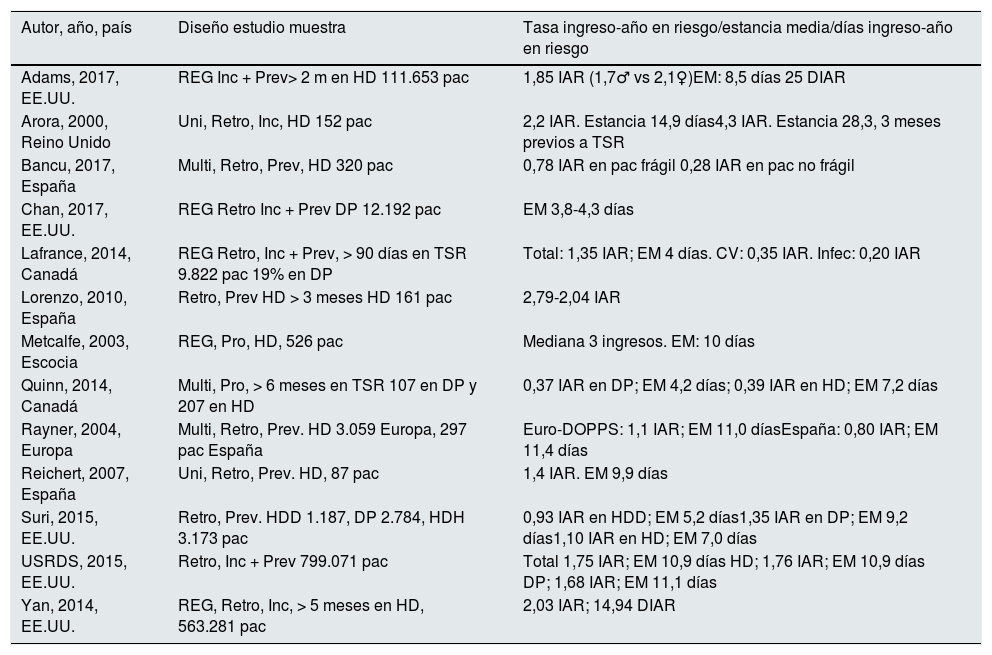
La tabla 5 recoge un resumen de las principales referencias publicadas sobre los ingresos hospitalarios asociados a TSR. En ella detallamos el tipo de estudio, país, año y tamaño muestral, aspectos que son muy relevantes a la hora de realizar comparaciones. Para entender la tremenda variación en tasas, estancias y resultados hay que considerar al menos los siguientes aspectos metodológicos:
- 1.
El modelo sanitario del país de referencia con la diferente accesibilidad a técnicas de TSR y el financiador del tratamiento.
- 2.
Las técnicas de diálisis consideradas.
- 3.
La referencia hospitalaria, de centro, o de registro territorial.
- 4.
El perfil y los criterios de inclusión de pacientes.
- 5.
El momento de seguimiento (primer año o prevalentes).
- 6.
El enfoque desde servicio de nefrología o global.
- 7.
La cumplimentación voluntaria u obligatoria (registros), así como el perfil clínico o administrativo del personal encargado de la recogida de las variables.
Principales estudios para estimar tasas de ingreso en TSR desde 2000 hasta 2017
| Autor, año, país | Diseño estudio muestra | Tasa ingreso-año en riesgo/estancia media/días ingreso-año en riesgo |
|---|---|---|
| Adams, 2017, EE.UU. | REG Inc + Prev> 2 m en HD 111.653 pac | 1,85 IAR (1,7♂ vs 2,1♀)EM: 8,5 días 25 DIAR |
| Arora, 2000, Reino Unido | Uni, Retro, Inc, HD 152 pac | 2,2 IAR. Estancia 14,9 días4,3 IAR. Estancia 28,3, 3 meses previos a TSR |
| Bancu, 2017, España | Multi, Retro, Prev, HD 320 pac | 0,78 IAR en pac frágil 0,28 IAR en pac no frágil |
| Chan, 2017, EE.UU. | REG Retro Inc + Prev DP 12.192 pac | EM 3,8-4,3 días |
| Lafrance, 2014, Canadá | REG Retro, Inc + Prev, > 90 días en TSR 9.822 pac 19% en DP | Total: 1,35 IAR; EM 4 días. CV: 0,35 IAR. Infec: 0,20 IAR |
| Lorenzo, 2010, España | Retro, Prev HD > 3 meses HD 161 pac | 2,79-2,04 IAR |
| Metcalfe, 2003, Escocia | REG, Pro, HD, 526 pac | Mediana 3 ingresos. EM: 10 días |
| Quinn, 2014, Canadá | Multi, Pro, > 6 meses en TSR 107 en DP y 207 en HD | 0,37 IAR en DP; EM 4,2 días; 0,39 IAR en HD; EM 7,2 días |
| Rayner, 2004, Europa | Multi, Retro, Prev. HD 3.059 Europa, 297 pac España | Euro-DOPPS: 1,1 IAR; EM 11,0 díasEspaña: 0,80 IAR; EM 11,4 días |
| Reichert, 2007, España | Uni, Retro, Prev. HD, 87 pac | 1,4 IAR. EM 9,9 días |
| Suri, 2015, EE.UU. | Retro, Prev. HDD 1.187, DP 2.784, HDH 3.173 pac | 0,93 IAR en HDD; EM 5,2 días1,35 IAR en DP; EM 9,2 días1,10 IAR en HD; EM 7,0 días |
| USRDS, 2015, EE.UU. | Retro, Inc + Prev 799.071 pac | Total 1,75 IAR; EM 10,9 días HD; 1,76 IAR; EM 10,9 días DP; 1,68 IAR; EM 11,1 días |
| Yan, 2014, EE.UU. | REG, Retro, Inc, > 5 meses en HD, 563.281 pac | 2,03 IAR; 14,94 DIAR |
CV: cardiovascular; DIAR: días ingreso/año en riesgo; DP: diálisis peritoneal; EM: estancia media; HD: hemodiálisis; IAR: ingresos por paciente y año en riesgo; Inci: incidentes; Multi: multicéntrico; pac: pacientes; Pre: prevalencia; Pro: prospectivo; REG: registro; Retro: retrospectivo; Uni: un solo centro.
Solo unas pocas publicaciones analizan este tema en la realidad española, casi siempre con enfoques parciales. Los clásicos estudios de Górriz et al.18 y Gallego et al.19 en los primeros años de este siglo se centraban en el impacto del seguimiento de la enfermedad renal crónica avanzada (ERCA) sobre el inicio programado de HD, y el estudio de Remón et al.20 se limita a la infección peritoneal en DP. Ninguno de ellos permite estimar tasas de ingreso anuales en TSR incidente. Los interesantes estudios de Reichert21 y Lorenzo et al.22 se centran en HD, y al ser de un solo centro, son difícilmente generalizables. El estudio de Conde et al.23 es pionero al estimar el impacto de la hospitalización en el coste del TSR, pero una vez más puede ser poco generalizable por incluir pacientes de un solo centro.
Descripción de los ingresos durante el primer año en tratamiento sustitutivo renalLa edad media de los incidentes, al igual que en otros registros4, está aumentando progresivamente, siendo incluso más alta que la referencia publicada por el grupo centro de DP (GCDP)24. La etiología de la enfermedad renal es similar a la descrita por el REER a nivel nacional5, con una elevada prevalencia de DM. Sin embargo, destaca un mayor porcentaje de glomerulonefritis y poliquistosis tanto en DP como en TX; los pacientes poliquísticos tienen un diagnóstico más precoz y son seguidos con frecuencia en consultas de ERC avanzada, por lo que es más fácil que inicien en DP o sean trasplantados sin pasar por diálisis25.
Considerando las diferencias por técnicas, los incidentes en DP son los que tienen una EM inferior, y los que reciben un TX son los que tienen una EM más alta. Si comparamos con las referencias norteamericanas, sus EM son más prolongadas en DP y mucho más cortas en el paciente trasplantado. La explicación se encuentra en las diferencias del modelo sanitario, con una aceptación de receptores de mayor edad y comorbilidad, una mayoría de donantes de criterio expandido frente al trasplante de vivo y perfil de selección de donante y receptor del modelo de Estados Unidos17. Los registros americanos de HD recogen una EM inferior a la nuestra, pero recordemos que las referencias se refieren a pacientes prevalentes tras descartar los que fallecen en los primeros 3meses.
Muchos registros autonómicos no recogen información de los ingresos en TSR (p.ej., el REMER), y si lo hacen, no publican análisis en este campo. Tan solo el registro de del País Vasco comunica datos sobre ingresos hospitalarios, con una EM de 11días en DP, 13días en TX y 14,5días en HD en 2008 en un centro concertado26.
La mayoría de los ingresos se realizan en el servicio de nefrología, incluso en casos en los que se recoge un GRD quirúrgico. Posiblemente este hecho deriva de la complejidad de manejo de nuestros pacientes y la dependencia que tienen de sus responsables médicos, que hacen más fácil que el cirujano haga su seguimiento integrado dentro de un ingreso en nuestro servicio médico.
La Consejería de Sanidad de la Comunidad de Madrid considera los reingresos urgentes por la misma categoría diagnóstica, en menos de 30días tras el alta, como un indicador de alta precoz e inadecuada y se incluye como objetivo de calidad asistencial. En nuestro estudio representan menos del 10% de ingresos, con un porcentaje más alto en TX que en DP o HD, posiblemente porque parte de las incidencias pueden ser tratadas/revisadas en la unidad de HD, en un modelo informal de continuidad asistencial post-alta. Este dato es mejor que en estudios canadienses (17,2% en HD)27 o en norteamericanos (34% global, 37% en HD)17. Otro trabajo realizado únicamente en pacientes en DP28 estima un 14,6% de reingresos a los 30días. En ese caso, los motivos de ingreso más relevantes son infarto, complicaciones de procedimientos y DM frente a complicación de dispositivo, injerto o trasplante en nuestra serie.
Un elemento de análisis reciente permite estimar los riesgos de complicaciones y/o mortalidad en función de los diagnósticos presentes en el momento del ingreso para un GRD dado, clasificándolos en 4 categorías. La comparación con la mortalidad real en cada categoría nos da una herramienta de análisis sobre nuestra calidad asistencial durante el ingreso10; en nuestro estudio, para cada GRD se obtuvo una mortalidad que fue inferior a la esperada. No hemos encontrado ninguna publicación que analice este aspecto para pacientes con ERC y/o TSR.
Inicio ingresadoEl inicio programado, ambulante y tras un seguimiento reglado en consultas de ERCA es un objetivo primordial del Plan Estratégico de Nefrología de nuestra comunidad29. Sin embargo, más de un tercio inician TSR de forma ingresada. Este inicio ingresado se considera como una situación subóptima18,19, y en series más antiguas se sitúa en torno al 50%18,30 o incluso el 75% de los casos en una referencia previa a la generalización de las consultas ERCA9.
Aunque otros países han publicado experiencias de inicio urgente de DP31, el inicio no programado de TSR se realiza casi siempre por HD en nuestro país, lo que justifica las diferentes tasas encontradas en nuestro estudio para ambas técnicas. Si el paciente había elegido DP, se le puede proponer transferencia precoz a DP tras estabilizar su situación con HD de inicio urgente18. Los pacientes que inician su diálisis de forma ingresada son más mayores que el resto de la cohorte incidente, sobre todo en DP, donde la diferencia es de casi 10años. Lamentablemente, no podemos analizar el impacto de la comorbilidad en la tasa de ingresos, pues solo disponemos de ese dato para los pacientes que han ingresado.
En nuestro estudio, el ingreso de inicio de diálisis conlleva una estancia superior a 2semanas frente al resto de ingresos posteriores, de forma similar a lo observado en el estudio sobre inicio no programado de diálisis previamente referenciado19.
Un inicio no programado contribuye a la utilización de catéteres vasculares19 que se asocia a una mayor tasa de hospitalización por infecciones8 y, por tanto, a un mayor coste18, además de comprometer la supervivencia del paciente durante el primer año8,18. El 13,5% de los pacientes que iniciaron diálisis de forma ingresada han fallecido en el primer año, casi el doble de los que no iniciaron ingresados, lo que concuerda con referencias previamente publicadas18,19.
CostesEl estudio de consumo de recursos no es el objetivo principal de este estudio, pero constituye una gran oportunidad para estimar este elemento de coste, que con frecuencia es infravalorado. En efecto, el coste de la técnica de diálisis, de la farmacia e incluso del trasporte ha sido estimado con bastante precisión en nuestro país y ha servido para definir una estrategia de apoyo al desarrollo de las técnicas domiciliarias7,32. Habitualmente se considera la referencia de coste anual de 45.170€ para la HD de centro, 61.280€ la hospitalaria, 33.255€ la DP y 11.766€ en TX, promediando el impacto del primer año en la vida media del injerto y paciente6. Sin embargo, en estos estudios no se considera el peso presupuestario de la atención hospitalizada, o si lo hacen, se utiliza un coste estándar33 en vez de emplear los costes asociados a los GRD22,23.
Nuestros cálculos son muy precisos, ya que emplean el coste por GRD real y no un fijo por día de ingreso sobre las estimaciones de EM. A los datos referidos del coste del TSR deberíamos sumarle más de 7.000€ por paciente incidente el primer año, más otros casi 5.000€ si el inicio de diálisis se realiza ingresado. En el apartado de resultados detallamos los costes por cada una de las técnicas de TSR y el sobrecoste del inicio ingresado/no programado. Estas referencias son de gran valor para la planificación y para el desarrollo de modelos predictivos del impacto económico de intervenciones que potencien técnicas domiciliarias34 o el inicio programado de diálisis con la creación de consultas ERCA y la aplicación de modelos de calidad.
Pero mientras llega la esperada revolución de la gestión clínica real y la planificación de la política sanitaria basada en costes y resultados de las intervenciones, podemos estimar que, a día de hoy y en nuestro medio, entre el 9 y el 17% del coste del TSR corresponde a gastos hospitalarios14,23,33.
No debemos olvidar que nuestro estudio se centra en el primer año de TSR, y que podría ser diferente en los siguientes años y explicar así por qué es menor en otras referencias sobre pacientes prevalentes23.
Limitaciones y fortalezasCon el fin de garantizar la inclusión de todos los ingresos de un paciente dado y analizar el tratamiento integrado, solo se han analizado los hospitales de la CM con cartera de servicios completa. La inclusión de hospitales de menor complejidad, que no disponen de trasplante o de guardias, aumentaría la potencia estadística pero dificultaría los análisis por ingresos cruzados entre hospitales. Este aspecto debe considerarse para la extrapolación de resultados a hospitales de menor nivel de complejidad o con cartera de servicios parcial. Para considerar el impacto del TSR a nivel hospitalario de modo integral deberíamos incluir los episodios de urgencia, que no pueden extraerse del CMBDH. Pero una de las ventajas de este análisis es que por su naturaleza engloba al 100% de los pacientes incidentes en TSR, así como todos sus ingresos en el ámbito de la CM.
Oportunidad perdida de análisis para la gestiónNuestro artículo aprovecha la oportunidad de analizar información ya disponible que permita generar nuevas hipótesis que abran caminos para investigar. Las limitaciones hasta ahora han sido de tipo organizativo, nunca técnico.
En los últimos años los datos de tipo sanitario se han incrementado exponencialmente y han ido aumentando las publicaciones médicas que incluyen el término «big data». Sin embargo, antes de analizar la información no estructurada, antes de «bucear en los lagos de datos», deberíamos aprovechar las bases de datos estructuradas ya disponibles para obtener información relevante sobre el efecto real de nuestras intervenciones en salud. Disponemos de bases de datos de titularidad pública, de obligado cumplimiento, amparadas legalmente y con frecuencia dependientes de una misma dirección general en nuestras consejerías de Sanidad. Integrando registros nacionales, autonómicos, hospitalarios, incluso bases de datos clínicas, de laboratorio, etc., y analizándolas de forma conjunta, se puede obtener mucha más información de la que disponemos hoy en día. Generemos información a partir de los datos estructurados y conocimiento a partir de la información. Sobre ella podremos diseñar y desplegar planes de atención sanitaria integrada y comprobar sus efectos en la salud de nuestra población, mejorando la gestión, los resultados y el cuidado de nuestros pacientes.
ConclusionesHemos realizado estimaciones precisas de las tasas, características y costes de los ingresos en el primer año del TSR. La validez interna está asegurada por el método de análisis y la procedencia de los datos y pueden dar soporte a la gestión local hospitalaria y a la generación de planes estratégicos a nivel autonómico y nacional. El impacto del TSR en la actividad hospitalaria estaba infraestimado y es muy relevante para la estimación del coste global del TSR. Los resultados de la literatura internacional no pueden extrapolarse a la realidad de nuestro país o autonomía por las diferencias en modelo sanitario, criterios de inclusión, perfil de paciente o aspectos metodológicos varios.
La integración de bases de datos clínicas es técnicamente viable, podría abrir una vía inmensa de información y solo requiere de apoyo institucional para su desarrollo.
Conflicto de interesesNinguno.
Queremos agradecer el apoyo de las Juntas Directivas de la Sociedad Madrileña de Nefrología (SOMANE) 2012-2018, de los jefes de servicio de los hospitales implicados y de todo el personal que con su trabajo diario contribuye a la generación y conservación de los registros REMER y CMBDH en servicios centrales de la Consejería de Salud, así como los servicios clínicos y de admisión de los hospitales.