La insuficiencia cardiaca (IC) es una comorbilidad frecuente y de gran impacto pronóstico en pacientes con enfermedad renal crónica (ERC). Sin embargo, las prácticas para el cribado y diagnóstico de la IC en las consultas de Nefrología no están optimizadas. El objetivo fue evaluar la práctica clínica habitual y detectar lagunas en el diagnóstico de IC en la atención a pacientes con ERC en cualquier estadio.
MétodosSe realizó una encuesta nacional a nefrólogos españoles a través de un cuestionario electrónico. La recogida de datos se realizó durante dos meses.
ResultadosUn total de 73 centros completaron el cuestionario. La prevalencia estimada de IC entre los pacientes atendidos fue del 44,1%, aunque se estimó que solo el 30% de estos casos estaban documentados en la historia clínica. Aunque el 55,4% de los encuestados refirió realizar cribado activo, el uso de herramientas diagnósticas como la ecocardiografía, los péptidos natriuréticos y el electrocardiograma fue variable y con frecuencia condicionado a la presencia de síntomas.
ConclusiónEstos resultados sugieren la conveniencia de avanzar hacia estrategias protocolizadas e interdisciplinares que optimicen el diagnóstico de la IC, como en la instauración precoz de terapias adecuadas para la IC en pacientes con ERC.
Heart failure (HF) is a common comorbidity with a major prognostic impact in patients with chronic kidney disease (CKD). However, screening and diagnostic practices for HF in nephrology clinics are not optimized. The aim was to assess routine clinical practice and identify gaps in HF diagnosis in the care of patients with CKD at any stage.
MethodsA nationwide survey of Spanish nephrologists was conducted using an electronic questionnaire. Data collection took place over a two-month period.
ResultsA total of 73 centers completed the questionnaire. The estimated prevalence of HF among the patients seen was 44.1%, although only 30% of these cases were thought to be documented in the medical record. Although 55.4% of respondents reported performing active screening, the use of diagnostic tools such as echocardiography, natriuretic peptides, and electrocardiography was variable and often conditioned by the presence of symptoms.
ConclusionThese findings support a call to action based on the need to implement protocolized, multidisciplinary strategies to optimize HF diagnosis, as well as the early initiation of appropriate therapies for HF in patients with chronic kidney disease
La insuficiencia cardiaca (IC) y la enfermedad renal crónica (ERC) coexisten con frecuencia debido a mecanismos fisiopatológicos comunes y a factores de riesgo compartidos, lo que se conoce como síndrome cardiorrenal1,2. En la población general, la prevalencia de IC se estima en torno al 1-2%, alcanzando cifras cercanas al 10% en mayores de 70 años3. Los datos del estudio ARIC muestran que los individuos con una tasa de filtrado glomerular estimada (FGe) <60mL/min/1,73 m2 tienen casi el doble de riesgo de desarrollar IC en comparación con aquellos con función renal normal4. En pacientes con ERC avanzada, estudios recientes muestran que más del 90% están en estadio B o C de IC, incluso sin diagnóstico previo5. La IC en pacientes con ERC se asocia a mayor mortalidad y hospitalización, con infradiagnóstico documentado en registros nacionales como HAKA o CONREN6,7. Por ello, la detección precoz de la IC en pacientes con ERC es clave para mejorar su pronóstico, pero los servicios de Nefrología carecen de protocolos estandarizados para su cribado y diagnóstico. Además, el diagnóstico precoz va mucho más allá de la identificación de signos clínicos de congestión, y requiere una evaluación multiparamétrica que incluya criterios morfológicos y funcionales ecocardiográficos, así como el uso de biomarcadores tal y como se indica en las actuales guías para el diagnóstico y manejo de la IC8,9. La IC sigue infradiagnosticada y, en consecuencia, infra-tratada en esta población de pacientes, a pesar de la disponibilidad de tratamientos modificadores del pronóstico. Algunos estudios han demostrado que, en pacientes con comorbilidades como la ERC, incluso cuando se sospecha clínicamente la IC, esta no se recoge formalmente en la historia clínica, lo que contribuye a la inercia terapéutica y al empeoramiento pronóstico6,10.
La brecha diagnóstica y terapéutica también se refleja en los resultados del estudio HAKA6, que evaluó a 5.012 pacientes con ERC avanzada en 29 centros españoles. En este trabajo, solo el 13% de los pacientes tenía diagnóstico de IC, con una alta variabilidad intercentros (rango del 2 al 44%), lo que sugiere una tasa muy relevante de infra-diagnóstico. Además, únicamente el 9,3% de los pacientes con IC con fracción de eyección reducida (IC-FEr) recibía tratamiento óptimo con las cuatro clases terapéuticas recomendadas (aunque la tasa de fracaso terapéutico probablemente esté desvirtuada por la limitación del uso de algunos fármacos como los antagonistas del receptor mineralocorticoideo en FGe <30mL/min/1,73 m2); y ninguno de los pacientes con ERC G5 alcanzaba el objetivo de un tratamiento optimizado acorde a su FGe y a las guías entonces vigentes. La tasa de infra-tratamiento era especialmente importante en pacientes con ERC e IC con fracción de eyección preservada o ligeramente reducida.
El problema no es unidireccional, ya que la ERC sigue estando infradiagnosticada en los pacientes con IC establecida. En este sentido, el registro CARDIOREN ha puesto de manifiesto la alta prevalencia de ERC en pacientes con IC y la escasa aplicación de terapias basadas en la evidencia2.
Ante la escasez de estudios que analicen cómo se evalúa la IC en pacientes con ERC, decidimos realizar una encuesta nacional con el objetivo de identificar los patrones clínicos seguidos por los nefrólogos en España.
Material y métodosSe diseñó una encuesta online, anónima (con opción de identificación voluntaria), que fue distribuida entre los miembros de la Sociedad Española de Nefrología (SEN). El cuestionario constaba de preguntas cerradas centradas en datos demográficos, ámbito asistencial, prevalencia estimada de IC en la población atendida en Nefrología, herramientas utilizadas para el diagnóstico, presencia de unidades cardiorrenales y comorbilidades más frecuentemente asociadas (tabla suplementaria 1).
Asimismo, se incluyeron ítems sobre la frecuencia de uso de técnicas diagnósticas (ecocardiograma, electrocardiograma, péptidos natriuréticos), prácticas de valoración clínica y registro del diagnóstico de IC en la historia clínica. La recogida de datos se llevó a cabo durante un periodo de dos meses. Se realizó un análisis descriptivo, presentando los resultados como porcentajes, medias y desviaciones estándar, según correspondiera. Para explorar diferencias entre grupos se aplicaron pruebas de chi-cuadrado para variables categóricas. Además, se llevó a cabo un análisis exploratorio mediante regresión logística binaria para identificar posibles factores asociados a la realización de cribado activo de IC, incluyendo como variables independientes la edad, el sexo, la existencia de unidad cardiorrenal en el centro y el número de pacientes atendidos mensualmente.
Todo el análisis estadístico se realizó con Stata v14.0 (StataCorp, College Station, TX, USA).
ResultadosUn total de 74 nefrólogos correspondientes a 73 centros completaron la encuesta. Más de la mitad de los participantes (55,4%) desarrollaban su labor asistencial en centros con unidad cardiorrenal, lo que resulta especialmente relevante para el objetivo del estudio. La edad media de los encuestados fue de 47,1 (DE 10,9) años y el 73% eran mujeres, en línea con la tendencia de feminización de la especialidad descrita en la SEN.
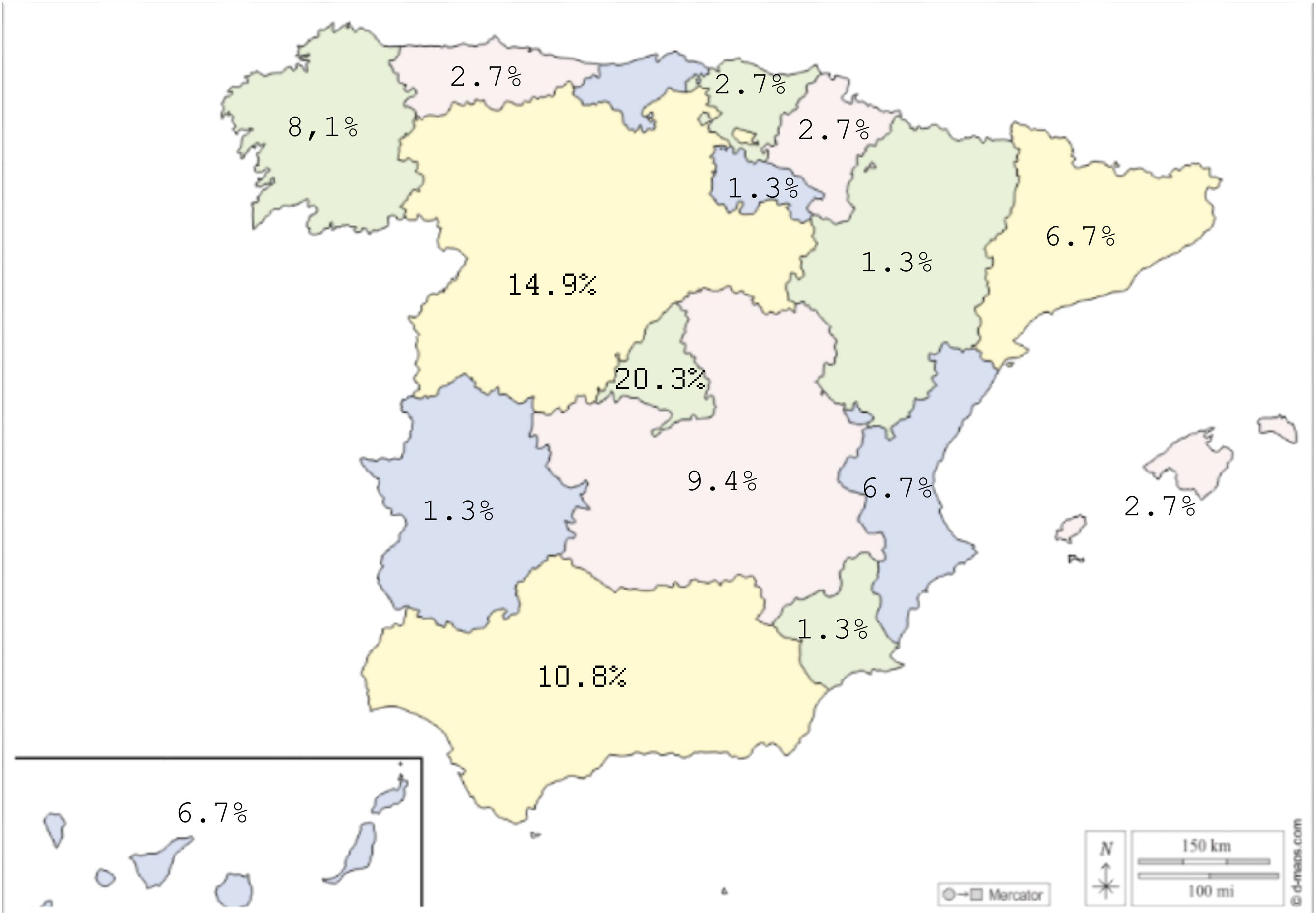
La distribución geográfica de los encuestados mostró una mayor participación desde la Comunidad de Madrid (20,3%), Castilla y León (14,9%) y Andalucía (10,8%), seguidas de Castilla-La Mancha (9,5%), Galicia (8,1%), Cataluña (6,8%), Canarias (6,8%) y Comunidad Valenciana (6,8%). El análisis comparado con la población general según el Instituto Nacional de Estadística evidenció diferencias significativas (χ2=33,97; p= 0,005), con sobrerrepresentación de algunas comunidades y menor representación de otras (fig. 1). De forma similar, la comparación con la distribución de los miembros de la SEN también mostró diferencias estadísticamente significativas (χ2=28,17; p=0,02) destacando la sobrerrepresentación de Castilla y León y Castilla-La Mancha, y la infrarrepresentación de Andalucía, Cataluña y la Comunidad Valenciana. Cantabria no registró participación a pesar de contar con miembros en la SEN.
El número medio estimado de pacientes atendidos mensualmente por cada encuestado fue de 135,8 (DE: 81,3). El análisis de las áreas de actividad asistencial de los encuestados mostró que la mayoría trabajaba en más de un ámbito de la nefrología. Concretamente, el 59,5% refirió desarrollar su labor en más de un área, siendo las combinaciones más frecuentes la atención a pacientes en diálisis y ERCA (16,2%), así como consulta externa, diálisis y ERCA (5,4%). La prevalencia estimada de IC en los pacientes atendidos en las consultas de Nefrología fue del 44,1%, aunque solo el 30% de estos casos estaba documentado en la historia clínica.
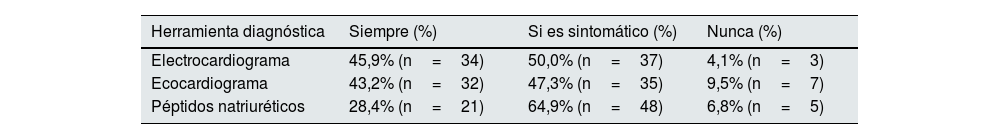
En cuanto a las prácticas diagnósticas, el 55,4% refirió que investiga de forma activa la presencia de IC, mientras que el 44,6% lo hace solo ante síntomas sugerentes. El uso de herramientas diagnósticas fue variable: el ECG se empleaba de forma rutinaria en 43,2% de los casos, y solo en aquellos con síntomas en el 50% de los casos; la ecocardiografía se utilizaba de forma rutinaria en al 43,2% y solo en aquellos con síntomas o péptidos natriuréticos elevados en el 47,3%, los péptidos natriuréticos se solicitaban de forma rutinaria en el 28,8% y solo en aquellos con síntomas o alteración electrocardiográficas o ecocardiográficas en el 64,8% de los casos. Con relación a la valoración clínica sistemática, el 93,2% realizaba anamnesis dirigida en cada visita y el 83,8% exploración física (tablas 1 y 2).
Frecuencia de uso de herramientas diagnósticas
| Herramienta diagnóstica | Siempre (%) | Si es sintomático (%) | Nunca (%) |
|---|---|---|---|
| Electrocardiograma | 45,9% (n=34) | 50,0% (n=37) | 4,1% (n=3) |
| Ecocardiograma | 43,2% (n=32) | 47,3% (n=35) | 9,5% (n=7) |
| Péptidos natriuréticos | 28,4% (n=21) | 64,9% (n=48) | 6,8% (n=5) |
Los porcentajes reflejan la frecuencia de uso reportada por nefrólogos en España. Es posible seleccionar múltiples respuestas por categoría.
No se observaron diferencias significativas en cuanto a la actitud frente al despistaje de la IC en función del centro salvo en la determinación rutinaria de los péptidos natriuréticos siendo esta mucho más frecuente en los nefrólogos que trabajan en centros con unidad cardiorrenal: 39% vs. 15%, p 0,049.
En un análisis exploratorio adicional, se observó que el mayor volumen de pacientes atendidos mensualmente se asoció con una probabilidad significativamente más alta de realizar cribado activo de IC (p=0,001), mientras que la edad, el sexo y la presencia de unidad cardiorrenal en el centro no mostraron asociación significativa. Este hallazgo sugiere que el contacto con un mayor número de pacientes puede favorecer la implementación de estrategias sistemáticas de despistaje de IC.
DiscusiónLa encuesta pone de manifiesto una importante heterogeneidad en el abordaje diagnóstico de la IC, lo que contribuye a un infradiagnóstico relevante en esta población. A pesar de que se estima que cerca de la mitad de los pacientes pueden presentar IC, en muchos casos el diagnóstico no figura en la historia clínica. Esta variabilidad puede atribuirse a diversos factores, incluyendo la falta de protocolos estandarizados y específicos para el cribado y diagnóstico de la IC en pacientes con ERC, diferencias en la formación y experiencia de los nefrólogos, la disponibilidad de recursos diagnósticos, y la inercia terapéutica.
Estos hallazgos coinciden con los del estudio HAKA6, que mostró una baja tasa de diagnóstico de IC en pacientes con ERC y una escasa implementación de tratamientos con impacto pronóstico. Aunque existieran síntomas o hallazgos ecocardiográficos compatibles, la falta de un diagnóstico formal condicionaba las decisiones terapéuticas, especialmente en pacientes con fracción de eyección preservada. La gran variabilidad intercentros en el diagnóstico de IC (2–44%) observada en dicho estudio, refuerza la necesidad de protocolos estandarizados. La discrepancia en la prevalencia de IC (13% en HAKA frente al 44% estimado en nuestra encuesta) puede explicarse, al menos en parte, por la naturaleza y población de cada estudio. HAKA se basó en un registro retrospectivo multicéntrico de pacientes con ERC avanzada con diagnóstico documentado en la historia clínica, mientras que nuestra encuesta recogió la estimación de los nefrólogos encuestados sobre la prevalencia de IC en sus consultas, abarcando distintos ámbitos asistenciales (diálisis, ERCA, hospitalización, trasplante y consulta externa). Así, la prevalencia del 44% refleja la percepción global de los clínicos más que un registro formal de casos, lo que podría justificar la divergencia observada.
El diagnóstico de IC en esta población es relevante porque abre la posibilidad de aplicar terapias basadas en la evidencia, que podrían mejorar su pronóstico. Numerosos estudios han demostrado que tratamientos como los inhibidores del cotransportador sodio-glucosa tipo 2 (iSGLT2) y los antagonistas del receptor mineralocorticoide mejoran el pronóstico incluso en pacientes con ERC10,11. No identificar la IC implica, por tanto, un riesgo en el empeoramiento del pronóstico de estos pacientes12.
Aunque el 55,4% de los encuestados declararon trabajar en centros con unidad cardiorrenal, esto no se tradujo en un cribado sistemático o en una práctica diagnóstica homogénea. Este hecho pone de relieve que la disponibilidad estructural, aunque necesaria, no es suficiente para garantizar la integración real de protocolos multidisciplinares. Es fundamental complementar la infraestructura con programas de formación continua dirigidos a nefrólogos, que mejoren su conocimiento sobre la fisiopatología, el diagnóstico y el tratamiento de la IC en pacientes con ERC. Asimismo, es esencial establecer mecanismos de coordinación asistencial que faciliten la comunicación y la colaboración entre nefrólogos y cardiólogos, no solo con la creación de unidades cardiorrenales, sino también implementando sistemas de cribado y alerta automática que han demostrado utilidad en ámbitos seleccionados. Por ejemplo, el cribado con péptidos natriuréticos ha mostrado ser una herramienta prometedora para la detección temprana de disfunción ventricular y la estratificación del riesgo cardiovascular en la población general, lo que podría ser adaptado para pacientes con ERC13,14. Los resultados de un estudio multicéntrico realizado en el ámbito nacional y publicado recientemente por de la Espriella et al.5, apoya la integración de la evaluación estructurada de la IC y el cribado basado en N-terminal pro-B-type natriuretic peptide (NT-proBNP) en la atención nefrológica de rutina. Este estudio multicéntrico realizado en población con ERC avanzada sin diagnóstico previo de IC y atendida en las consultas de nefrología encontró que una proporción sustancial de esta población ya se encuentran en las etapas B (53,3%) o C (38,6%) de la IC. El estudio propone un algoritmo para el uso de NT-proBNP en el diagnóstico de IC en pacientes ambulatorios con ERC avanzada, donde un NT-proBNP <125 pg/mL indica una baja probabilidad de anomalías cardiacas significativas, un NT-proBNP >500 pg/mL aumenta la probabilidad de anomalías cardiacas y justifica un estudio adicional, y niveles marcadamente elevados de NT-proBNP (> 2.000 pg/mL) representan un subgrupo de alto riesgo que puede justificar una derivación cardiológica rápida.
Por otro lado, la ecocardiografía constituye una herramienta clave para caracterizar fenotipos de IC en pacientes con ERC, permitiendo detectar alteraciones estructurales y funcionales incluso en fases subclínicas. Además, la incorporación de técnicas simplificadas como la ecocardioscopia o el focused cardiac ultrasound (FoCUS), cada vez más accesibles desde las consultas de Nefrología, podría facilitar un cribado más amplio y sistemático, especialmente en entornos con acceso limitado a estudios ecocardiográficos formales. Es importante destacar que los parámetros morfológicos y funcionales empleados para diagnosticar IC pueden requerir ajustes en pacientes con ERC avanzada, debido a la alta prevalencia de enfermedad cardiaca estructural y a que la presentación clínica está condicionada por el estado de volemia y la respuesta a la terapia renal sustitutiva. En este sentido, Chawla et al.15 propusieron una clasificación funcional específica para esta población, basada en criterios ecocardiográficos adaptados. Esta aproximación refuerza la necesidad de dotar a los nefrólogos de competencias en imagen cardiaca básica16.
Más allá del valor de los péptidos natriuréticos y de la ecocardiografía para el cribado de población de riesgo, en esta encuesta también se evidenció una heterogeneidad importante en la elección y frecuencia de uso del resto de herramientas diagnósticas, pese al conocimiento generalizado de su relevancia. Esto refuerza la necesidad de establecer rutas clínicas que integren el cribado de IC en la atención nefrológica rutinaria, independientemente de las preferencias del profesional o de las tradiciones del centro. En este contexto, la incorporación de escalas pronósticas como el índice de Charlson, el Prevent test o el Kidney Failure Risk Equation (KFRE) puede aportar un valor añadido al permitir una mejor estratificación del riesgo cardiovascular y de progresión renal, facilitando una atención más personalizada y proactiva17.
Las guías KDIGO 202418 sobre evaluación y manejo de la ERC recomiendan una evaluación integral del riesgo cardiovascular, incluyendo cribado de IC mediante péptidos natriuréticos y ecocardiografía «cuando esté clínicamente indicado». Sin embargo, esta recomendación es vaga y no especifica criterios concretos para dicho cribado, lo que limita su aplicabilidad en la práctica clínica diaria y favorece la variabilidad en el abordaje diagnóstico. En este sentido, los resultados de la encuesta reflejan la falta de sistematización en el cribado de IC en pacientes con ERC, ya que solo el 55,4% de los encuestados refirió investigar de forma activa la presencia de IC, mientras que el 44,6% lo hace solo ante síntomas sugerentes. Además, el uso de herramientas diagnósticas como la ecocardiografía y los péptidos natriuréticos fue variable y, con frecuencia, condicionado a la presencia de síntomas. Esto sugiere que muchos nefrólogos no están realizando un cribado sistemático de IC en todos los pacientes con ERC, lo que podría llevar a un infra-diagnóstico de la enfermedad. Para mejorar la implementación de las guías KDIGO en la práctica clínica, sería necesario desarrollar recomendaciones más específicas y detalladas sobre el cribado de IC en pacientes con ERC, incluyendo criterios clínicos y bioquímicos claros para identificar a los pacientes que se beneficiarían de una evaluación más exhaustiva.
Los resultados de esta encuesta plantean varias líneas futuras de investigación. En primer lugar, sería deseable desarrollar estudios multicéntricos prospectivos que evalúen el impacto de implantar protocolos sistemáticos de cribado de IC en consultas de Nefrología. Estos estudios podrían comparar diferentes estrategias de cribado (por ejemplo, cribado universal versus cribado selectivo basado en factores de riesgo) y evaluar su efecto sobre el diagnóstico precoz de la IC, el inicio de tratamientos basados en la evidencia y los resultados clínicos a largo plazo (mortalidad, hospitalización, calidad de vida). En segundo lugar, se requieren intervenciones que evalúen si son generalizables los resultados de establecer modelos de colaboración estructurada entre Nefrología y Cardiología19. Estos modelos deberán incluir unidades cardiorrenales multidisciplinares, así como herramientas de apoyo a la decisión clínica específicas para pacientes con ERC e IC (programas de cribado, alertas automáticas, etc.) con el objetivo de homogeneizar la práctica y mejorar la calidad asistencial.
Esta encuesta aporta información novedosa sobre la práctica nefrológica real con respecto al cribado y diagnóstico de la IC en pacientes con ERC, basándose en una muestra representativa a nivel nacional. Entre sus fortalezas destacan el enfoque estructurado y el análisis de variabilidad en la práctica clínica. Sin embargo, al ser una encuesta autodeclarada, implica posibles sesgos de recuerdo o deseabilidad. Además, la distribución desigual de respuestas por comunidades autónomas puede limitar la generalización territorial de los resultados.
Este estudio presenta como fortalezas su carácter nacional, el enfoque estructurado del cuestionario y la inclusión de un número elevado de centros, lo que permite una visión global de la práctica clínica en torno al diagnóstico de la IC en pacientes con ERC. Sin embargo, debe interpretarse teniendo en cuenta ciertas limitaciones: al tratarse de una encuesta autodeclarada, los resultados son estimativos y susceptibles de sesgos de recuerdo o deseabilidad; y la desigual distribución territorial de los encuestados, que condiciona la representatividad de la muestra y limita la generalización de los resultados a nivel nacional. Aunque el carácter multicéntrico aporta valor, la sobrerrepresentación de ciertas comunidades autónomas y la ausencia de otras obliga a interpretar con cautela la extrapolación de los hallazgos. Otra limitación relevante es que no se recogieron parámetros analíticos ni clínicos como FGe o el cociente albúmina/creatinina (UACR), que habrían permitido estratificar la prevalencia de IC en función de los estadios de la ERC. Por tanto, el valor del 44,1% reportado debe interpretarse como una estimación global de la práctica clínica nefrológica en España y no como una prevalencia ajustada por estadio de ERC.
En resumen, este trabajo sugiere que la prevalencia estimada de IC no diagnosticada podría ser muy elevada. Además, existe una importante fata de homogeneidad en el despistaje de IC en la población con ERC atendida en las consultas de Nefrología, lo que tiene importante implicación clínica siendo una de las más relevantes la limitación para el acceso a tratamientos con probado beneficio pronóstico.
Para mejorar el diagnóstico de la IC en pacientes con ERC, es necesario implementar estrategias que aumenten la concienciación sobre la enfermedad entre los nefrólogos, mejoren su capacidad para identificar a los pacientes de alto riesgo y faciliten el acceso a pruebas diagnósticas como la ecocardiografía y los péptidos natriuréticos.
FinanciaciónMMV es IP del proyecto PI23/01518 financiado por el Instituto de Salud Carlos III. Cofinanciado por la Unión Europea. La investigación de AO está financiada por Comunidad de Madrid en Biomedicina P2022/BMD-7223, CIFRA_COR-CM. Instituto de Salud Carlos III (ISCIII), (PI22/00469, PI22/00050, PI21/00251, ERA-PerMed-JTC2022 (SPAREKID AC22/00027). La investigación de MMV, BQ y AO está financiada por el Instituto de Salud Carlos III (ISCIII) RICORS2040: RD24/0004/0028, RD21/0005/0001 y RD24/0004/0001 (Fondo Europeo de Desarrollo Regional [FEDER] y la Unión Europea).
Conflicto de interesesMMV ha recibido apoyo financiero en concepto de actividades formativas viajes y participación en consultorías de Bayer, Novo Nordisk, Boehringer Ingelheim, AstraZeneca, CSL Vifor, Menarini y Novartis. JD declara no tener conflictos de intereses para el presente manuscrito, PS ha recibido apoyo financiero por viajes, consultoría o conferencias de CSL-Vifor, Amgen, GSK, Fresenius, Nipro, AstraZeneca, Bial, Astellas, Braun y Bax, AO ha recibido apoyo financiero por viajes, consultoría o conferencias de Astellas, AstraZeneca, Bioporto, Boehringer Ingelheim, Fresenius Medical Care, GSK, Bayer, Sanofi-Genzyme, Sobi, Menarini, Lilly, Chiesi, Otsuka, Novo-Nordisk, Sysmex. Vifor Fresenius Medical Care Renal Pharma, Spafarma. GR ha recibido apoyo financiero por viajes, consultoría o conferencias de AstraZeneca, Boehringer Ingelheim, CSL-Vifor, Sakura-Sonoscape y Echonous, MS declara no tener conflictos de intereses para el presente manuscrito, AP ha recibido apoyo financiero en concepto de actividades formativas y viajes de AstraZeneca, Bayer, Boehringer Ingelheim, Esteve, Menarini, Mundipharma, Kyowa Kirin, Lilly, Novartis, Novo-Nordisk, Sanofi y Vifor, BQ ha recibido apoyo financiero en concepto de actividades formativas viajes y participación en consultorías de Bayer, Novo Nordisk, Genzyme-Sanofi, AstraZeneca, Boehringer y CSL-Vifor.