El trasplante renal es el tratamiento de elección en la población pediátrica, con enfermedad renal crónica terminal (ERCT)1. En la población pediátrica hay pocos estudios que evalúen la efectividad y la seguridad a largo plazo del alemtuzumab en el trasplante renal.
Este es un estudio descriptivo retrospectivo realizado en el Hospital Pablo Tobón Uribe; se incluyeron todos los pacientes trasplantados renales, menores de 18 años, durante el periodo 2005-2012, que recibieron alemtuzumab como terapia de inducción.
El protocolo de inmunosupresión utilizado incluía la administración de alemtuzumab y terapia triple de mantenimiento, con un anticalcineurínico (tacrolimus o ciclosporina), antimetabolito (azatioprina o micofenolato) y esteroides. Este estudio contó con la aprobación del comité de ética del Hospital Pablo Tobón Uribe.
Durante el período 2005-2012, se realizaron 21 trasplantes renales pediátricos, que recibieron alemtuzumab como terapia de inducción, el 57,1% fueron varones, la edad tuvo una mediana de 13 años (p25-75: 9-15), las malformaciones de las vías urinarias fue la causa más frecuente de enfermedad renal crónica (42,9%), el estado serológico para citomegalovirus fue receptor negativo-donante positivo en el 23,8%, receptor positivo-donante positivo en el 71,4% y receptor positivo donante-negativo en el 4,8%, y el tiempo de isquemia fría tuvo una mediana de 18h (p25-75: 12-20).
La supervivencia de los pacientes a 6, 12, 24, 36 y 60 meses, luego del trasplante renal fue del 100, 100, 95,2, 95,2 y 95,2%, respectivamente. La mortalidad se presentó en un paciente. La supervivencia del injerto renal a 6, 12, 24, 36 y 60 meses posteriores al trasplante fue de 95,2, 95,2, 90,5, 85,7 y 85,7%, respectivamente.
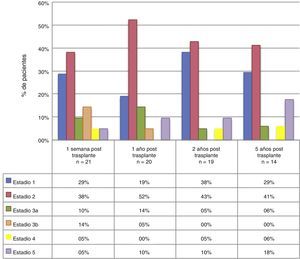
La mediana de TFG a la semana y a 1, 2 y 5 años posterior al trasplante fueron: 72,5ml/min (p25-75: 45-94; n=21), 70,5ml/min (p25-75: 61-88,5; n=20), 89ml/min (p25-75: 66-108; n=19) y 76ml/min (p25-75: 61-101,5; n=14), respectivamente. Al año, 2 y 5 años de seguimiento el 28,6, 19,1 y 29,4% de los pacientes, respectivamente presentaron una TFG menor a 60ml/min/1,73m2. Al agrupar los pacientes de acuerdo al estadio de ERC encontramos que, durante el seguimiento a 5 años, un alto porcentaje de los pacientes se encuentran en estadio 1 y 2 (fig. 1). En la tabla 1 se describen las principales complicaciones encontradas.
Complicaciones posteriores al trasplante renal al año
| Complicaciones | Porcentaje de incidencia a un año n (%) | Tasa de incidencia un año (eventos persona-año) | Tasa de incidencia 5 años (eventos persona-año) |
|---|---|---|---|
| Función retardada del injerto | 2 (9,5) | 10,1% persona-año | — |
| Rechazo agudo del injerto al año | 3 (14,3) | 16% persona-año | 5,6% persona-año |
| Infecciones por CMV | 5 (23,8) | 26% persona-año | 6,7% persona-año |
| Infección por BK virus | 1 (4,8) | 5,2% persona-año | 1,1% persona-año |
| Tuberculosis | 1 (4,8) | 5,2% persona-año | 1,1% persona-año |
| Total | 21 pacientes |
CMV: citomegalovirus.
En este estudio se describen los desenlaces clínicos de los pacientes trasplantados renales pediátricos que recibieron alemtuzumab como terapia de inducción. Dentro de los hallazgos más importantes se pueden resaltar una buena supervivencia del injerto renal, con una baja incidencia de rechazo y pocas complicaciones. La mortalidad se presentó en un paciente que perdió el injerto a los 18 meses del trasplante, ingresó en hemodiálisis y falleció por insuficiencia cardiaca descompensada. Los otros 3 pacientes que perdieron el injerto renal fueron secundarios a rechazo agudo, por mala adherencia en la terapia inmunosupresora.
Otros de los beneficios que encontramos con el uso de esta terapia fue la estabilidad de la TFG en el tiempo. Por otro lado, en nuestro estudio, solamente 28,6, 19,1 y 29,4% de los pacientes tuvieron una TFG inferior a 60ml/min/1,73m2 a 1, 2 y 5 años. De acuerdo con esto, la mayoría de la población estudiada se mantuvo en estadios 1 y 2 de enfermedad renal crónica durante el tiempo de seguimiento, lo que implica menor riesgo futuro de complicaciones asociadas a la enfermedad renal.
La incidencia acumulada de rechazo agudo de nuestros pacientes a 1, 2 y 5 años fue en su respectivo orden del 14,3, 21,1 y 35,7%. A todos estos pacientes se les documentó mala adherencia al tratamiento inmunosupresor, y posteriormente 3 de ellos perdieron el injerto renal. Solo uno de los rechazos fue clasificado como mediado por anticuerpos.
Uno de los mayores temores con el uso de alemtuzumab ha sido su perfil de seguridad. En este estudio se encontró una incidencia de infección por CMV del 23,8% al año posterior del trasplante, la cual es muy alta al compararla con otros estudios y que explicamos porque no usamos profilaxis universal contra este virus2–9. Con respecto a otras complicaciones infecciosas como BK virus y tuberculosis, ambas infecciones solo se presentaron en un paciente durante todo el período de seguimiento (incidencia del 1,1% persona-año).
Durante el tiempo de seguimiento, que tuvo una mediana de 6 años, no se documentó ningún caso de PTLD en la población estudiada, lo que está acorde con lo reportado en la literatura10, sumado a que en esta cohorte el 23,8% de los pacientes fueron seronegativos para el virus de Epstein-Barr. Los estudios con los que comparamos nuestros desenlaces, tampoco encontraron casos de PTLD5,7–9,11. Una de las posibles explicaciones por las cuales alemtuzumab tiene una baja tasa de PTLD es su efecto depletor de linfocitos T y B, lo que evitaría la proliferación de clonas de linfocitos anormales que son los causantes de este tipo de desorden linfoproliferativo.
En conclusión, la terapia de inducción inmunosupresora con alemtuzumab, en receptores pediátricos de trasplante renal, es efectiva en la prevención del rechazo agudo, brinda un adecuado perfil de seguridad a corto y largo plazo, favorece una adecuada tasa de filtración glomerular y una buena supervivencia del paciente y del injerto renal.