La prevalencia de diabetes mellitus aumentó en el último siglo y se estima que el 45% de los pacientes, no estarían diagnosticados. En Sudamérica la prevalencia de diabetes y de enfermedad renal crónica (ERC) incrementó, existiendo gran disparidad entre los países respecto al acceso a diálisis. En Ecuador es una de las principales causas de mortalidad, principalmente en las provincias ubicadas en la costa del océano Pacífico. La mayor causa aislada de ingreso a diálisis es la nefropatía diabética (ND). Aun utilizando las mejores opciones terapéuticas para la ND, el riesgo residual de proteinuria y de ERC terminal permanece elevado. En esta revisión describimos la importancia del problema en el mundo y en nuestra región. Analizamos estudios moleculares y celulares relevantes que indican la crucial importancia de eventos glomerulares en el desarrollo y en la evolución de la ND y en la insulinorresistencia. Incluimos conceptos anatómicos, fisiopatológicos y clínicos básicos, desarrollando especial énfasis en el rol de factores angiogénicos como el factor de crecimiento vascular endotelial (VEGF-A) y su relación con el receptor de insulina, la sintasa endotelial de óxido nítrico-óxido nítrico (eNOS) y las angiopoietinas. En el transcurso del texto proponemos diversas vías, que a nuestro entender tienen potencial terapéutico. Profundizar en el estudio del VEGF-A y las angiopoietinas, el estado de VEGF resistencia glomerular, la relación del receptor 2 de VEGF/ nefrina, VEGF/receptores de insulina/nefrina, la relación VEGF/eNOS-ON a nivel glomerular podría aportar soluciones al acuciante problema de la ND en el mundo y generar nuevas alternativas de tratamiento.
The prevalence of diabetes mellitus increased during the last century and it is estimated that 45% of the patients are not diagnosed. In South America the prevalence of diabetes and chronic kidney disease (CKD) increased, with a great disparity among the countries with respect to access to dialysis. In Ecuador it is one of the main causes of mortality, principally in the provinces located on the coast of the Pacific Ocean. The greatest single cause of beginning dialysis is diabetic nephropathy (DN). Even using the best therapeutic options for DN, the residual risk of proteinuria and of terminal CKD remains high. In this review we indicate the importance of the problem globally and in our region. We analyse relevant cellular and molecular studies that illustrate the crucial significance of glomerular events in DN development and evolution and in insulin resistance. We include basic anatomical, pathophysiological and clinical concepts, with special attention to the role of angiogenic factors such as the vascular endothelial growth factor (VEGF-A) and their relationship to the insulin receptor, endothelial isoform of nitric oxide synthase (eNOS) and angiopoietins. We also propose various pathways that have therapeutic potential in our opinion. Greater in-depth study of VEGF-A and angiopoietins, the state of glomerular VEGF resistance, the relationship of VEGF receptor 2/nephrin, VEGF/insulin receptors/nephrin and the relationship of VEGF/eNOS-NO at glomerular level could provide solutions to the pressing world problem of DN and generate new treatment alternatives.
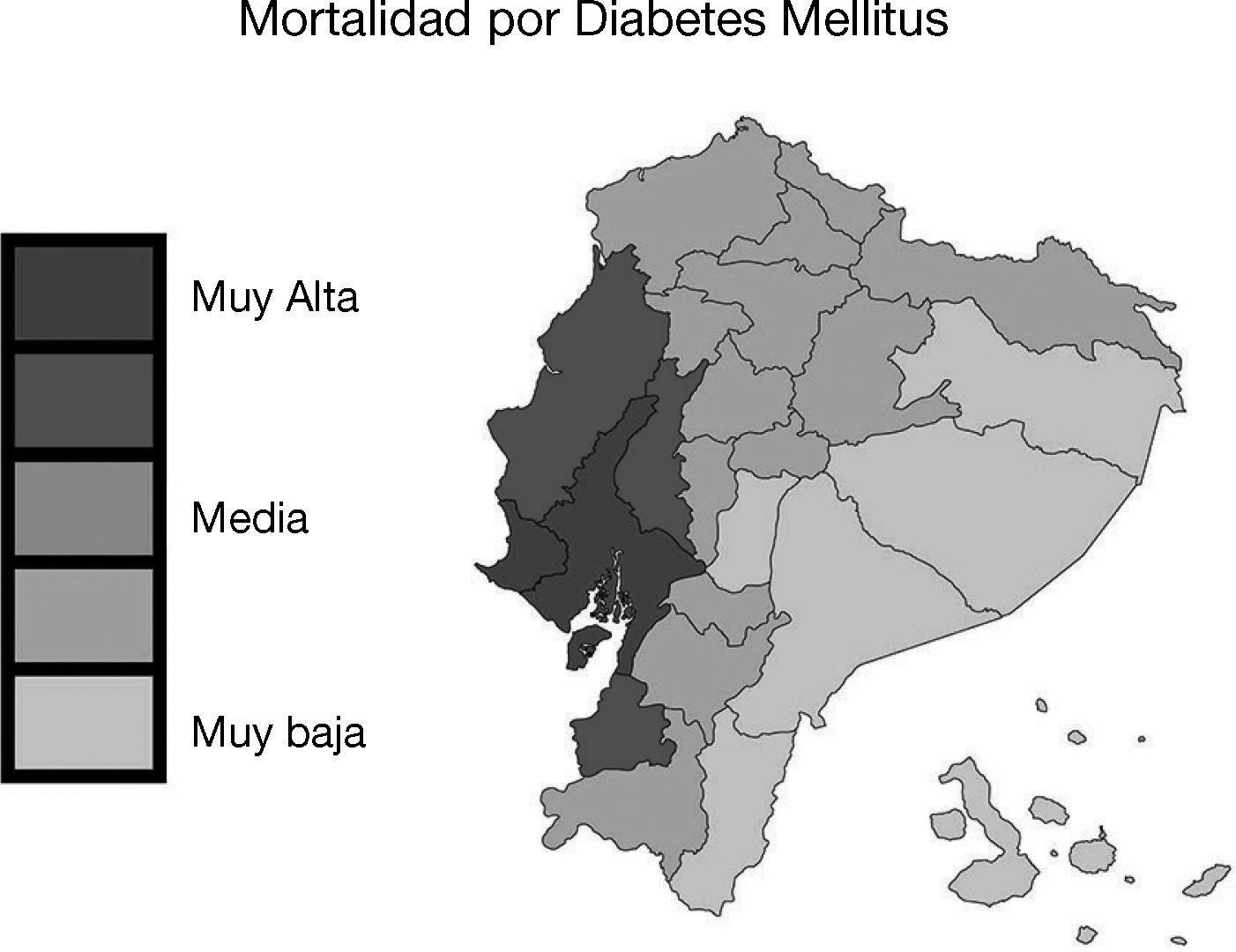
La prevalencia mundial de diabetes mellitus ha aumentado desde el siglo pasado1. En adultos de 20 a 79 años de edad es del 8%1. La diabetes se esparce en países ricos y pobres pero es prevalente en grupos vulnerables y en regiones del mundo con menores ingresos. Los territorios con mayor número de afectados son: China, India, Estados Unidos, Brasil y Rusia1. Esta situación está asociada a una mayor urbanización, bajo nivel socioeconómico, inequidad, incremento de la expectativa de vida y de la densidad poblacional, factores étnicos, alimentación, inactividad física y sobrepeso1,2. En España fue reportada una prevalencia de diabetes del 13,8% y el 6,0% desconocía el diagnóstico3. Estimaciones recientes sugieren que la prevalencia mundial se duplicará en el año 2035, mientras que en nuestra región, Sudamérica y América central, aumentará al 9,8%1,2. Adicionalmente el 45,5% de las personas con diabetes no estarían diagnosticadas1,2. En la población urbana ubicada en las costas de nuestra región, la prevalencia de diabetes es mayor que en las montañas o en la selva, y lo mismo ocurre en personas que se desplazan del medio rural al urbano1,2. Asimismo, la población de nativos sería particularmente vulnerable, debido a cambios del estilo de vida, marginación y menor exposición a los sistemas de salud2. En Ecuador, la diabetes tiene una prevalencia del 6%, y en el año 2010 fue la segunda causa de mortalidad2,4,5. En las provincias de Guayas, Los Ríos y Manabí, ubicadas en la costa del océano Pacífico, el índice de mortalidad por diabetes y el consumo de alimentos industrializados es mayor, mientras que en la Amazonía predomina la alimentación con productos naturales y dicho índice es menor6 (fig. 1).
Mapa de la tasa de mortalidad por diabetes mellitus en Ecuador. En Ecuador la mortalidad causada por diabetes mellitus fue mayor en las provincias de Guayas, Los Ríos y Manabí, ubicadas en la costa del océano Pacífico. Mapa de la tasa de mortalidad por diabetes mellitus (muertes/100.000 individuos por año, INEC 2011). Esta figura es parte de una figura publicada originalmente por Neira-Mosquera y col.6 con leves modificaciones (con permiso para reproducción).
La enfermedad renal producida por la diabetes es llamada nefropatía diabética (ND). Alrededor del 30% de los pacientes con diabetes desarrollan ND7,8. Dicha enfermedad es la principal causa de enfermedad renal crónica (ERC) y de ingreso a diálisis7–11. El aumento de diabetes registrado en las últimas décadas fue acompañado de un incremento en la prevalencia de ERC7–11. La ERC afecta del 10% al 16% de adultos, constituyendo un serio problema mundial7–11. En Sudamérica, la prevalencia de diabetes y de ERC en estadios terminales (ERCT) incrementó en las últimas décadas, existiendo gran disparidad entre los países respecto al acceso a diálisis9–11. En Ecuador, la prevalencia de pacientes que recibieron tratamiento sustitutivo de la función renal fue de 406 personas por millón de habitantes, en el 201011. Por otra parte, los inhibidores del sistema renina-angiotensina-aldosterona (SRA) constituyen la mejor opción terapéutica para la ND, pero el riesgo residual de ERCT permanece elevado y la asociación de estas drogas fue relacionada a hiperpotasemia e insuficiencia renal aguda12,13 (IRA). La búsqueda de nuevas alternativas terapéuticas es necesaria.
Los estudios poblacionales permiten tomar conciencia de la problemática, mientras que el conocimiento generado en laboratorios de investigación, ayuda a comprender la intimidad de los eventos biológicos que suceden en las personas. En esta revisión incluiremos conceptos anatómicos y fisiopatológicos, que revelan la crucial importancia de sucesos que ocurren a nivel glomerular. Además analizaremos el rol del factor de crecimiento vascular endotelial (VEGF-A) y de sus relaciones con el óxido nítrico (ON), el receptor de insulina y las angiopoietinas. Finalmente contemplaremos aspectos básicos y el análisis de estudios moleculares y celulares recientemente publicados.
Aspectos anatómicos y fisiopatológicos de la NDEn la diabetes hay alteraciones renales funcionales y estructurales que inducen proteinuria en magnitudes variables, desde microgramos a varios gramos por día7,8,13. El riesgo de desarrollar ERCT está relacionado a la excreción urinaria de albumina, indicar tempranamente los inhibidores del SRA es importante por sus efectos beneficiosos renales y sistémicos7,8,13. La ND se acompaña de excreción urinaria de albumina persistente o microalbuminuria, definida como la pérdida de albumina urinaria entre 20 y 199μg/min o 30 a 299 mg/d, en dos ocasiones diferentes, y cuando el cociente albumina/creatinina es de 30-299 mg/g, en una muestra aislada de orina7,8. En la diabetes tipo 1, se recomienda cuantificar anualmente la excreción urinaria de albumina, desde los 5 años del diagnóstico; en la diabetes tipo 2 dada la dificultad de precisar su inicio, es preferible medirla desde el momento del diagnóstico7,8. La prevalencia de microalbuminuria, en pacientes con diabetes tipo 2, fue del 24,9% a los 10 años de seguimiento14, pero el 30% de personas con diabetes tipo 2 sin microalbuminuria desarrollaron ND. También es importante cuantificar el filtrado glomerular (FG), porque algunos pacientes solo deterioran la función renal sin presentar proteinuria7,8. Considerando que el 85% de personas con diabetes son de tipo 2, son necesarios mejores biomarcadores7,8,13,14.
Los factores de riesgo para desarrollar ND son hiperglucemia, hipertensión arterial (HTA), dislipidemia, edad superior a 65 años, género masculino, tabaquismo, antecedentes familiares y origen hispano o afroamericano7,8. Fue reportada la agregación familiar en poblaciones con diferentes ancestros, especialmente en indios Pima y en afroamericanos15. Mooyaart y col. encontraron 24 variantes genéticas asociadas a la ND16. También, fueron implicados los mecanismos epigenéticos8,17. Por ejemplo, la hiperglucemia crónica, sin alterar la secuencia de nucleótidos, podría modificar el DNA o metilar histonas asociadas al DNA17. Sin embargo la relevancia de estos hallazgos en el desarrollo de la ND no ha sido determinada.
En la fisiopatología de la ND fueron implicados muchos factores como: la glucosa, los receptores de glucosa, el VEGF-A, el ON, las especies reactivas al oxígeno (ROS), el factor transformante de crecimiento beta (TGF-Beta), el SRA, calicreínacinina, el sistema blanco de rapamicina en mamíferos, la inflamación, el factor de necrosis tumoral alfa, la adiponectina, los productos de la glicosilación avanzada y sus receptores, el estrés oxidativo mitocondrial y los micro-RNA7,8,18–22.
Desde el punto de vista anatomopatológico, la diabetes tipo 1 y 2 inducen lesiones renales comunes. Estas lesiones fueron caracterizadas en la diabetes tipo8,17,18,23–26. En la tipo 2, el curso y la histología renal tienen particularidades, asociadas a comorbilidades como HTA, enfermedades vasculares, envejecimiento y obesidad7,8,23,24. Después de 5 años del diagnóstico de diabetes, hay hiperfiltración, microalbuminuria, glomerulomegalia, engrosamiento de la membrana basal g lomer ular (MBG) y alteración de los podocitos26. Posteriormente, la matriz extracelular (MEC) se deposita en el mesangio. Aproximadamente 10 años más tarde, la proteinuria y la HTA son evidentes, y progresivamente el FG se deteriora7,23,24,26. En un período de 20 a 25 años, la esclerosis es avanzada, hay fibrosis túbulo intersticial y la ERC progresa a fases terminales7,24–26.
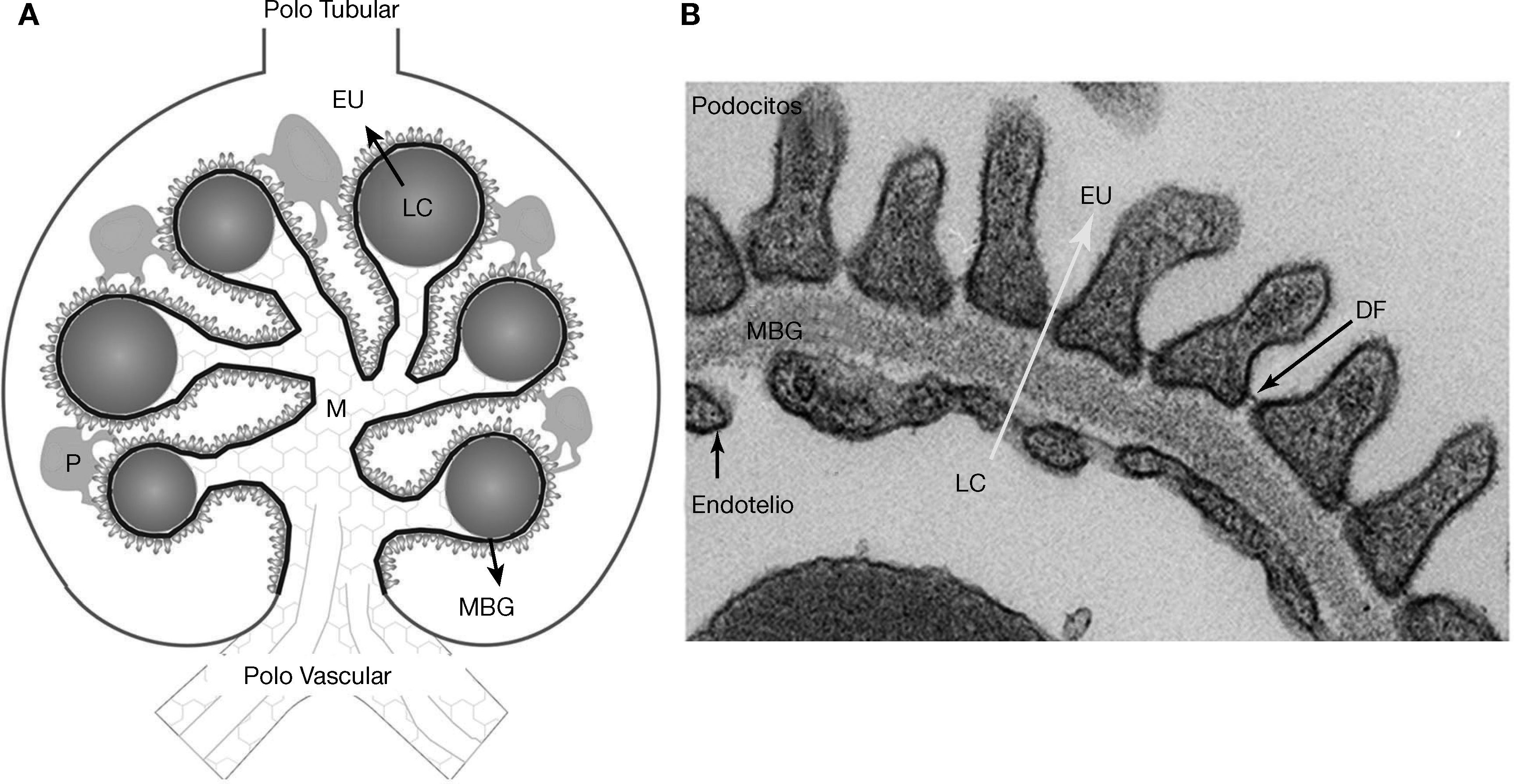
Por su parte, los glomérulos, los túbulos, el intersticio y los vasos renales son modificados por el medio diabético. Los cambios glomerulares comprenden la barrera de filtración glomerular (BFG), la MEC y las principales células que lo componen (podocitos, células endoteliales y mesangiales)7,15,19–25. Además impide el paso anormal de proteínas plasmáticas según el tamaño y la carga, y su alteración fue asociada a proteinuria7,18–20,25. La BFG está formada por los podocitos, la MBG y el endotelio (fig. 2). Los podocitos son células epiteliales muy diferenciadas, con gran cuerpo celular, y prolongaciones primarias y secundarias conectadas por los diafragmas de filtración18–20 (DF). El DF es permeable al agua y a pequeños solutos, pero es selectivo al paso de grandes moléculas, constituyendo un factor clave en la permeabilidad de la BFG25. Asimismo, está formado por un complejo de proteínas, donde la nefrina cumple un rol importante7,18–20. Por el lado apical, los podocitos flotan en el espacio urinario, mientras que por el lado basolateral, contactan la MBG. Las proteínas del citoesqueleto de los podocitos se relacionan con proteínas de la MBG a través de integrinas y dextroglicanos18,20,25. La MBG está constituida principalmente por proteínas como colágeno tipo IV y lamininas18,25. El endotelio fenestrado, cubierto por el glicocalix, es la capa más interna de la BFG7,18,21,25. La diabetes altera las tres capas de la BFG. Entre los cambios tempranos, se describieron neoangiogénesis en el polo vascular glomerular y pérdida de las fenestraciones endoteliales7,15,22,23. La MBG incrementa de espesor debido a alteraciones del recambio de proteínas7,18–20,25. En los podocitos tempranamente se observa achatamiento, hipertrofia, despegamiento y apoptosis, mientras que tardíamente, se observa podocitopenia7,18–20.
La barrera de filtración glomerular. A: representación esquemática del glomérulo, la barrera filtración glomerular (BFG) formada por los podocitos (P), la membrana basal glomerular (MBG) y el endotelio. El ultrafiltrado del plasma atraviesa la BFG (flecha negra) para llegar al espacio urinario (EU). Los podocitos (verde) contactan varios capilares glomerulares (representados como círculos rojos) y el mesangio intraglomerular (M). La MBG (línea negra) envuelve los capilares y rodea al mesangio. El endotelio glomerular está simbolizado por una línea celeste entrecortada, ubicada entre la luz capilar (LC) y la MBG, el polo vascular en la parte inferior del glomérulo, el polo tubular en la parte superior. B: Ultraestructura de la BFG observada con un microscopio electrónico. Los podocitos, la MBG, el diafragma de filtración (DF) y el endotelio fenestrado. El ultrafiltrado del plasma atraviesa la BFG, flecha amarilla, desde la luz capilar (LC) al espacio urinario (EU).
A continuación, analizaremos trabajos recientemente publicados que relacionan el VEGF-A a proteínas glomerulares involucradas en la fisiopatogenia de la ND humana y experimental. En el transcurso del texto señalaremos algunas vías que podrían ser utilizadas en la generación de nuevas herramientas terapéuticas (tabla 1).
Vías glomerulares con potencial terapéutico para la ND
| Vías estimuladas | Vías inhibidas |
|---|---|
| TGF-Beta | eNOS |
| CTGF | Actividad de VEGFR2 |
| VEGF-A | Nefrina |
| Angiopoietina 2 | Angiopoietina 1 |
TGF-Beta: transforming growth factor; CTGF: connective tissue growth factor; VEGF-A: vascular endothelial growth factor; eNOS: endotelial nitric oxide sinthase.
El VEGF-A es un potente factor angiogénico relacionado a la angiogénesis normal y patológica. Promueve la proliferación, diferenciación y migración de células endoteliales; induce vasodilatación y aumenta la permeabilidad vascular18–20,27. Cumple un rol importante durante el desarrollo renal, en el riñón adulto es secretado por los podocitos y es indispensable para el mantenimiento de la BFG15. Actúa a través de receptores tirosina-kinasa, conocidos como receptor 1 y 2 de VEGF18,27 (VEGFR1 y 2). El VEGFR2 es expresado en las células endoteliales y en los podocitos, fue relacionado a las señales más importantes del VEGF-A18,27. Dos correceptores llamados neurofilinas 1 y 2 amplifican la señal del VEGFR218,27.
Existen evidencias que demuestran que la glucosa estimula directa e indirectamente la expresión de VEGF-A en podocitos, a través de la angiotensina II y del TGF-Beta18–20. La glucosa juega un rol muy importante en la fisiopatogenia de la ND. El control de la hiperglucemia disminuye la progresión de la ND e induce reversión de la proteinuria y de lesiones histológicas avanzadas28–32. Cuando hubo mejor control de la glucemia mejoró la proteinuria, el FG y la HTA en pacientes con diabetes tipo 1, seguidos durante 30 años28. Cuando hubo mayor control de la hiperglucemia, la MBG evidenció menor engrosamiento29. Los cambios histológicos de ND avanzada, revirtieron después de 10 años de un trasplante de páncreas30. Haraguchi y col. lograron revertir la proteinuria en rango nefrótico y las lesiones histológicas compatibles con ND avanzada, después de 5 años de intensivo tratamiento de la hiperglucemia31. El tratamiento con cirugías bariátricas practicado a pacientes con diabetes tipo 2 y obesidad, mejoró el FG y la proteinuria, relacionado a la disminución del peso y la hiperglucemia32.
La hiperglucemia incrementa la expresión de renina y de angiotensinógeno en las células mesangiales20. Las células mesangiales y los podocitos sintetizan angiotensina II y expresan receptores de angiotensina19,20. El aumento de angiotensina II estimula la expresión de TGF-Beta, VEGF-A, factor de crecimiento del tejido conectivo (CTGF), interleukina 6 y proteína quimiotáctica para monocitos-1 induciendo expansión de la MEC y apoptosis de los podocitos7,18–20.
Adicionalmente la glucosa incrementa la expresión de TGF-Beta en células mesangiales y en podocitos19. El TGF-Beta activo induce engrosamiento de la MBG y glomeruloesclerosis a través de VEGF y CTGF; el aumento de VEGF-A inhibe la expresión de TGF-Beta, en un mecanismo de retroalimentación negativo18–20. De manera opuesta en la diabetes el aumento de VEGF-A se asocia a TGF-Beta y CTGF incrementado; proliferación y acumulación de proteínas en la MEC glomerular18–20. El TGF-Beta fue relacionado a la proliferación de células mesangiales, a la glomeruloesclerosis nodular y difusa como así también a la fibrosis18–20. Ratones transgénicos con ausencia del receptor tipo 2 de TGF-Beta y la administración de anticuerpos anti TGF-Beta previnieron la acumulación mesangial y el deterioro de la función renal19,20. Estos anticuerpos constituyen una esperanza terapéutica para la ND, pero aún no están disponibles para el uso humano19.
Modificaciones del VEGF-A glomerular en la NDEl VEGF-A sistémico y renal están incrementados desde estadios tempranos de la ND, en humanos y en roedores, y fue asociado a neoangiogénesis18,21,22. El SRA, el VEGF-A y la nefrinuria fueron implicados en este proceso18–20,22,33–38. Los podocitos y las células endoteliales en cultivo incrementaron la expresión de VEGF-A y de VEGFR2 en respuesta al aumento de glucosa39–41.
Nosotros demostramos que el VEGF glomerular es determinante para el desarrollo y la evolución de la ND33,34. Ratones normoglucémicos con sobreexpresión de VEGF en los podocitos desarrollaron glomerulomegalia, hiperfiltración, engrosamiento de la MBG y lesión de los podocitos, cambios similares a la ND temprana33. En estos ratones transgénicos, la diabetes provocó proteinuria masiva, glomeruloesclerosis nodular avanzada y menor expresión de nefrina34. Los ratones diabéticos sin sobreexpresión de VEGF, solo exhibieron leve glomeruloesclerosis difusa34. Estos experimentos demuestran que el aumento de VEGF glomerular, independientemente del medio diabético, genera cambios idénticos a la ND temprana y que incrementar el VEGF glomerular acelera la evolución de la ND a estadios más avanzados. En ausencia de diabetes, el VEGF-A urinario fue un buen marcador de la expresión glomerular de VEGF y se correlacionó con la proteinuria33. Contrariamente en la diabetes el VEGF-A no fue un buen marcador de la expresión glomerular ni de la gravedad de la ND. Los niveles urinarios y sistémicos de VEGF-A estuvieron elevados en ratones diabéticos con y sin sobreexpresión de VEGF glomerular34. Probablemente en el contexto de diabetes la excreción urinaria de VEGF-A refleja los niveles sistémicos, ocultando los cambios glomerulares del VEGF34. Resumiendo estos experimentos sugieren que el VEGF-A glomerular es determinante en la evolución de la ND, la sobreexpresión de VEGF en los podocitos es peligrosa y la glucosa en forma directa e indirecta estimula la cascada de señales de VEGF-A en los podocitos. En la diabetes el VEGF-A urinario y sistémico no se correlacionaron con la expresión glomerular de VEGF, ni con la severidad de las lesiones glomerulares, cuestionando al VEGF-A como biomarcador de ND.
Fue demostrado que la disminución glomerular de VEGF-A genera lesiones de la BFG, proteinuria e insuficiencia renal en animales y en humanos42,43. Ratones transgénicos con silenciamiento de VEGF-A en los podocitos presentaron IRA, alteración de las tres capas de la BFG y disminución de la expresión de integrinas43. Algunos pacientes tratados con anticuerpos anti VEGF-A presentaron proteinuria, lesiones endoteliales y microangiopatía trombótica42. Estas evidencias sugieren que el VEGF-A liberado por los podocitos es importante para el mantenimiento de la función y de la estructura glomerular en el riñón adulto. Si el control de la expresión glomerular de VEGF-A mejora la ND no fue definido, hay evidencias que muestran resultados contradictorios. La administración de anticuerpos anti-VEGF mejoró la ND en roedores44. En experimentos con ratones, la endostatina y la tumstatina previnieron el desarrollo de ND debido a disminución de VEGF-A y de angiopoietina 236. En contraste ratones diabéticos con deleción genética del VEGF-A en podocitos presentaron proteinuria y severa glomeruloesclerosis difusa, asociada a injuria endotelial y apoptosis42.
Las evidencias antes descriptas sugieren que en la diabetes es necesario mantener niveles de VEGF-A glomerular muy controlados, para no sumar nuevas lesiones, ni empeorar la ND. Controlar la expresión de VEGF-A glomerular, en márgenes muy estrechos, podría tener potencial terapéutico pero cuáles son las concentraciones óptimas y cuál es el momento apropiado para realizar esta manipulación no fue definido.
Relaciones del VEGF-A con los receptores de insulina, nefrina y ROS en la NDEn la ND coexisten glomérulos con diferentes grados de lesión, la expresión de VEGF-A y de su cascada de señales fue relacionada a los cambios glomerulares37. En biopsias de pacientes con ND se evidenció mayor expresión de VEGF en los glomérulos lesionados por la diabetes que en glomérulos indemnes37. No obstante la expresión del receptor unido a VEGF estuvo incrementada en glomérulos con lesiones leves, y disminuida en glomérulos con moderado o severo compromiso37. Un comportamiento similar fue observado con la fosforilación de serina/treonina protein kinasa, proteína ubicada en la cascada de señales de VEGF, sugiriendo que otros factores modularían la actividad del VEGF/VEGFR37.
Los podocitos expresan receptores de insulina cuya actividad depende de la expresión de nefrina45,46. El receptor de insulina está ubicado en el DF, lugar donde los podocitos expresan nefrina y VEGFR233,46. Nosotros caracterizamos la interacción existente entre la nefrina y el VEGFR215. La sobreexpresión de VEGF en los podocitos disminuyó la expresión y la fosforilación de la nefrina15,33. Hale y col. reportaron que la insulina aumenta la producción de VEGF-A en podocitos humanos y de ratones45. En ratones transgénicos, este aumento del VEGF-A fue perturbado por la insulinorresistencia, anticipando el desarrollo de lesiones en podocitos secundar ias a la insulinorresistencia45. En pacientes con insulinorresistencia, causada por diabetes y por otras enfermedades, fueron descriptas alteraciones renales como hiperfiltración, proteinuria, modificaciones de la BFG y del mesangio47,48. En conjunto estos hallazgos sugieren que el VEGF, la nefrina y el receptor de insulina podrían estar relacionados en la ND y en la insulinorresistencia, constituyendo vías glomerulares susceptibles de ser modificadas.
Por otra parte el estrés oxidativo, secundario a la hiperglucemia, puede modificar el glicocalix, incrementar ROS y los productos de glicosilación avanzada, alterando el endotelio. Adicionalmente la activación glomerular de protein kinasa C (PKC) fue asociada a expansión mesangial, engrosamiento de la MBG, disfunción endotelial, activación de citoquinas y de TGF-Beta7,18,21,40,41. Mima y col. describieron que la hiperglucemia altera la fosforilación de nefrina en ratas diabéticas y en podocitos en cultivo expuestos a altas concentraciones de glucosa49. La interrupción de la fosforilación de nefrina fue atribuida a un estado de “VEGF resistencia glomerular” relacionado a la activación de PKC49. La cascada de señales del VEGF en podocitos y en células endoteliales fue inhibida selectivamente por la hiperglucemia49. El aumento de la glucosa y la diabetes causarían mayor apoptosis de los podocitos y disfunción endotelial debido, en parte, a mayor activación de la protein kinasa activada por mitógeno (PKCδ/p38) y a la sobreexpresión de Src homology-2 domain-containing phosphatase-1 (SHP-1)49. Adicionalmente SHP-1 regula negativamente al VEGFR2 y al receptor de insulina49.
Warren y col. demostraron que en la diabetes la hiperglucemia disminuye la actividad del VEGFR2 endotelial41. La generación de ROS causada por la hiperglucemia, indujo activación del VEGFR2 y su posterior degradación, independientemente del VEGF-A41. Esto alteraría la normal respuesta de las células endoteliales al VEGF-A circulante, debido a menor disponibilidad del receptor. Bloqueando la producción de ROS con antioxidantes se revirtió la disponibilidad del VEGFR2 y la falta de respuesta endotelial al VEGF-A causada por la hiperglucemia41. Estos resultados sugieren que el aumento de VEGF-A presente desde estadios tempranos de la ND, podría ser secundario a una “VEGF-resistencia” del VEGFR2, causado por una mayor degradación del receptor en las células endoteliales.
En conjunto estos trabajos indican que en la ND la sobreexpresión de VEGF en podocitos podría estar estimulada de forma autocrina y paracrina por un estado de “VEGF-resistencia”. Las conexiones del VEGF-A con el estrés oxidativo a nivel glomerular, podrían constituir vías con potencial terapéutico.
Relación entre las angiopoietinas y el VEGF-A en la NDLas angiopoietinas, factores de crecimiento involucrados en la angiogénesis, fueron vinculadas a la ND18,36. Los niveles plasmáticos de angiopoietina 2 están elevados en humanos y en ratones diabéticos, alterando el cociente angiopoietina-1/ angiopoietina-2. Los ratones diabéticos con menores niveles de angiopoietina 1 presentaron angiogénesis aberrante, hiperfiltración, glomerulomegalia y albuminuria acompañados de sobreexpresión de VEGF-A y de VEGFR2 fosforilado. Las alteraciones causadas por la disminución de angiopoietina 1, fueron parcialmente impedidas al restaurar su expresión en los podocitos de ratones transgénicos36. Estos experimentos demuestran la importancia de las angiopoietinas y su relación con el VEGF-A en la fisiopatogenia de la ND. La modificación de la expresión de proteínas a nivel glomerular, manipulando las células que las producen, constituye una alternativa terapéutica36.
Relación entre el VEGF-A y el óxido nítrico en la NDEl VEGF-A estimula la producción de ON mediante la activación de la sintasa endotelial de ON18,35,50 (eNOS). Los efectos del VEGF-A en la vasodilatación y en el aumento de la permeabilidad vascular son mediados por el aumento de ON dependiente de eNOS18,27,35,50. En condiciones normales el VEGF-A induce activación de eNOS y aumento de ON, este aumento regula negativamente al VEGF-A y al CTGF, inhibiendo la acumulación de MEC18. En la diabetes esta relación cambia, el aumento de VEGF-A coexiste con menor actividad de eNOS, hay desacoplamiento de VEGF-A y ON50. En correspondencia con esta teoría ratones diabéticos con ausencia de eNOS desarrollaron aumento de la expresión de VEGF-A y severa ND50. Nosotros demostramos que la sobreexpresión de VEGF en podocitos, asociada a ausencia de eNOS, indujo cambios indistinguibles a la ND avanzada35. En ausencia de diabetes, estos ratones transgénicos, desarrollaron proteinuria, insuficiencia renal y glomeruloesclerosis nodular35. Estas evidencias sugieren que las alteraciones de la relación VEGF-A/eNOS-ON glomerulares son críticas y muy peligrosas, destacando a estos eventos y a su relación con el VEGF-A como blancos de tratamiento a nivel glomerular.
La deficiencia de ON endotelial secundaria a la actividad de eNOS disminuida, podría también relacionar los mecanismos de insulinorresistencia a la disfunción endotelial47,48. Las células endoteliales expresan receptores de insulina. Estos receptores, mediante la activación de eNOS, controlan el tono vascular induciendo vasodilatación. Por ejemplo en pacientes con diabetes hay alteraciones de la activación de eNOS, relacionando el ON a la insulinorresistencia endotelial47–49. Estos hallazgos sugieren que el VEGF-A y la relación eNOS/ON glomerular podrían estar implicados en los estados de insulinorresistencia asociados a prediabetes, diabetes y ERC.
ConclusionesLos estudios poblacionales revelan una creciente prevalencia mundial de diabetes tipo 2, lo que hace prever que la ND será un problema aún mayor. Buscar alternativas para el diagnóstico, prevención y tratamiento de la ND es perentorio. Profundizar en el estudio de vías moleculares con potencial terapéutico como los factores angiogénicos, el estado de VEGF resistencia glomerular, la insulinorresistencia en podocitos, la relación del VEGFR2/nefrina, VEGF/receptores de insulina/ nefrina, la relación VEGF/eNOS-ON, podría aportar soluciones al acuciante problema de la ND en el mundo.
Conceptos claves- 1.
La prevalencia de diabetes mellitus y de ERC incrementó en las últimas décadas. La causa aislada más frecuente de ERC es la ND. Los factores relacionados al desarrollo de ND son: edad superior a 65 años, hiperglucemia no controlada, hipertensión arterial, dislipidemia, género masculino, hábito de fumar, antecedentes familiares y origen hispano o afroamericano.
- 2.
La glucosa en forma directa e indirecta incrementa la expresión celular de VEGF-A. En la ND hay aumento sistémico y glomerular de VEGF-A, pero el VEGF-A glomerular y la relación VEGF-A/eNOS-ON glomerular son claves en la fisiopatogenia de la ND.
- 3.
Las células endoteliales y los podocitos expresan receptores de insulina. La nefrina es indispensable para la acción del receptor de insulina en podocitos, su activación está relacionada al VEGF-A. El VEGFR2 y la nefrina interactúan en podocitos. El receptor de insulina, la nefrina y el receptor de VEGF-A podrían estar mecanísticamente conectados en la ND y en la insulinorresistencia.
- 4.
En la ND la sobreexpresión de VEGF en podocitos podría estar estimulada de forma autocrina y paracrina por un estado de “VEGF-resistencia” donde PKC y ROS estarían implicados. Las conexiones del VEGF-A con el estrés oxidativo a nivel glomerular, podrían constituir vías con potencial terapéutico para la ND.
- 5.
Los factores angiogénicos como el VEGF-A y las angiopoietinas, el estado de VEGF resistencia, la insulinorresistencia en podocitos, la relación del VEGFR2/nefrina, VEGF-A/ receptores de insulina/nefrina, la relación VEGF/eNOS-ON se constituyen en vías glomerulares de crucial importancia y podrían ser posibles blancos de tratamiento para la ND.
Secretaría de Ciencia Tecnología e Innovación de Ecuador (Senescyt), Proyecto Prometeo. Universidad Estatal de Milagro (UNEMI-OCAS-SO-27092013-N.° 26 DV). Universidad de Guayaquil.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Maiten Fernández Verón, Facultad de Arquitectura, Diseño y Urbanismo, Universidad de Buenos Aires, Argentina por colaborar en el diseño de las figuras. Eco. Patricio Álvarez, UNEMI, por ayudar en los procesos de publicación y Gonzalo Fernández Verón, por la revisión del idioma.