Después de muchos años de ausencia de novedades en este campo, recientemente se han incorporado nuevas herramientas diagnósticas de la infección tuberculosa, tanto en la fase latente como en la de infección activa. Si eran necesarios nuevos métodos en el estudio de población general que mejoraran el armamentario existente, en el caso del enfermo renal, sobre todo en fases avanzadas y en terapia sustitutiva, la necesidad de mejora era evidente. Con motivo de la publicación en este número de la Revista de un estudio analizando los resultados de la comparación de la prueba de la tuberculina (PT) y los nuevos métodos de diagnóstico in vitro, en la detección de la infección tuberculosa latente (ITL), resumimos en este Comentario editorial la posible repercusión de estos métodos en el tratamiento del paciente con enfermedad renal.
LA ENFERMEDAD TUBERCULOSA HOY
Según datos de la Organización Mundial de la Salud (OMS)1, un tercio de la población mundial presenta actualmente ITL. En 2006, hubo en el mundo más de 9.200.000 casos nuevos de tuberculosis (TBC), con una prevalencia de más de 14 millones de personas y casi 1,7 millones de muertes, lo que supone una letalidad del 18%. La OMS considera que la tasa de incidencia mundial de TBC ha alcanzado su pico en 2002 con variaciones en relación con los cambios poblacionales. Según los últimos datos publicados por la Red de Vigilancia Epidemiológica de España2, en 2009 se registraron 6.070 casos de TBC. Sin embargo, estas cifras deben considerarse con reservas, ya que a pesar de que la TBC es una enfermedad de declaración obligatoria, se estima que al menos una tercera parte de los casos no se notifican.
Según el Registro de la Sociedad Española de Nefrología (S.E.N.) en el año 2009 la incidencia de pacientes con tratamiento renal sustitutivo (TRS) fue de 129 pacientes por millón de población (pmp), la mayoría en hemodiálisis (HD), un 85%, un 12% en diálisis peritoneal (DP) y el 2,8% con trasplante renal (TR) prediálisis. La prevalencia fue de 1.039,4 pacientes pmp, estando un 47,67% en HD, un 4,8% en DP y un 47,51% con injerto funcionante. Aunque la incidencia de pacientes en TRS se ha mantenido estable en la última década en España, hay diferencias entre las distintas regiones de nuestro país. En Europa la incidencia varía entre 94,6-263 pacientes pmp, y la prevalencia entre 64,9-1.115,1 pacientes pmp, por lo que nos encontramos en la zona media respecto a los países de nuestro entorno3. Es evidente que tanto los pacientes trasplantados por la inmunosupresión como los que están en diálisis, por las alteraciones del sistema inmune asociadas con la uremia, presentan un estado de inmunodeficiencia que les hace más susceptibles a la infección. Estas alteraciones afectan principalmente a la inmunidad celular4, como la disminución en la respuesta proliferativa de los linfocitos, deficiencia de interleucina-2, déficit de linfocitos B periféricos y aumento de la apoptosis celular5-7. Puesto que la ITL se caracteriza por una importante respuesta inmune de tipo celular (en ausencia de micobacterias detectables), una alteración de la misma puede llevar a un aumento en la reactivación de la TBC en los pacientes urémicos y a una hiporrespuesta en las pruebas que se basan en la hipersensibilidad retardada.
DIAGNÓSTICO DE LA INFECCIÓN TUBERCULOSA
La forma habitual para diagnosticar la infección tuberculosa es la PT que pone de manifiesto, tras la inyección de un derivado proteico purificado (PPD), un estado de hipersensibilidad previo del organismo frente a dicha sustancia. La tuberculina utilizada en Europa es la PPD RT-23. En los últimos años se han investigado y aprobado nuevos métodos diagnósticos basados en la cuantificación in vitro de la respuesta inmune celular. Estos métodos, denominados genéricamente en la bibliografía anglosajona con el acrónimo de IGRA (Interferon-Gamma-Release Assays) detectan la liberación de interferón-gamma en respuesta a antígenos tuberculosos específicos8. El interferón-gamma es una molécula imprescindible en la respuesta inmune protectora frente a dicho microorganismo. Esta citoquina, producida por los linfocitos T CD4+, CD8+ y NK, activa a los macrófagos infectados con la consiguiente liberación de IL-1 y TNF-alfa, que limitan el crecimiento y multiplicación de las micobacterias. Los individuos con deficiencias en los receptores o en los genes que codifican la síntesis de esta molécula son más susceptibles de presentar infecciones micobacterianas con mayor frecuencia y de mayor gravedad. Al igual que los pacientes sometidos a tratamientos inmunosupresores que interfieran con dichas vías de señalización de la respuesta inmune.
ENSAYOS IN VITRO BASADOS EN LA PRODUCCIÓN DE INTERFERÓN (IGRA)
Existen dos técnicas comercializadas para el diagnóstico in vitro de la infección tuberculosa: el QuantiFERON-TB-Gold In Tube (Cellestis®, Victoria, Australia)9 y el T-SPOT.TB (Oxford Immunotec®, Oxford, Reino Unido)10. La primera generación de QuantiFERON TB, aprobada por la Food and Drugs Administration (FDA) de los estados Unidos en el año 2001, detectaba la liberación de interferón-gamma en respuesta a PT. En el año 2004, la FDA aprobó la segunda generación de esta prueba diagnóstica, denominada QuantiFERON-TB Gold, que a diferencia de la primera generación, no utilizaba como antígenos micobacterianos los de la PT, sino péptidos sintéticos que simulan antígenos más específicos como son el Early Secreted AntigenicTarget-6 (ESAT-6) y el Culture Filtrate Protein-10 (CFP-10). Estas dos moléculas están codificadas por la región RD-1 del genoma de Mycobacterium tuberculosis e incrementan significativamente la especificidad con respecto a la PT. Estos antígenos están ausentes en M. bovis y en la mayoría de las micobacterias no tuberculosas (excepto M. kansasii, M. marinum o M. szulgai). En la actualidad ya se encuentra comercializada la tercera generación de esta prueba, denominada QuantiFERON-TB Gold In Tube (QFT-GIT), que incorpora un tercer antígeno micobacteriano: el TB 7.7 y tubos específicamente diseñados para esta prueba en los que debe recogerse la muestra de sangre.
VALOR DE QTF-GIT Y T.SPOT.TB EN LA PREDICCIÓN DEL DESARROLLO DE ENFERMEDAD TUBERCULOSA
Para una persona con una PT positiva, el riesgo de desarrollar tuberculosis activa se estima en un 5-10%11,12. Sin embargo, existen pocos estudios longitudinales que nos permitan concluir la capacidad de los IGRA para predecir el riesgo de desarrollar TBC activa.
En un estudio realizado en Alemania en que participaron 601 contactos cercanos a personas con baciloscopia y cultivo positivo para M. tuberculosis, el QFT-GIT obtuvo un mejor rendimiento en la predicción de TBC activa13 que la PT, utilizando un punto de corte de 5 mm. Cinco (2,3%) de los 219 contactos con induración >5 mm en la PT desarrollaron TBC, mientras que seis (14,6%) de los 41 contactos con resultados positivos para QFT-GIT desarrollaron la enfermedad. Sin embargo, un 59% de los contactos tenían una induración (PT) entre 5 y 9 mm. La proporción de los que se consideran positivos por PT con un corte de 10 mm que desarrollaron TBC activa (cinco de los 90 [5,6%]) fue similar a la proporción positiva de QFT-GIT (6 de 41 [14,6%]). Además, sólo en 2 de los 6 contactos con resultados positivos QFT-GIT que desarrollaron TBC activa hubo confirmación microbiológica. En otro estudio la sensibilidad para predecir la posterior TBC activa no fue diferente para las dos pruebas14.
Otro estudio sobre 339 inmigrantes en los Países Bajos dio como resultado que la PT y el QFT-GIT tienen un valor similar en la predicción de TBC activa15. Se realizó un seguimiento durante 2 años a aquellos contactos con PT >5 mm entre los 0 y 3 meses después del diagnóstico del paciente índice. Nueve (3,1%) de 288 contactos con PT >10 mm desarrollaron TBC activa, siete (3,8%) de 184 con PT >15 mm, cinco (2,8%) de 178 con un resultado positivo QFT-GIT, y seis (3,3%) de 181 con un T-SPOT.TB positivo desarrollaron a su vez la enfermedad. La sensibilidad para la detección del desarrollo de TBC activa en el período de seguimiento fue del 100% para una PT con un punto de corte de 10 mm, del 88% para una PT con un punto corte de 15 mm, del 63% para QFT-GIT y del 75% para T-SPOT.TB. A pesar de que PT con un punto corte de 10 mm identificaba el mayor número de contactos que desarrollaron TBC activa (100%), y QFT-GIT identificaba el menor número de contactos que desarrollaron TBC activa (5/[63%]), la sensibilidad de las dos pruebas no fue diferente. A la vista de todo lo publicado no parece que los IGRA aporten grandes ventajas en la predicción del desarrollo de enfermedad tuberculosa en comparación con la PT.
USO DE QTF-GIT Y T.SPOT.TB EN ESTUDIOS DE CONTACTOS
Hasta el momento se han realizado numerosos trabajos basados en el estudio de contactos en TBC. Inicialmente se basaron en la PT; desde la incorporación de los IGRA, estos últimos han sido objeto frecuente de investigación en este grupo16, 7. En dos trabajos se observó que una mayor exposición reciente (mayor duración de la exposición o mayor número de bacilos ácido-alcohol resistentes en los esputos) se asociaba con más positivos para IGRA que con PT, lo que sugiere que los IGRA podrían ser mejores en la detección de infección reciente.
SENSIBILIDAD DE LOS TESTS DE CRIBADO
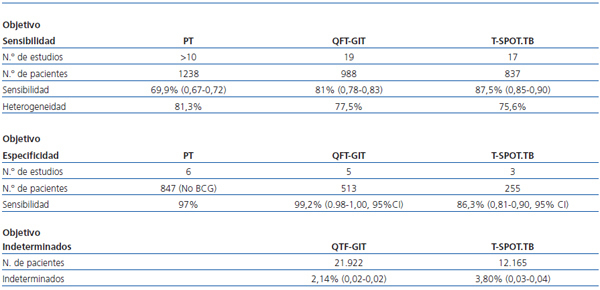
Existen dos metanálisis18, 9 que resumen los resultados que se han obtenido hasta ahora con los IGRA cuyas conclusiones quedan reflejadas en la tabla 1.
RESULTADOS NO VÁLIDOS PARA AMBAS PRUEBAS
Resultados indeterminados para QTF-GIT
Sobre un total de 21.922 pacientes, 469 (2,14%) presentaron resultados indeterminados (IC 95% 0,02-0,023).
Resultados indeterminados para T-SPOT.TB
Sobre un total de 12.165 pacientes, 462 (3,80%) fueron indeterminados (IC 95% 0,035-0,042). Si se añadían 80 casos en los cuales no había suficientes células disponibles para realizar la prueba, el número de resultados indeterminados asciende a 4,46 (IC 95% 0,041-0,048).
La diferencia en la tasa de resultados indeterminados entre los dos IGRA es mayor para el QTF-GIT.
Resultados indeterminados en pacientes inmunodeprimidos
En el caso del QTF-GIT aumentan hasta el 4,42% y en el caso del T.SPOT.TB hasta el 6,12%.
VENTAJA DE LAS TÉCNICAS DE DETERMINACIÓN DE IGRA SOBRE LA PRUEBA DE LA TUBERCULINA
Estas técnicas ofrecen importantes ventajas sobre la PT: 1) no presentan interferencias con la vacuna BCG; 2) evitan la subjetividad de la interpretación y la visita de lectura, y 3) incorporan un control positivo que proporciona valiosa información a la hora de interpretar una prueba, aparentemente negativa, como verdadera negativa o indeterminada (errores técnicos o inmunosupresión).
Experiencia en pacientes en diálisis
Debido a las alteraciones en el sistema inmunológico, los pacientes en diálisis son particularmente susceptibles a desarrollar TBC activa, llegando a tener TBC con una incidencia hasta ocho veces superior a la población20 y asociando una elevada mortalidad, por lo que la detección de la ITL en esta población es una cuestión importante. Durante décadas, la PT se ha utilizado para detectar la tuberculosis latente, con pobres resultados en estos pacientes con una tasa de anergia que puede llegar al 44%21-24. A pesar de que se están empezando a publicar estudios sobre el valor de los IGRA en la detección de la ITL, comparándolos en ocasiones con la tuberculina, disponemos de pocos datos sobre la sensibilidad y la tasa de resultados indeterminados en pacientes con enfermedades renales en general y en tratamiento con técnicas sustitutivas en particular.
Hasta hoy no se disponía de estudios similares en la población en DP. En el estudio publicado en este número, se analiza en 54 pacientes en DP el valor de los IGRA frente a la PT en la detección de la ITL con resultados esperanzadores. Al igual que en los trabajos realizados en pacientes en HD, hay un porcentaje no despreciable de resultados indeterminados, por lo que es clavela acumulación de nuevas series para afianzar y matizar los resultados. En el artículo se utiliza como gold standard la valoración por un neumólogo experto en la detección de ITL y los autores llegan a la conclusión de que los IGRA pueden complementar a la prueba de la tuberculina, pero no hay evidencia suficiente todavía.
Pacientes con trasplante renal
La prevalencia de TBC entre los receptores de trasplante renal ha sido ampliamente publicada. La incidencia de ITL entre estos pacientes se estima que es de 20-70 veces superior a la de la población general25. En estos pacientes, la TBC contribuye a la disfunción del injerto, tanto a través de efectos directos sobre el injerto, como de las interacciones medicamentosas, y aumenta la mortalidad26. Reducir el riesgo de TB es una prioridad importante en el trasplante de órganos, especialmente en los países en los que la enfermedad es endémica. El tratamiento antituberculoso es complicado, especialmente con los tuberculostáticos que inducen el citocromo P450 (rifampicina)27 o por la disfunción hepática inducida por la isoniacida28. Los resultados sobre IGRA en trasplante de órgano sólido son controvertidos, mientras en algunos estudiso es similar a la PT, en otros la sensibilidad es mayor25,29.
Futuro del uso de los IGRA
Con los conocimientos actuales, la cuestión es si los IGRA podrían sustituir a la PT para descartar infección tuberculosa en los pacientes inmunodeprimidos. En espera de nuevos estudios al respecto podemos afirmar que: 1) actualmente no se dispone de datos suficientes sobre el desarrollo de TBC a largo plazo que nos permitan tomar la decisión de tratar o no basándonos únicamente en el resultado de los IGRA en pacientes en TRS; 2) las bases teóricas de los IGRA indican que estas técnicas miden un tipo de respuesta inmunitaria diferente a la que interviene en la respuesta de hipersensibilidad retardada a la PT; 3) a diferencia de lo que ocurre en el estudio de contactos, en los pacientes inmunodeprimidos, es tan importante la infección tuberculosa reciente como la remota; 4) parece que no hay todavía evidencia suficiente para que los IGRA sustituyan a la prueba de la tuberculina, y 5) podemos concluir que los IGRA complementan a la prueba de la tuberculina, ya que la realización de ambas simultáneamente aumenta la probabilidad diagnóstica de TBC. En cualquier caso los IGRA representan un avance notable en el diagnóstico de la infección tuberculosa.
CONCEPTOS CLAVE
Tabla 1. Resultados de los estudios sobre los distintos métodos diagnósticos en la detección de tuberculosis confirmada