La cistitis hemorrágica se define como una inflamación de la mucosa vesical que produce un sangrado difuso agudo o subagudo1. Es el resultado de la activación inapropiada de citocinas proinflamatorias, que destruyen la mucosa y el corion por apoptosis inflamatoria (piroptosis), lo cual conduce a la apertura de los microvasos a la luz vesical. Las principales causas de la piroptosis vesical son los agentes patógenos bacterianos o virales, las radiaciones ionizantes o la acroleína, un metabolito urinario de la ciclofosfamida y la ifosfamida2.
El virus BK es una de las causas más importantes de cistitis hemorrágica de inicio tardío en pacientes sometidos a trasplante de células hematopoyéticas (TCH). La evidencia para el tratamiento de la cistitis hemorrágica asociada al virus BK (BKV-HC) es limitada, siendo el cidofovir una de sus alternativas terapéuticas3. Cidofovir es un análogo citidínico que presenta actividad in vitro e in vivo frente al citomegalovirus humano (CMVH) debido a que suprime su replicación mediante la inhibición selectiva de la síntesis del ADN viral4. El uso de este fármaco en BKV-HC sería fuera de ficha técnica.
Se describe el caso de un varón de 53 años sin alergias medicamentosas y con antecedentes personales de dislipemia e hipertensión arterial.
El paciente es diagnosticado en el 2016 de una leucemia mielomonocítica crónica (LMC) y, tras varios ciclos de quimioterapia (MAZE: amsacrina-azacitidina-etopósido; IDA-ARA-C: idarubicina-citarabina), es sometido a un alotrasplante de progenitores hematopoyéticos (ALO-TPH) en mayo de 2018.
Dos meses después el paciente acude al hospital de día de hematología (HDH) para recibir tratamiento con foscarnet contra el citomegalovirus (CMV), adquirido tras el ALO-TPH, refiriendo durante los últimos días hematuria acompañada de disuria y ardor. Con el presente cuadro se ingresa al paciente y se le diagnostica de cistitis hemorrágica.
Después de varias pruebas para descubrir la etiología de la enfermedad, se detectan copias de poliomavirus BK en orina. Tras estos hallazgos y tras la comunicación con el centro regional de referencia, se propone el uso de cidofovir intravenoso a una dosis día 400mg/24h/durante 2 semanas (inducción) y luego cada 15 días hasta la erradicación del virus.
Antes de comenzar el tratamiento con cidofovir se evaluó la función renal (>60ml/min) y se fijó la fecha del inicio del tratamiento: 03/07/18. Para disminuir la toxicidad renal se administró probenecid conjuntamente con el cidofovir.
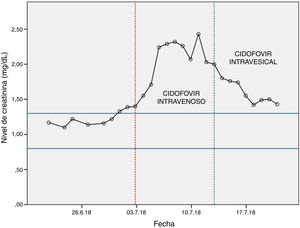
Después de la primera dosis de cidofovir se observó un aumento significativo de los niveles de creatinina en sangre (fig. 1), así que la unidad de hematología se puso en contacto con farmacia para encontrar una solución al problema.
Como se ha comentado anteriormente, la principal toxicidad del cidofovir es la nefrotoxicidad, dosis dependiente. La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) informa que no se ha evaluado la seguridad de cidofovir en pacientes en tratamiento con otros agentes que se sabe que son potencialmente nefrotóxicos (por ejemplo: tenofovir, aminoglucósidos, anfotericina B, foscarnet, pentamidina intravenosa, adefovir y vancomicina)4. En nuestro caso, la nefrotoxicidad del cidofovir se vio potenciada con el uso concomitante del foscarnet, que no podía suprimirse puesto que el paciente continuaba con copias positivas de CMV en plasma.
Ante este panorama, desde el servicio de farmacia realizamos una búsqueda bibliográfica localizando una revisión sistemática que comparaba el tratamiento intravenoso e intravesical del cidofovir en el tratamiento de cistitis hemorrágica asociada a poliomavirus BK tras un ALO-TPH, donde se mostraba una elevada tasa de respuestas completas por vía intravesical, pero sin toxicidad renal5.
En base a estos resultados se recomendó el uso de cidofovir intravesical 5mg/kg diluido en 60ml de suero fisiológico al 0,9% e instilado durante una hora en vejiga, con cambios de postura (decúbito supino, decúbito lateral izquierdo, decúbito prono y decúbito lateral derecho), cada 15min con el fin de que el fármaco penetrase en toda la mucosa de la vejiga (recomendación de enfermería).
La primera dosis de cidofovir intravesical se administró el 13/07/18 y tras ella se observó una mejoría de la función renal (fig. 1). Tras la primera instilación de cidofovir intravesical se repitió la PCR en orina para detectar copias de poliomavirus BK, siendo el resultado negativo, por lo que se interrumpió el tratamiento con cidofovir.
Nuestro caso aporta que el uso de cidofovir intravesical se puede proponer como una alternativa eficaz en pacientes que presenten un aclaramiento de creatinina ≤55ml/min (límite para la contraindicación de cidofovir intravenoso).