La nefritis lúpica (NL) es la primera manifestación en morbimortalidad, del lupus eritematoso sistémico (LES) y condiciona el pronóstico de los pacientes. En torno a un 30% de los casos no consiguen respuesta completa, y un 10-30% de los casos evolucionan a enfermedad renal terminal en 10 años1. Presentamos 2 casos de NL refractaria tratados con voclosporina, un inhibidor de la calcineurina (ICN) aprobado en España en 2024 para la NL proliferativa o mixta en combinación con micofenolato mofetil (MMF)2,3.
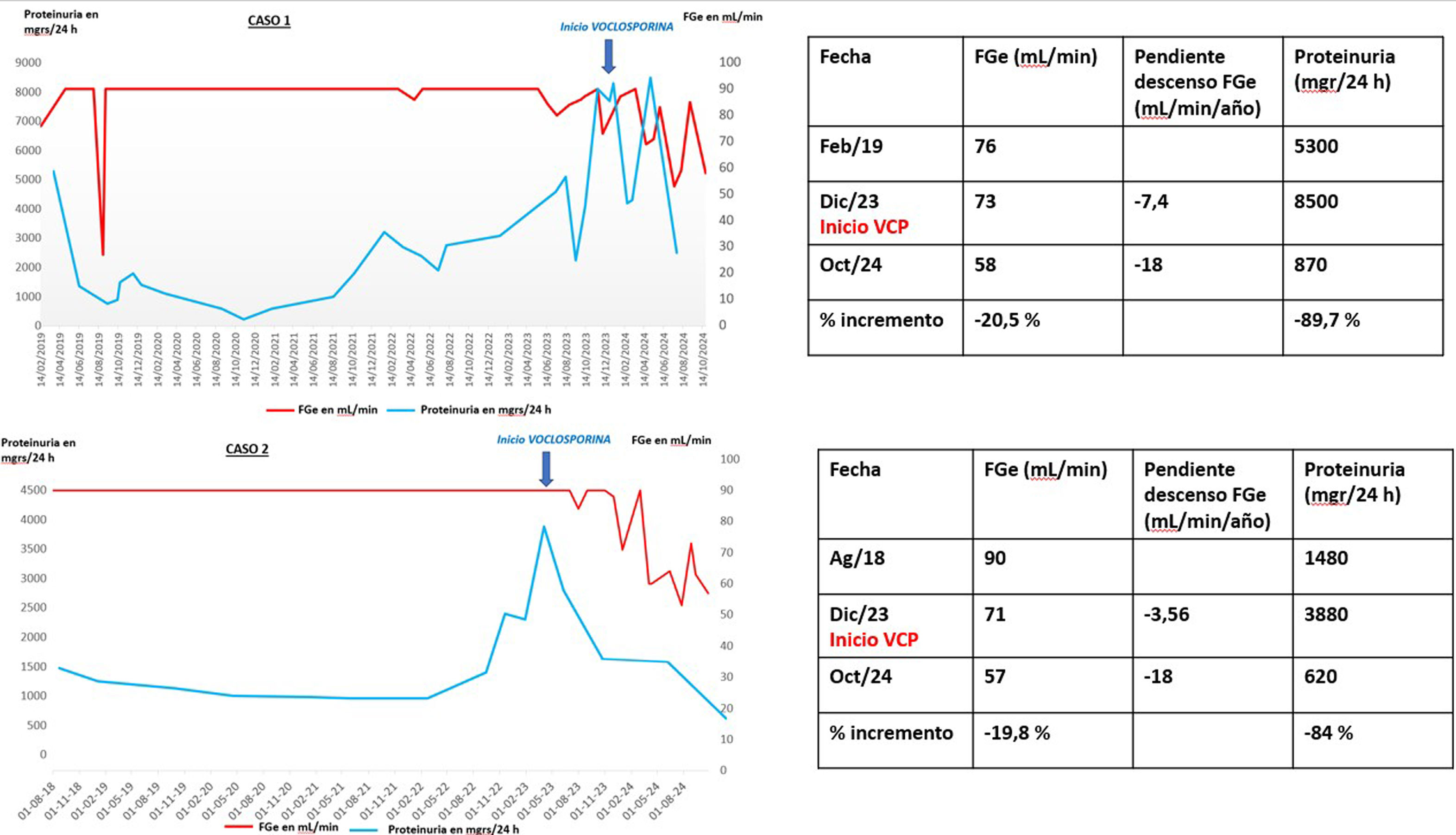
El primer caso es una mujer venezolana de 36 años, con antecedentes de hipertensión arterial (HTA) que comienza en 2014 durante su posparto con edema de manos, Raynaud, síndrome seco, leuco y trombocitopenia e hipocomplementemia con autoanticuerpos antinucleares (ANA), anti U1-RNP, SSa, SSb, Sm y antifosfolípido positivos. Inicia tratamiento con corticoides, hidroxicloroquina y azatioprina. Desde entonces desarrolla distintas complicaciones que incluyen proteinuria nefrótica con filtrado glomerular (FG) conservado en 2016 y pleuropericarditis en 2017. Se traslada a España y comienza seguimiento en nuestro centro. Se realiza biopsia renal con diagnóstico de NL clase V. Entre 2019 y 2023 por distintas complicaciones clínicas, infecciosas y ausencia de remisión renal, concatena diversos tratamientos que no consiguen inducir remisión (tabla 1). Se realiza nueva biopsia renal con resultado de NL clase III+V con un índice de actividad de 5/24 y de cronicidad de 5/12. Se decide iniciar anifrolumab y voclosporina a dosis inicialmente reducida para minorizar el riesgo de infección, aumentada a dosis plena en 3 meses tras constatar tolerancia y ausencia de complicaciones infecciosas periodo en el que se consigue un descenso de la actividad de la enfermedad (anti-DNA negativizados, linfopenia resuelta e hipocomplementemia en menor grado), de la proteinuria mayor de un 89% (fig. 1), cumpliendo criterios de remisión DORIS4 y permitiendo disminuir sensiblemente la dosis de corticoides. La única complicación reseñables es una recidiva de pioderma gangrenoso tratado satisfactoriamente con micro injertos de piel. En la actualidad mantiene tratamiento con anifrolumab, MFM, voclosporina y prednisona.
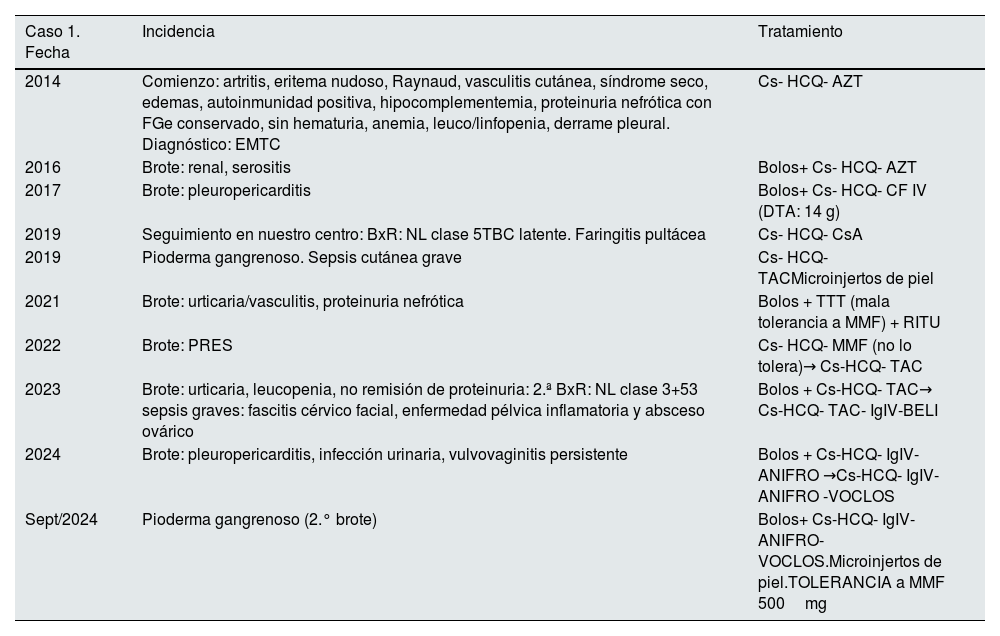
Evolución clínica y de tratamiento de los casos 1 y 2
| Caso 1. Fecha | Incidencia | Tratamiento |
|---|---|---|
| 2014 | Comienzo: artritis, eritema nudoso, Raynaud, vasculitis cutánea, síndrome seco, edemas, autoinmunidad positiva, hipocomplementemia, proteinuria nefrótica con FGe conservado, sin hematuria, anemia, leuco/linfopenia, derrame pleural. Diagnóstico: EMTC | Cs- HCQ- AZT |
| 2016 | Brote: renal, serositis | Bolos+ Cs- HCQ- AZT |
| 2017 | Brote: pleuropericarditis | Bolos+ Cs- HCQ- CF IV (DTA: 14 g) |
| 2019 | Seguimiento en nuestro centro: BxR: NL clase 5TBC latente. Faringitis pultácea | Cs- HCQ- CsA |
| 2019 | Pioderma gangrenoso. Sepsis cutánea grave | Cs- HCQ- TACMicroinjertos de piel |
| 2021 | Brote: urticaria/vasculitis, proteinuria nefrótica | Bolos + TTT (mala tolerancia a MMF) + RITU |
| 2022 | Brote: PRES | Cs- HCQ- MMF (no lo tolera)→ Cs-HCQ- TAC |
| 2023 | Brote: urticaria, leucopenia, no remisión de proteinuria: 2.ª BxR: NL clase 3+53 sepsis graves: fascitis cérvico facial, enfermedad pélvica inflamatoria y absceso ovárico | Bolos + Cs-HCQ- TAC→ Cs-HCQ- TAC- IgIV-BELI |
| 2024 | Brote: pleuropericarditis, infección urinaria, vulvovaginitis persistente | Bolos + Cs-HCQ- IgIV-ANIFRO →Cs-HCQ- IgIV-ANIFRO -VOCLOS |
| Sept/2024 | Pioderma gangrenoso (2.° brote) | Bolos+ Cs-HCQ- IgIV-ANIFRO-VOCLOS.Microinjertos de piel.TOLERANCIA a MMF 500mg |
| Caso 2. Fecha | Incidencia | Tratamiento |
|---|---|---|
| 2018 | Comienzo: artritis, eritema malar, autoinmunidad positiva, hipocomplementemia, proteinuria nefrótica con FGe conservado, sin hematuria, anemia, leuco/linfopenia, derrame pleural., asma grave, síndrome de pulmón encogido’. Diagnóstico: LES | Cs- HCQ- AZT |
| 2021 | Brote: articular, pulmonar, renal: BxR: NL clase 3 | Cs- HCQ- AZT- BELI- RITU |
| 2022 | Brote: sistémico, hematológico, articular, pulmonar | Cs- HCQ- TTT→ intolerancia a MMF |
| 2022 | Brote: pulmonar | Bolos + Cs- HCQ- AZT- RITU |
| 2023 | Brote: sistémico, hematológico, articular, pulmonar + síndrome de activación macrofágica | Cs- HCQ- CF IV→ leucopenia grave: Cs- HCQ-IgIV- ANAKINRA |
| 2023 | Brote: sistémico, hematológico, articular, pulmonar, cutáneo (urticaria/vasculitis) + fiebre prolongada y síndrome constitucional. | Bolos + Cs- HCQ- ANAKINRA- ANIFRO → Cs- HCQ- ANAKINRA- BELI- MFA a dosis muy baja |
| 2023 | Brote: pulmonar-serositis | Cs- HCQ- ANAKINRA- VOCLOS |
ANIFRO: anifrolumab; AZT: azatioprina; BELI: belimumab; BOLOS: 3 dosis de metilprednisolona 250 mg; BxR: biopsia renal; Cs: corticoides (prednisona); CFIV: ciclofosfamida intravenosa; CsA: ciclosporina A; DTA: dosis total acumulada; EMTC: enfermedad mixta del tejido conectivo; HCQ: hidroxicloroquina; IgIV: inmunoglobulinas intravenosas; MFA: ácido micofenólico; MMF: micofenolato mofetil; NL: nefropatía lúpica; PRES: síndrome de encefalopatía posterior reversible; RITU: riruximab; TAC: tacrolimus; Tbc: tuberculosis; TTT: triple terapia; VOCLOS: voclosporina.
El segundo caso es el de una mujer venezolana de 44 años con antecedentes de hipotiroidismo, asma y anemia ferropénica de origen ginecológico que comienza en 2016 con artritis, lupus cutáneo, síndrome de pulmón encogido, proteinuria nefrótica con FG conservado, hipocomplementemia y ANA con anti-DNA positivos. Inicia tratamiento con corticoides, hidroxicloroquina y azatioprina. En 2020 por artritis, serositis pleuropericárdica y proteinuria inicia seguimiento en nuestro centro. Se realiza biopsia renal que muestra una NL clase III (índice de cronicidad 2/12). Desde entonces se concatenan varios brotes sistémicos y renales graves a pesar de múltiples tratamientos (tabla 1). En 2022 comienza con un síndrome de activación macrofágica. Se añade al tratamiento anakinra con buena respuesta sistémica, pero refractariedad renal por lo que en noviembre de 2024 se inicia tratamiento con voclosporina y MFM a baja dosis por intolerancia digestiva. La proteinuria desciende un 84% en los 3 meses siguientes (fig. 1) y alcanza remisión renal y sistémica completas salvo por datos de actividad biológica (linfopenia, DNA a títulos altos e hipocomplementemia) con dosis de corticoides en descenso.
En ambos casos se observó un descenso rápido y sostenido en la proteinuria, un buen perfil de tolerancia, control metabólico y seguridad, y se pudo disminuir la dosis de corticoides. Paralelamente, se constató un descenso del FG en torno al 20% por circunstancias funcionales y de carácter reversible.
La voclosporina es un inhibidor de la calcineurina (ICN) de estructura similar a la ciclosporina A, modificado en un grupo funcional del resto aminoácido 1, lo que le otorga un mayor poder de unión a la calcineurina y una cinética lineal que permite no monitorizar sus niveles plasmáticos. Actúa sobre el proceso de activación de los linfocitos al inhibir la vía NFTAC dependiente de la calcineurina, lo que produce descenso en la síntesis de citoquinas, entre ellas interleuquina 2, una menor proliferación linfocitaria y estabilización del citoesqueleto podocitario y la arquitectura del diafragma de hendidura por su acción sobre la sinaptopodina5. En los estudios Aurora 1 y Aurora 2 se consiguió una remisión renal completa del 41 y 50,9% con más riesgo de provocar HTA y descenso del FG de carácter reversible y funcional6–9.
Presentamos 2 casos de NL complejos, con múltiples pautas previas de tratamientos que no han sido eficaces y se han acompañado de complicaciones sistémicas infecciosas y renales graves, en los que la voclosporina ha permitido mejorar el control de la enfermedad, disminuyendo la necesidad de corticoides, mejorando notoriamente la proteinuria, y disminuyendo las complicaciones sistémicas, a pesar de un descenso del FG en torno al 20%. Solo hemos encontrado un caso publicado de asociación de voclosporina con anifrolumab10.
En definitiva, la suma de voclosporina al arsenal terapéutico en la NL abre una esperanzadora vía de tratamiento en los pacientes con proteinuria significativa que deberá ser refrendada en el futuro.
FinanciaciónEste artículo no tiene fuentes de financiación
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses