Sr. Director:
Queremos comunicar los resultados de un trabajo reciente del Laboratorio, que investiga la posibilidad de que la aldosterona tenga un papel relevante en la calcificación vascular. En breve, como método, se ha empleado un modelo in vitro sobre células normales de músculo liso vascular (CMLV) en cultivo primario, inducidas a calcificar en presencia de beta-glicerofosfato. El resultado obtenido demuestra que la aldosterona incrementa la calcificación de estas CMLV. Este efecto se inhibe por espironolactona.
Hasta hace poco tiempo, la calcificación vascular se consideraba un proceso pasivo, provocado por una respuesta no específica de los tejidos vasculares frente a diversos tipos de daño, con deposición de fosfato cálcico, principalmente en forma de hidroxiapatita. En la actualidad, se sabe que la calcificación es un proceso regulado, en el que intervienen diferentes tipos celulares y gran numero de mediadores, tanto pro- como anti-calcificantes, vg, fosfatasa alcalina (FALC), Cbfa-1, osteocalcina, y anti-calcificantes, como la proteína de gliadina de matriz (MGP), osteoprotegerina (OPG) y fetuina-A1-3. La respuesta normal de las CMLV es anticalcificante.
En la uremia, sin embargo, debido a diversas causas, como el aumento de las concentraciones de Ca y/o P en el medio, a los mencionados procesos inflamatorios y oxidativos, o simplemente al estrés por uso prolongado que acompaña al envejecimiento, este balance se altera a favor de los factores procalcificantes. Las calcificaciones vasculares urémicas en la capa media de CMLV, afectan principalmente a zonas de matriz extracelular y a la lámina elástica. Este tipo de calcificación es la principal y más precoz de las calcificaciones urémicas2.
En la actualidad, se considera a la aldosterona como un factor pro-fibrótico vascular. Este concepto ha encontrado amplia aceptación en la práctica clínica, especialmente desde la publicación del estudio RALES4. Existen numerosas evidencias de la existencia de receptores de aldosterona en las CMLV, con diferentes implicaciones funcionales5, 6. Sin embargo, y a pesar de la evidente relación en el tiempo entre el desarrollo de fibrosis y rigidez vascular y calcificación de los vasos, no se han llevado a cabo estudios que investiguen una posible relación entre ambos fenómenos. Datos antiguos de la literatura sugerían que la aldosterona podría participar en el transporte de calcio en las CMLV7. Nuestros propios datos indican que la población en diálisis y enfermedad renal avanzada presenta cifras significativamente altas de aldosterona respecto a los individuos normales (Caramelo y cols., resultados no publicados).
El motivo del presente trabajo ha sido examinar el papel de la aldosterona en la inducción de calcificaciones vasculares, en un modelo experimental reconocido, la exposición de células de CMLV a beta-glicerofosfato. Nuestra hipótesis aborda la posibilidad de que la aldosterona participe en este proceso. Como métodos, se han empleado:
Cultivo primario de CMLV de aorta bovina según el método descrito por Campbell8. Las CMLV fueron empleadas entre los pases 2 y 8.
Inducción del proceso de calcificación: Hemos utilizado un método de calcificación estandarizado e implantado en el Laboratorio9. El medio de calcificación, cambiado cada 48 h durante 12 días, se basa en el beta-glicerofosfato (10 mM) (Sigma-Aldrich, Madrid). El beta-glicerofosfato actúa como un dador de PO4-3 al ser hidrolizado por la fosfatasa alcalina.
Cuantificación de la calcificación mediante acumulación de 45Ca: Las células sometidas a proceso de calcificación se incuban en presencia de 0,5 mCi/ml de 45Ca (GE Healthcare, Barcelona). La detección de esta acumulación se realiza con líquido de centelleo UltimaGold (Perkin Elmer, Waltham, MA) y se detectaron en un contador Beckman LS6000TA.
Tinción de von Kossa: Para visualizar el proceso de calcificación, las CMLV se fijaron con Merkcofix (Merck KGaA, Darmstadt, Alemania), se incubaron con 5% nitrato de plata durante 30 minutos en oscuridad y se dejaron expuestas a la luz solar hasta que la tinción fuera observable. Las fotos se realizaron con una cámara digital Nikkon Coolpix 995 sobre un fondo iluminado.
Incubación con aldosterona: Durante todo el proceso calcificante, las CMLV se incubaron con aldosterona o vehículo agregados al medio. En cada cambio de medio se agregó aldosterona a la concentración correspondiente.
Datos estadísticos: Los datos se expresaron como media ± error estándar de la media. Excepto indicación en contrario, todos los valores corresponden a un mínimo de 5 experimentos con muestras en triplicado. Las comparaciones se hicieron mediante la prueba t de Student, emparejada o no emparejada y la prueba de ANOVA con test de Scheffé. Un valor de P < 0,05 se consideró significativo. Todos los cálculos se realizaron con el paquete estadístico SPSS 10.0, para Windows.
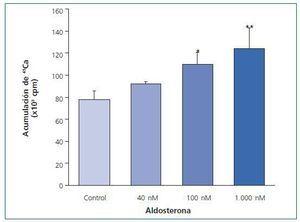
Los hallazgos realizados demuestran la validez del modelo en cuanto a acumulación de calcio en forma de cristales von Kossa positivos y 45Ca. El incremento alcanzó en general cifras superiores a 250%. El resultado experimental con aldosterona demuestra un incremento de captación de 45Ca significativo, aunque a concentraciones altas de la hormona (fig. 1). Este incremento resultó inhibido en forma masiva (85 ± 4% de inhibición, p < 0,01) en presencia de espironolactona (10-7 y 10-6 M).
Jaffe y cols., acaban de referir un resultado similar pero en un modelo extremadamente selectivo, células calcificantes, no extrapolable a la generalidad de las CMLV10. Nuestros resultados indican que la aldosterona potencia la calcificación en CMLV de tipo normal, lo que extiende ampliamente el marco posible de acción calcificante de la hormona. De importancia, la marcada inhibición por espironolactona indica que se trata de un efecto a nivel del receptor mineralocorticoide.
Si bien es conocido que la aldosterona induce cambios pro-fibróticos en la composición proteica de la pared arterial4, en nuestro conocimiento, excepto en el trabajo de Jaffe y cols.10, se desconocía que influyera también en el proceso de calcificación. Si bien las concentraciones a las que hemos detectado el efecto calcificante son elevadas, las interacciones que ocurren in vivo con otros factores pro-calcificantes pueden ser cruciales para que concentraciones más bajas de aldosterona actúen como coadyuvante de otros mediadores.
La existencia de calcificaciones extraóseas en pacientes con hiperaldosteronismo de comienzo temprano en la infancia, como los síndromes de Bartter y Gitelman, son otro posible ejemplo donde la relación hiperaldosteronismocalcificación puede tener un papel hasta ahora no sospechado11, 12.
En conjunto, el presente trabajo aporta nuevos datos en cuanto a los factores que intervienen en la calcificación vascular. No se puede minimizar el interés terapéutico potencial de estos resultados al emplear antagonistas aldosterónicos. De comprobarse que estos actúan sobre el proceso de calcificación vascular, podrían agregarse una nueva herramienta terapéutica a las ya disponibles para el control de las calcificaciones.
Figura 1.