La enfermedad aterotrombótica (EA) es una enfermedad progresiva que provoca uno de los mayores índices de morbimortalidad en las sociedades occidentales con la presentación de sus manifestaciones clínicas más habituales, el infarto agudo de miocardio y el accidente vascular cerebral, provocando muerte súbita por infarto, sin clínica previa, en el 50% de los hombres y en el 64% de las mujeres1.
Una de las principales herramientas para controlar la incidencia de las enfermedades vasculares es establecer intervenciones de prevención. Disponemos de fórmulas que permiten estimar el riesgo cardiovascular (Framingham, Score, etc.)2. Se basan en datos de estudios poblacionales a partir de los cuales se obtiene el riesgo de sufrir un evento/mortalidad de causa cardiovascular a los 5 o 10 años3. Este sistema de cálculo de riesgo, si bien es fácilmente generalizable, disponible y universal, presenta una serie de dificultades. La principal es que la sensibilidad para la detección de individuos susceptibles de tener un evento cardiovascular es baja. Grandes estudios evidencian que el 62% de los sujetos con antecedentes de infarto agudo de miocardio no presentan ningún factor de riesgo cardiovascular o tan sólo uno4, hecho que impide su correcta identificación y, por tanto, establecer medidas preventivas eficaces.
En los últimos años han existido grandes avances tecnológicos en las técnicas de imagen aplicadas a la medicina y específicamente en el área de la patología vascular. A continuación se exponen las ventajas, inconvenientes y aplicaciones tanto en la población general como en la enfermedad renal crónica (ERC).
POBLACIÓN GENERAL
Para el diagnóstico y prevención de enfermedad cardiovascular (ECV) se han empleado varios métodos. La calcificación de las arterias coronarias estudiadas mediante tomografía axial computarizada (TAC) helicoidal o multidetector permite cuantificar el contenido de calcio (scorede calcio coronario), aunque no es útil en aquellos pacientes con riesgo bajo estimado por los métodos tradicionales5. Tiene gran especificidad para diagnosticar aterosclerosis coronaria, y según algunos estudios se relaciona directamente con la mortalidad a lo largo del tiempo6, pero es una técnica cara, que requiere tecnología avanzada y por tanto no es aplicable para el diagnóstico precoz en la población general; además, con el scorede calcio coronario se diagnostica la presencia de calcio en las coronarias, pero no se pueden diagnosticar estadios previos de enfermedad arterial, y la EA es una enfermedad evolutiva en la que la calcificación ocurre en los últimos estadios.
En cuanto a la ultrasonografía intravascular7: la coronariografía se ha complementado recientemente con la aplicación de los ultrasonidos que permiten un diagnóstico más preciso de la arteriosclerosis coronaria; sin embargo, éste es un método cruento, caro y, por tanto, tampoco aplicable para detectar precozmente la EA a nivel poblacional.
La ecografía carotídea aporta múltiples ventajas sobre los métodos anteriores, aunque su uso para el diagnóstico precoz de enfermedad ateromatosa no está generalizado. La ecografía de troncos supraaórticos se emplea para estudiar pacientes con enfermedad arteriosclerosa sintomática, especialmente aquellos que han sufrido un accidente vascular cerebral. Al tratarse de pacientes que han sufrido un evento derivado de la patología arterial, poco podemos hablar de ventajas preventivas; únicamente de diagnóstico o de confirmación de sospecha diagnóstica y para establecer la indicación quirúrgica.
La aplicación de esta técnica en el diagnóstico precoz de la EA requiere una formación cuidadosa del técnico explorador y del especialista que interpreta las imágenes, para que los parámetros derivados sean útiles en el diagnóstico precoz de esta patología.
La medición del grosor íntima-media (GIM) mediante ecografía carotídea fue identificada por Pignoli et al. en 1984 y validada por los mismos autores en 1986, estableciendo la correlación entre el grosor de la pared arterial medida por ecografía y los resultados anatomopatológicos8. A partir de ese momento la ecografía carotídea se reconoce como una técnica con potenciales aplicaciones en el campo de la arteriosclerosis, pero después de más de 20 años no forma parte de la práctica clínica habitual para el diagnóstico de enfermedad arterial por la variabilidad en las técnicas utilizadas y en los parámetros derivados. Se dio un definitivo paso adelante en la generalización de la técnica en la práctica clínica en la XIII European Stroke Conference en 2004, (Manheim IMT Consensus)9.
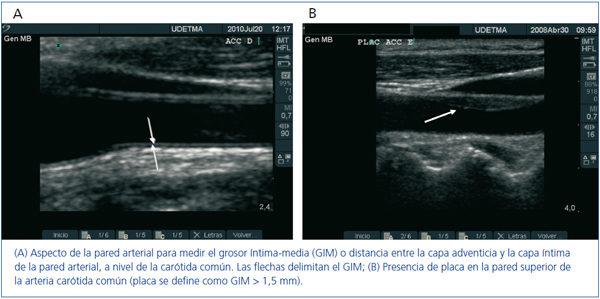
La ecografía de arterias carótidas –medida del GIM y detección de placas de ateroma (figura 1a y b)– es un potente indicador del estado de salud vascular global. La medida del GIM es un marcador implementado y aceptado para la predicción de ECV10.
En ensayos clínicos, la medida del GIM se usa paralelamente a los factores de riesgo tradicionales, remarcando la utilidad y la importancia de emplear medidas no invasivas para evaluar los efectos de los factores de riesgo sobre la pared del vaso. A lo largo de los años, los ensayos clínicos han proporcionado resultados que refuerzan el papel de la medida del GIM para la prevención de eventos cardiovasculares (cuanto mayor es el grosor del GIM, mayor es el riesgo de infarto de miocardio e infarto cerebral)11.
La medida del GIM ha sido aceptada como marcador sustituto para diagnóstico de aterosclerosis, y es usada por la US Food and Drug Administration (FDA) y por la European Agency for the Evaluation of Medicinal Products. Actualmente la medición del GIM representa la técnica no invasiva de elección más utilizada en ensayos clínicos para determinar la arteriosclerosis, y las guías clínicas y sociedades científicas recomiendan su uso para una evaluación más precisa del estado cardiovascular en poblaciones seleccionadas12 y su empleo en programas de prevención de patología cardiovascular13. Respecto a los incrementos del GIM, una diferencia de GIM de 0,1 mm, adaptada por edad y sexo, estableció un incremento del 10-15% de futuro infarto de miocardio, y del 13-18% de riesgo de infarto cerebral11.
Recientemente Davidsson14 ha documentado que la ratio de eventos cardiovasculares en sujetos con placa en la carótida es de 2,09 (95%, IC 1,05-4,16; p = 0,03) en un análisis multivariable de 391 hombres en Suecia. Nambi et al.15 han publicado los últimos resultados del estudio ARIC, demostrando la relación entre el aumento del GIM y/o la presencia de placas de ateroma y los eventos cardiovasculares. Reportan el rol predictivo de la ecografía carotídea (GIM y placas) en un análisis de 13.145 sujetos sanos. Recogieron 1.812 eventos cardiovasculares en un período de seguimiento de 15 años. El área bajo la curva aumentó de forma significativa al incluir el GIM y la presencia de placas en la lista de factores de riesgo cardiovascular convencionales.
ECOGRAFÍA CAROTÍDEA EN LA ENFERMEDAD RENAL CRÓNICA
Las tablas de cálculo de riesgo cardiovascular no han sido específicamente diseñadas para su aplicación en los pacientes con ERC, que presentan aspectos diferenciales en los principales factores de riesgo respecto a la población general. En esta población existe la denominada «epidemiología inversa». En estudios de pacientes en hemodiálisis no se ha encontrado asociación entre niveles séricos de colesterol ni de tensión arterial sistólica, con enfermedad coronaria, enfermedad cerebrovascular o enfermedad vascular periférica16,17. Además, existen factores «no tradicionales» y «emergentes» que participan en la patogénesis de la aterosclerosis en la ERC como la anemia, la inflamación crónica y el estrés oxidativo, o alteraciones en el metabolismo mineral que no se incluyen en las tablas de cálculo de riesgo tradicionales.
Estas evidencias, junto con la elevada incidencia de ECV en los pacientes con ERC18, han llevado a sugerir el uso de herramientas nuevas y más sensibles para la detección precoz y la prevención cardiovascular19. Las Guías de la Sociedad Europea de Cardiología recomiendan un control estricto de los factores de riesgo tradicionales en los pacientes con enfermedad renal crónica20, y la National Kidney Foundation (NKF) propone la ecografía de arterias carótidas para una valoración más precisa del estado cardiovascular de la población con enfermedad renal21.
Debido a que la patología cardiovascular también es la principal causa de morbimortalidad en la ERC22, el diagnóstico precoz de enfermedad arterial por ecografía se está implantando de forma progresiva en esta población.
No sabemos con certeza la evolución del GIM y la relación con los factores de riesgo en la ERC. Algunos estudios sugieren que el GIM aumenta en la medida que disminuye el filtrado glomerular23.
Nuestro grupo constató la elevada prevalencia y severidad de la ateromatosis en enfermos con distintos estadios de enfermedad renal (n = 409)24. Los métodos de diagnóstico utilizados fueron la ecografía de carótidas y el índice tobillo-brazo (ITB). Ambos test están validados como marcadores de predicción de eventos cardiovasculares25. Aplicamos una clasificación de enfermedad vascular basada en los resultados del ITB y de la ecografía carotídea empleando para el GIM los intervalos de referencia ajustados por edad y sexo. Encontramos una alta proporción de pacientes renales con enfermedad vascular ateromatosa muy superior a sujetos con función renal normal emparejados por edad y sexo (n = 851). Observaciones destacables de este estudio fueron la superior prevalencia de EA en los pacientes en diálisis respecto a estadios previos y la ausencia de relación entre enfermedad arterial y niveles de colesterol LDL. La presencia de placas de ateroma fue superior en pacientes en diálisis (78,3%)26 que en prediálisis (55,6%)27 y que en el grupo control (43,2%). Las variables que se asociaron de forma positiva con la ateromatosis fueron: edad, tratamiento con diálisis y niveles plasmáticos de proteína C reactiva. También en esta población el género femenino constituyó un factor protector.
La ecografía carotídea permite añadir una importante información: la detección de la calcificación vascular. La calcificación vascular es un potente marcador pronóstico de morbimortalidad, tanto en la población general como en la población con ERC. En pacientes con ERC, la calcificación vascular es más prevalente, aparece en edades más tempranas y resulta más severa28. La valoración del grado de calcificación arterial puede realizarse mediante TAC, utilizando el scorede calcificación de Agatston, que es el único método cuantitativo y que, por ello, constituye en la actualidad el patrón oro y es utilizado sobre todo en investigación clínica. También se han revelado útiles los métodos semicuantitativos, como los descritos por Adragao y Kauppila, que emplean la radiología simple, son más asequibles en la práctica clínica y han demostrado un buen poder predictivo de eventos cardiovasculares en la población con ERC.
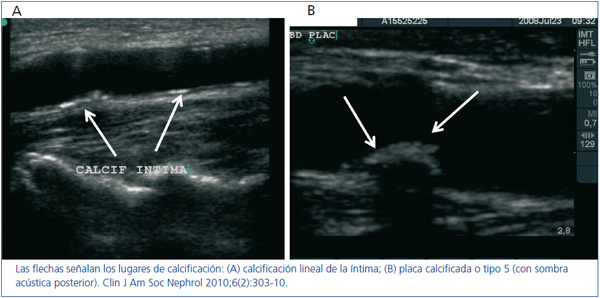
La ecografía carotídea es la única técnica que permite localizar el lugar que ocupa el calcio en la pared arterial. Nuestro grupo ha llevado a cabo un estudio para analizar este aspecto mediante ecografía de arterias carótidas y femorales, utilizando como control la arteria braquial por ser un territorio libre de ateromatosis29. Observamos que la calcificación se encontraba principalmente en la capa íntima, siguiendo dos patrones: 1) calcificación de la placa ateromatosa (figura 2a), y 2) calcificación lineal de la íntima no relacionada anatómicamente con la placa ateromatosa (figura 2b). Esta localización, no descrita anteriormente, se asoció en el análisis multivariante con: edad, fósforo plasmático, proteína C reactiva y presencia de ateromatosis. Estos resultados ponen de manifiesto que en el sustrato de la calcificación de las arterias elásticas subyace la inflamación y la ateromatosis. Aunque el fósforo plasmático sigue siendo un «enemigo a batir», debemos prestar atención a la prevención de la ateromatosis y a disminuir en lo posible el estado proinflamatorio de la ERC.
CONCLUSIONES
La ecografía carotídea es una herramienta que aporta numerosas ventajas respecto a otros métodos: a) es fácil de manejar y no requiere instalaciones complejas; puede realizarse en la consulta o junto a la cama del paciente; es barata y no invasiva; b) la información que proporciona tiene dos aspectos valiosos para el clínico: la carga ateromatosa y la severidad de la calcificación, identificando su localización en el interior de la pared vascular, y c) detecta EA desde estadios precoces, antes de que sea evidente la placa ateromatosa y por ello es un método idóneo para establecer medidas de prevención.
Actualmente no disponemos de estudios que permitan conocer el valor pronóstico de la calcificación de la placa de ateroma (placa tipo V de la clasificación de la American Heart Association) y del nuevo patrón de calcificación lineal de la íntima en pacientes renales.
El estudio español NEFRONA (www.nefrona.es)30, planteado con el objetivo de dar respuesta a numerosos interrogantes sobre la historia natural de la EA en la ERC, en el que se valorará tanto la ateromatosis como la calcificación mediante ecografía y parámetros ecocardiográficos, nos ofrecerá una información valiosa en pacientes con diferentes estadios de enfermedad renal en comparación con un grupo control con función renal normal.
Conflictos de interés
Los autores declaran conflictos de interés potenciales.
Becas: FIS (Instituto de Salud Carlos III).
Honorarios por ponencias: Shire, Abbott, Genzyme y Amgen.
Figura 1. Ecografías de arterias carótidas
Figura 2. Patrones de calcificación definidos por ecografía