La hipertensión arterial intradiálisis (HTAID) es un fenómeno poco conocido del que no existe consenso en su definición, ni datos sobre su etiología o factores relacionados, y hay poca evidencia sobre sus repercusiones.
ObjetivoDefinir la prevalencia según diferentes definiciones en 2 unidades de hemodiálisis (HD), de 2 hospitales diferentes, con distinta práctica clínica y valoración de posibles eventos después de haber pasado 18 meses.
Material y métodosEstudio observacional transversal realizado en 2 unidades de HD donde se incluyeron todos los pacientes prevalentes desde marzo de 2021 hasta septiembre de 2022. Establecimos 3 definiciones de HTAID:
- -
Def 1: Diferencia de presión arterial media (PAM) pre- y pos-HD>15mmHg.
- -
Def 2: Diferencia de presión arterial sistólica (PAS) pre- y pos-HD>10mmHg.
- -
Def 3: Diferencia de PAS>0 y UFR>5ml/kg/h.
Consideramos que había HTAID si se cumplía el criterio en más del 50% de las 6 sesiones consecutivas (2 semanas) de seguimiento. Se recogieron antecedentes personales, medicamentos, características de diálisis y datos bioquímicos pre- y pos-HD. Se consideró función renal residual (FRR) una diuresis >250ml/24h. Se analizó a los 18 meses los posibles eventos del grupo.
ResultadosIncluimos 169 pacientes (68% varones), con una edad media de 67,9 (14,2) años y una mediana de tiempo en HD de 34,5 (AIC 17,5-67,5) meses. De ellos, 94 provienen de una unidad y 75 de la otra. La prevalencia de HTAID fue según Def 1 (8,3%), Def 2 (27,2%) y Def 3 (29,6%). Se evidencia una asociación en la Def 2 con antecedente de HTA previa, uso de inhibidores del sistema renina angiotensina (ISRA) y furosemida y en los pacientes con FRR, en la Def 3 solo asociación a coronariopatía. Existe asociación con las diferentes prescripciones de los líquidos de diálisis. No aumentaron las hormonas catecolaminérgicas y aldosterona en los pacientes con HTAID durante la sesión de HD. No presentaron mayor incidencia de eventos cardiovasculares o mortalidad a los 18 meses.
ConclusionesLa HTAID tiene una prevalencia distinta tanto según la definición utilizada como la unidad estudiada. El futuro plantea un importante reto: conocer cuál de las definiciones determina una mayor implicación clínica y el papel que tienen las diferencias encontradas en las distintas unidades de HD.
Intradialytic hypertension (IDH) is a poorly understood phenomenon with no consensus on its definition, etiology, or related factors, and there is limited evidence on its consequences.
ObjectiveTo determine the prevalence of IDH according to different definitions in hemodialysis (HD) units, with different clinical practices and assessment of possible events after 18 months have passed.
Materials and methodsA cross-sectional observational study was conducted in two HD units, including all prevalent patients from March 2021 to September 2022. We established three definitions of IDH: Def 1: Mean arterial pressure (MAP) difference pre- and pos-HD>15mmHg. Def 2: Systolic blood pressure (SBP) difference pre- and pos-HD>10mmHg. Def 3: SBP difference >0 and ultrafiltration rate (UFR)>5ml/kg/h.
IDH was considered present if the criterion was met in more than 50% of the six consecutive sessions (2 weeks) of follow-up. Personal history, medications, dialysis characteristics, and pre- and post-HD biochemical data were collected. Residual renal function (RRF) was considered as urine output >250ml/24h. At 18 months, the possible events of the group were analyzed.
ResultsWe included 169 patients (68% men) with a mean age of 67.9 (14.2) years and a median HD duration of 34.5 (IQR: 17.5-67.5) months. Of these, 94 come from one unit and 75 from the other. The prevalence of IDH was 8.3% according to Def 1, 27.2% according to Def 2, and 29.6% according to Def 3. Def 2 showed an association with a history of previous hypertension, use of renin-angiotensin system inhibitors (RASIs), and furosemide, as well as with patients with RRF. Def 3 showed an association only with coronary artery disease. There was an association with different prescriptions of dialysis fluids. Catecholaminergic hormones and aldosterone did not increase in patients with hypertension during the HD session. They did not present a higher incidence of cardiovascular events or mortality at 18 months.
ConclusionsIDH has different prevalence rates depending on the definition used and the studied center. The future poses an important challenge: to determine which definition correlates with higher morbidity and mortality and the role of differences found in different HD units.
La hipertensión arterial intradiálisis (HTAID) es el aumento de la presión arterial (PA) durante la sesión de hemodiálisis (HD), un fenómeno que muchos describen como paradójico, debido a que es un efecto contrario al que cabría esperar, sobre todo, en aquellos pacientes a los que se les realiza una depleción de volumen. Es un fenómeno poco estudiado en la mayor parte de aspectos y con pocos datos concluyentes1–3.
Para empezar, no existe una definición ampliamente aceptada de la HTAID. Estos son algunos de los criterios propuestos en diferentes estudios:
- -
Incremento de la presión arterial media (PAM)≥15mmHg durante la sesión de HD2 en 2/3 de las últimas 12 sesiones4.
- -
Incremento de la presión arterial sistólica (PAS)≥10mmHg durante la sesión de HD en 4/6 sesiones5,6.
- -
Incremento de la PA resistente a la ultrafiltración en más del 50% de las últimas 6 sesiones7 o durante 4 sesiones consecutivas3.
Tampoco se conoce su epidemiologia, ya que la prevalencia de la HTAID no ha sido sistemáticamente estudiada. Según distintas publicaciones la prevalencia se sitúa entre un 5 y un 15%5,8. Existen pocos datos sobre sus consecuencias; se describe un mayor riesgo de hospitalización o muerte a corto plazo (6 meses)9, un descenso de 2 años de supervivencia en aquellos pacientes con PA pre-diálisis <120mmHg5. Además, esta situación nos obliga en muchas ocasiones a interrumpir precozmente la sesión de HD, a administrar fármacos antihipertensivos, y a prolongar la estancia del paciente en la unidad de diálisis o en el hospital, con sus consecuencias inmediatas como infradiálisis, peor calidad de vida y mayor gasto sanitario.
Existen varias teorías para explicar la patogenia, con resultados contradictorios. Las hipótesis propuestas para explicar este fenómeno son las siguientes: 1) El exceso de volumen7, que también se describe en los pacientes con hipertensión arterial (HTA) pre-diálisis10; 2) La activación del sistema nervioso simpático (SNS)11,12; 3) La activación del sistema renina angiotensina aldosterona (SRAA)13; 4) La disfunción endotelial que conlleva una vasoconstricción3; 5) La ganancia neta de sodio durante la sesión de HD14–16; 6) La eliminación de los antihipertensivos durante la sesión9; 7) El uso de agentes estimulantes de la eritropoyetina17,18, y 8) La rigidez vascular19.
En cuanto al manejo no existen estrategias claras. Suele intentarse un control estricto del volumen intravascular20, bloqueo farmacológico del SNS o SRAA, modificaciones de la concentración de sodio (Na) del líquido de diálisis (LD), evitar hemoglobinas elevadas o fármacos hipotensores que se eliminen con HD21.
En resumen, en el momento actual no está claramente definido el concepto, desconocemos su fisiopatología, no se han establecido sus características epidemiológicas y no existe un manejo terapéutico concreto. Además, a pesar de saber que la HTA es un claro factor de riesgo cardiovascular, no existen estudios que analicen la relación entre HTAID y la morbimortalidad cardiovascular.
Con estas premisas, hemos querido estudiar cuál es la prevalencia de HTAID de acuerdo con las distintas definiciones y qué factores pueden estar asociados, tanto epidemiológicos, clínicos o de técnicas de HD, además de determinar sus consecuencias.
Material y métodosSe trata de un estudio observacional prospectivo multicéntrico realizado a los pacientes prevalentes en marzo del año 2021, con seguimiento hasta septiembre del año 2022, en 2 unidades de HD; Hospital Clínica Benidorm (HCB) y Hospital Universitario Infanta Leonor (HUIL). La realización del estudio fue aprobada por el Comité Ético de Investigación Clínica del HUIL (Código interno 003/21).
Se incluyeron en el estudio a todos los pacientes prevalentes (≥3 meses en HD) mayores de edad, que habían iniciado tratamiento renal sustitutivo mediante HD hospitalaria antes del 1 de marzo del año 2021, con un mínimo de 2 sesiones semanales y tras haber firmado el consentimiento informado.
Definición de HTAIDSe ha realizado la medición de la PA a través de los esfingomanómetros presentes en los monitores de HD, considerado como primera medición de PA la realizada después de la conexión y la última medición, la tomada antes de la desconexión. Consideramos que son 2 situaciones donde el paciente se encuentra en el mismo estado de actividad/reposo al iniciar y finalizar la sesión de HD.
Se ha definido su prevalencia según las distintas definiciones empleadas en los estudios previos, estableciendo el diagnóstico si se cumple el criterio en más del 50% de 6 sesiones consecutivas de seguimiento:
- -
Definición 1: Diferencia en la PAM≥15mmHg, entre la última y la primera medición2,4.
- -
Definición 2: Diferencia en la PAS≥10mmHg, entre la última y la primera medición5,6.
- -
Definición 3: Cualquier aumento de la PAS con ratio de ultrafiltración mayor a 5ml/kg/h (ratio mínima considerado como UF significativa), entre la última y la primera medición3,7.
Los datos que se han recogido a través del programa informático de los centros participantes (Nefrolink®) son los siguientes:
- -
Datos demográficos: edad, sexo, etiología enfermedad renal, HTA previa, otros factores de riesgo cardiovascular (tabaco, diabetes mellitus [DM], dislipemia [DLP], obesidad, actividad física), antecedentes de enfermedades cardiovasculares (enfermedad coronaria, enfermedad cerebrovascular, vasculopatía periférica) y tiempo en HD.
- -
Tratamiento antihipertensivo: calcio antagonistas, diuréticos del asa, inhibidores del sistema renina angiotensina (ISRA), antagonistas alfa adrenérgicos, β-bloqueantes.
- -
Datos bioquímicos del análisis mensual: sodio, potasio, calcio, bicarbonato, hormona paratiroidea (PTH), hematocrito y estudio de función renal residual (FRR), en todo paciente con volumen de diuresis >250ml/24h, mediante el cálculo de filtrado glomerular mediante el aclaramiento medio de creatinina y urea (AcCrU).
- -
Parámetros de HD habituales: modalidad de HD (convencional o hemodiafiltración online) y composición del líquido de diálisis (bicarbonato, sodio, calcio, potasio).
- -
Muestra de sangre de la línea arterial en el momento de la conexión y al finalizar la sesión, en los pacientes diagnosticados de HTAID (sin diferenciar entre Def 2 y Def 3): glucosa, sodio, potasio, cloro, bicarbonato, calcio y hormonas (epinefrina, norepinefrina, dopamina y aldosterona) mediante el sistema HPLC con detector electroquímico en plasma (Chromosystem®). No se ha realizado un ajuste de los valores teniendo en cuenta la ultrafiltración realizada.
- -
A los 18 meses categorizamos a los pacientes en 4 posibles eventos (fallecimiento, evento cardiovascular, salida de HD por cualquier otra causa o continúan en HD).
El análisis estadístico se ha realizado con el programa STATA® 17 (StataCorp LLC®).
Para las variables cuantitativa se ha utilizado como medida de tendencia central la media (x̄), y la desviación estándar (S) como medida de dispersión. Se presentan mediana (Md) y amplitud intercuartil (AIC) para datos fuertemente asimétricos. Para las variables cualitativas se presentan tablas de frecuencia. La distribución normal de las variables se ha averiguado a través de diagrama de caja y función de distribución acumulada.
El estudio de asociación simple se ha realizado utilizando las pruebas de la t de Student y la de Chi-cuadrado. El test exacto de Fisher y la prueba de rango de Wilcoxon se han utilizado como pruebas no paramétricas. La asociación simple entre variables cualitativas se ha realizado a través del cálculo de odds ratio.
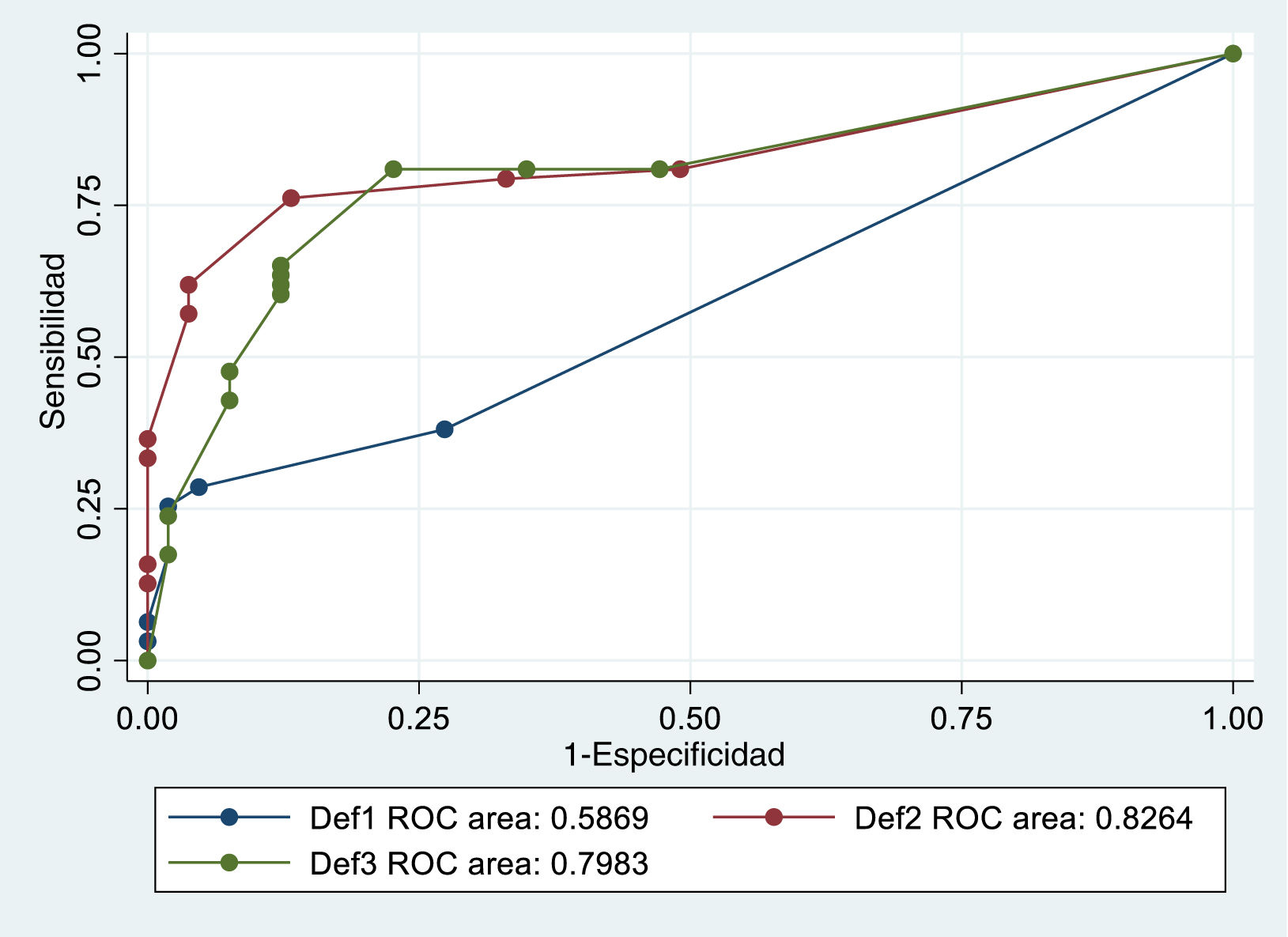
Para la valoración y comparación de la exactitud de las definiciones diagnósticas se ha utilizado el estudio de sensibilidad y especificidad y una curva ROC con patrón de referencia compuesto (composite reference standard). Para dicho patrón se ha definido como «hipertenso» al paciente que cumple al menos una de las 3 definiciones de HTAID, considerando el porcentaje de aciertos de cada definición a lo largo de 6 sesiones consecutivas de diálisis.
ResultadosSe han incluido 169 pacientes en HD (115 varones y 54 mujeres), con una edad media de 67,9 (14,2) años, con una mediana de tiempo en HD de 34,5 (AIC: 17,5-67,5) meses. Con relación a las unidades de HD, 94 pertenecen al HCB y 75 al HUIL, sin haber diferencia en la edad, ni en el tiempo de HD. Los monitores utilizados con el esfingomanómetro incorporado han sido en HCB Fresenius 5008 y 5008S, y en HUIL 66% Gambro AK200 y 33% Fresenius 5008. Sí existen diferencias significativas en la proporción de pacientes con nefropatía no filiada y congénita a favor del HUIL y de nefropatía vascular a favor del HCB (Anexo tabla 1). Con relación a los antecedentes y al tratamiento antihipertensivo, existe más proporción de DM, coronariopatía, tratamiento con ISRA y calcio antagonistas en HUIL (Anexo tabla 2). No hay diferencias en la proporción de pacientes con FRR, aunque el aclaramiento medio es mayor en HUIL (Anexo tabla 3). Sí existen diferencias significativas en la prescripción del líquido de diálisis, en HUIL las concentraciones de calcio y potasio son más altas, y las de bicarbonato y sodio son más bajas (Anexo tabla 4).
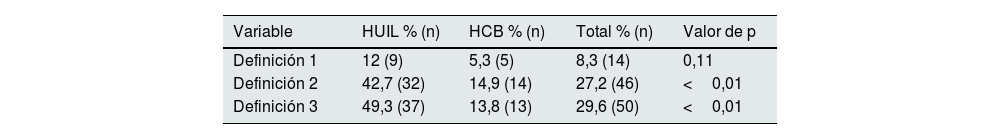
Los pacientes que hemos identificado presentaban HTAID según la definición 1 (Def 1) son 14 (8,3%), según la definición 2 (Def 2) son 46 (27,2%) y según la definición 3 (Def 3) son 50 (29,6%). En la tabla 1 se detallan los resultados diferenciando por centro, existiendo una diferencia significativa en la definición 2 y 3, con mayor frecuencia en HUIL.
Comparativa entre pacientes por centro según las diferentes definiciones de HTAID
| Variable | HUIL % (n) | HCB % (n) | Total % (n) | Valor de p |
|---|---|---|---|---|
| Definición 1 | 12 (9) | 5,3 (5) | 8,3 (14) | 0,11 |
| Definición 2 | 42,7 (32) | 14,9 (14) | 27,2 (46) | <0,01 |
| Definición 3 | 49,3 (37) | 13,8 (13) | 29,6 (50) | <0,01 |
HCB: Hospital Clínica Benidorm; HTAID: hipertensión arterial intradiálisis; HUIL: Hospital Universitario Infanta Leonor.
Las definiciones 1 y 2 se basan en un único criterio similar para establecer diagnóstico de HTAID, elevación de PAM y PAS, respectivamente, y observamos que todos los pacientes diagnosticados de HTAID según la definición 1 están incluidos en la definición 2, por lo que, para el análisis posterior, utilizaremos solo la definición 2, siendo el criterio que aporta más sensibilidad.
Valoración y comparación de la exactitud de las definicionesEl resultado del estudio de sensibilidad y especificidad evidencia que existe diferencia entre las definiciones (Def 1 AUC: 0,59; IC: 0,51-0,66; Def 2 AUC: 0,83; IC: 0,75-0,90; Def 3 AUC: 0,80: IC 0,72-0,87). Siendo la definición 2 la que mejor clasifica la hipertensión intradiálisis, aunque con una diferencia no significativa respecto a la definición 3 (p=0,61), y la definición 1 la peor (p<0,01) (fig. 1).
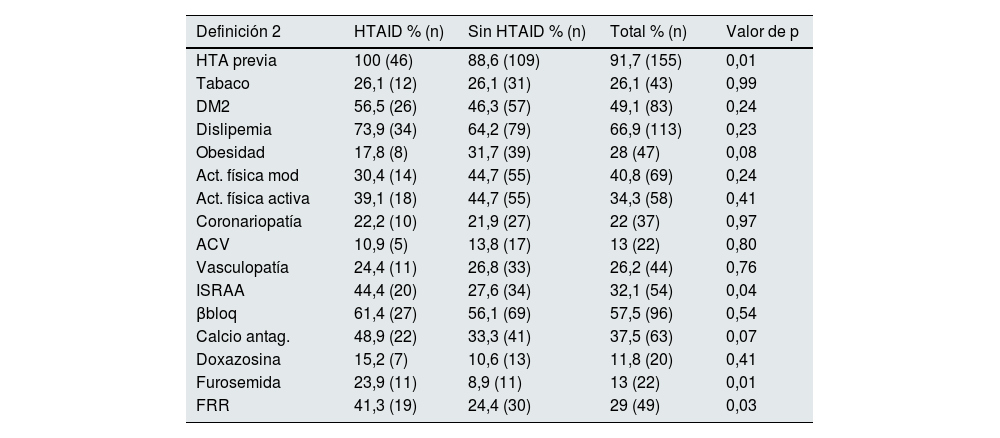
Comparación entre pacientes con o sin HTAID según la definición 2 y 3Los pacientes con antecedentes de HTA previa tuvieron más probabilidad de sufrir HTAID según Def 2 (p=0,01) y los pacientes con antecedentes de coronariopatía tuvieron más probabilidad de sufrir HTAID según Def 3 (p=0,015). No se encontraron diferencias en ninguno de los otros antecedentes recogidos.
Con relación a los medicamentos antihipertensivos, los pacientes con prescripción de ISRA y furosemida tuvieron más probabilidad sufrir HTAID acorde a la Def 2 (OR: 2,09; IC 95%: 1,03-4,25; p=0,039) y (OR: 3,2; IC 95%: 1,28-8,01; p=0,01), respectivamente, mientras que según la Def 3 fueron los que tomaban calcio antagonistas (OR: 2,22; IC 95%: 1,13-4,38; p=0,02). No existieron diferencias con otros fármacos.
Los pacientes con FRR presentaron con más frecuencia HTAID según Def 2 (OR: 2,18; IC 95%: 1,07-4,47; p=0,03). Las tablas 2 y 3 exponen todos los datos.
Comparación entre pacientes con y sin HTAID, definición 2 (n=46 [27,2%] y n=123 [72,8%]) según antecedentes, antihipertensivos y FRR
| Definición 2 | HTAID % (n) | Sin HTAID % (n) | Total % (n) | Valor de p |
|---|---|---|---|---|
| HTA previa | 100 (46) | 88,6 (109) | 91,7 (155) | 0,01 |
| Tabaco | 26,1 (12) | 26,1 (31) | 26,1 (43) | 0,99 |
| DM2 | 56,5 (26) | 46,3 (57) | 49,1 (83) | 0,24 |
| Dislipemia | 73,9 (34) | 64,2 (79) | 66,9 (113) | 0,23 |
| Obesidad | 17,8 (8) | 31,7 (39) | 28 (47) | 0,08 |
| Act. física mod | 30,4 (14) | 44,7 (55) | 40,8 (69) | 0,24 |
| Act. física activa | 39,1 (18) | 44,7 (55) | 34,3 (58) | 0,41 |
| Coronariopatía | 22,2 (10) | 21,9 (27) | 22 (37) | 0,97 |
| ACV | 10,9 (5) | 13,8 (17) | 13 (22) | 0,80 |
| Vasculopatía | 24,4 (11) | 26,8 (33) | 26,2 (44) | 0,76 |
| ISRAA | 44,4 (20) | 27,6 (34) | 32,1 (54) | 0,04 |
| βbloq | 61,4 (27) | 56,1 (69) | 57,5 (96) | 0,54 |
| Calcio antag. | 48,9 (22) | 33,3 (41) | 37,5 (63) | 0,07 |
| Doxazosina | 15,2 (7) | 10,6 (13) | 11,8 (20) | 0,41 |
| Furosemida | 23,9 (11) | 8,9 (11) | 13 (22) | 0,01 |
| FRR | 41,3 (19) | 24,4 (30) | 29 (49) | 0,03 |
Act.: actividad; ACV: accidente cerebro vascular; βbloq: betabloqueadores; Calcio antag.: calcio antagonistas; DM2: diabetes mellitus 2; FRR: función renal residual; HTA: hipertensión arterial; HTAID: hipertensión arterial intradiálisis; ISRAA: inhibidores del sistema renina angiotensina aldosterona.
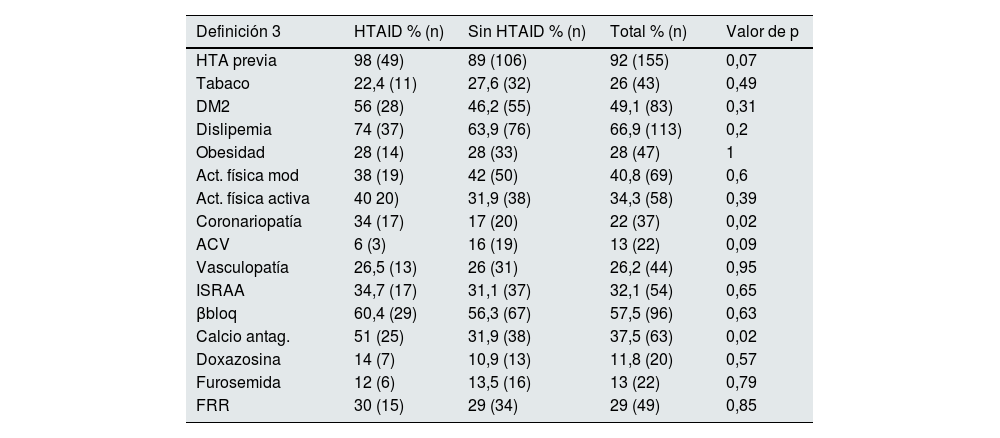
Comparación entre pacientes con y sin HTAID, definición 3 (n=50 [29,6%] y n=119 [70,4%]) según antecedentes, antihipertensivos y FRR
| Definición 3 | HTAID % (n) | Sin HTAID % (n) | Total % (n) | Valor de p |
|---|---|---|---|---|
| HTA previa | 98 (49) | 89 (106) | 92 (155) | 0,07 |
| Tabaco | 22,4 (11) | 27,6 (32) | 26 (43) | 0,49 |
| DM2 | 56 (28) | 46,2 (55) | 49,1 (83) | 0,31 |
| Dislipemia | 74 (37) | 63,9 (76) | 66,9 (113) | 0,2 |
| Obesidad | 28 (14) | 28 (33) | 28 (47) | 1 |
| Act. física mod | 38 (19) | 42 (50) | 40,8 (69) | 0,6 |
| Act. física activa | 40 20) | 31,9 (38) | 34,3 (58) | 0,39 |
| Coronariopatía | 34 (17) | 17 (20) | 22 (37) | 0,02 |
| ACV | 6 (3) | 16 (19) | 13 (22) | 0,09 |
| Vasculopatía | 26,5 (13) | 26 (31) | 26,2 (44) | 0,95 |
| ISRAA | 34,7 (17) | 31,1 (37) | 32,1 (54) | 0,65 |
| βbloq | 60,4 (29) | 56,3 (67) | 57,5 (96) | 0,63 |
| Calcio antag. | 51 (25) | 31,9 (38) | 37,5 (63) | 0,02 |
| Doxazosina | 14 (7) | 10,9 (13) | 11,8 (20) | 0,57 |
| Furosemida | 12 (6) | 13,5 (16) | 13 (22) | 0,79 |
| FRR | 30 (15) | 29 (34) | 29 (49) | 0,85 |
Act.: actividad; ACV: accidente cerebro vascular; βbloq: betabloqueadores; Calcio antag.: calcio antagonistas; DM2: diabetes mellitus 2; FRR: función renal residual; HTAID: hipertensión arterial intradiálisis; ISRAA: inhibidores del sistema renina angiotensina aldosterona.
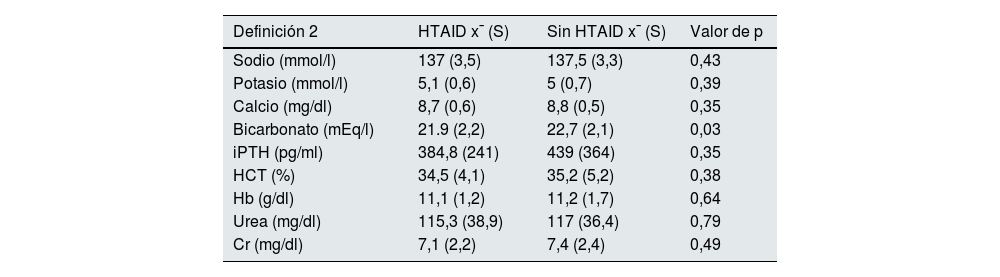
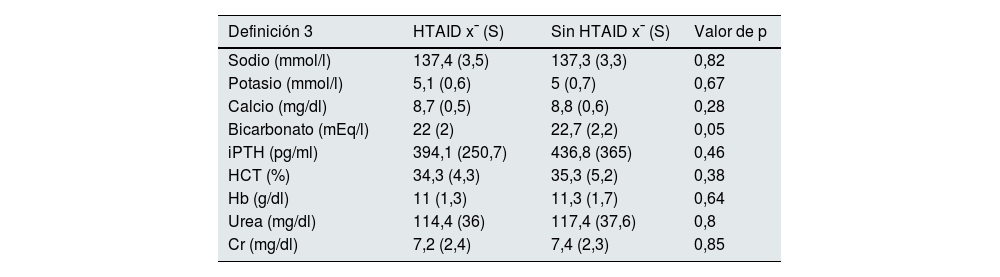
Se realiza una comparación de las medias de los datos bioquímicos mensuales de los pacientes con o sin HTAID según Def 2 y Def 3, detectando únicamente una asociación con concentraciones más bajas de bicarbonato en la HTAID según Def 2 (tablas 4 y 5).
Comparación entre pacientes con y sin HTAID, definición 2 (n=46 [27,2%] y n=123 [72,8%]) según datos bioquímicos mensuales
| Definición 2 | HTAID x¯ (S) | Sin HTAID x¯ (S) | Valor de p |
|---|---|---|---|
| Sodio (mmol/l) | 137 (3,5) | 137,5 (3,3) | 0,43 |
| Potasio (mmol/l) | 5,1 (0,6) | 5 (0,7) | 0,39 |
| Calcio (mg/dl) | 8,7 (0,6) | 8,8 (0,5) | 0,35 |
| Bicarbonato (mEq/l) | 21.9 (2,2) | 22,7 (2,1) | 0,03 |
| iPTH (pg/ml) | 384,8 (241) | 439 (364) | 0,35 |
| HCT (%) | 34,5 (4,1) | 35,2 (5,2) | 0,38 |
| Hb (g/dl) | 11,1 (1,2) | 11,2 (1,7) | 0,64 |
| Urea (mg/dl) | 115,3 (38,9) | 117 (36,4) | 0,79 |
| Cr (mg/dl) | 7,1 (2,2) | 7,4 (2,4) | 0,49 |
Cr: creatinina; Hb: hemoglobina; HCT: hematocrito; HTAID: hipertensión arterial intradiálisis; iPTH: hormona paratiroidea; S: desviación estándar; x̄: media.
Comparación entre pacientes con y sin HTAID, definición 3 (n=50 [29,6%] y n=119 [70,4%]) según datos bioquímicos mensuales
| Definición 3 | HTAID x¯ (S) | Sin HTAID x¯ (S) | Valor de p |
|---|---|---|---|
| Sodio (mmol/l) | 137,4 (3,5) | 137,3 (3,3) | 0,82 |
| Potasio (mmol/l) | 5,1 (0,6) | 5 (0,7) | 0,67 |
| Calcio (mg/dl) | 8,7 (0,5) | 8,8 (0,6) | 0,28 |
| Bicarbonato (mEq/l) | 22 (2) | 22,7 (2,2) | 0,05 |
| iPTH (pg/ml) | 394,1 (250,7) | 436,8 (365) | 0,46 |
| HCT (%) | 34,3 (4,3) | 35,3 (5,2) | 0,38 |
| Hb (g/dl) | 11 (1,3) | 11,3 (1,7) | 0,64 |
| Urea (mg/dl) | 114,4 (36) | 117,4 (37,6) | 0,8 |
| Cr (mg/dl) | 7,2 (2,4) | 7,4 (2,3) | 0,85 |
Cr: creatinina; Hb: hemoglobina; HCT: hematocrito; HTAID: hipertensión arterial intradiálisis; iPTH: hormona paratiroidea; S: desviación estándar; x¯: media.
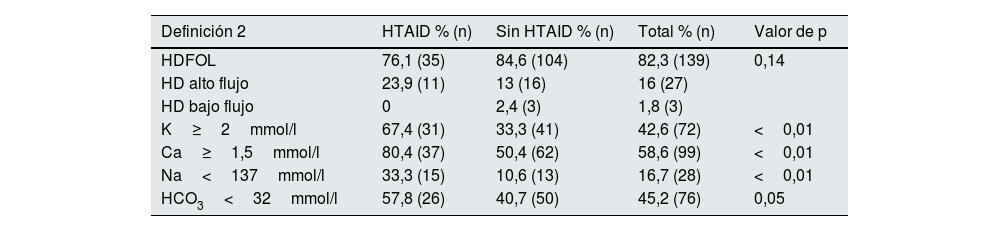
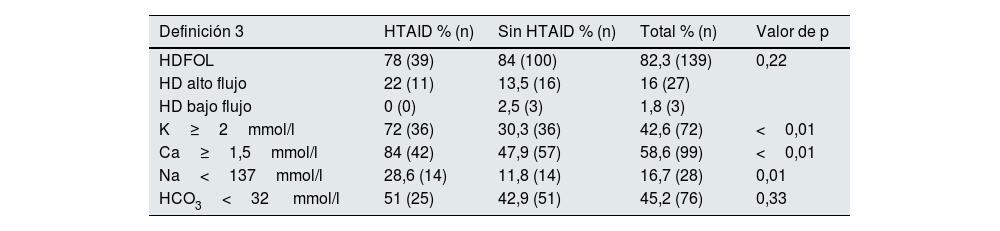
Cuando comparamos los parámetros de HD en la HTAID según Def 2 vemos que se dializan, con mayor frecuencia, con LD con sodio ≤137mmol/l, potasio ≥2mmol/l, calcio ≥1,5mmol/l y bicarbonato ≤32mmol/l (tabla 6). Los resultados comparando según Def 3 fueron similares, excepto que, no se encontraron diferencias en la prescripción del LD de bicarbonato (tabla 7).
Comparación entre pacientes con y sin HTAID, definición 2 (n=46 [27,2%] y n=123 [72,8%]) según parámetros de hemodiálisis
| Definición 2 | HTAID % (n) | Sin HTAID % (n) | Total % (n) | Valor de p |
|---|---|---|---|---|
| HDFOL | 76,1 (35) | 84,6 (104) | 82,3 (139) | 0,14 |
| HD alto flujo | 23,9 (11) | 13 (16) | 16 (27) | |
| HD bajo flujo | 0 | 2,4 (3) | 1,8 (3) | |
| K≥2mmol/l | 67,4 (31) | 33,3 (41) | 42,6 (72) | <0,01 |
| Ca≥1,5mmol/l | 80,4 (37) | 50,4 (62) | 58,6 (99) | <0,01 |
| Na<137mmol/l | 33,3 (15) | 10,6 (13) | 16,7 (28) | <0,01 |
| HCO3<32mmol/l | 57,8 (26) | 40,7 (50) | 45,2 (76) | 0,05 |
Ca: calcio; HCO3: bicarbonato; HD: hemodiálisis; HDFOL: hemodiafiltración online; HTAID: hipertensión arterial intradiálisis; K: potasio (mmol/L); Na: sodio.
Comparación entre pacientes con y sin HTAID, definición 3 (n=50 [29,6%] y n=119 [70,4%]) según parámetros de hemodiálisis
| Definición 3 | HTAID % (n) | Sin HTAID % (n) | Total % (n) | Valor de p |
|---|---|---|---|---|
| HDFOL | 78 (39) | 84 (100) | 82,3 (139) | 0,22 |
| HD alto flujo | 22 (11) | 13,5 (16) | 16 (27) | |
| HD bajo flujo | 0 (0) | 2,5 (3) | 1,8 (3) | |
| K≥2mmol/l | 72 (36) | 30,3 (36) | 42,6 (72) | <0,01 |
| Ca≥1,5mmol/l | 84 (42) | 47,9 (57) | 58,6 (99) | <0,01 |
| Na<137mmol/l | 28,6 (14) | 11,8 (14) | 16,7 (28) | 0,01 |
| HCO3<32 mmol/l | 51 (25) | 42,9 (51) | 45,2 (76) | 0,33 |
Ca: calcio; HCO3: bicarbonato; HD: hemodiálisis; HDFOL: hemodiafiltración online; HTAID: hipertensión arterial intradiálisis; K: potasio (mmol/L); Na: sodio.
En todos los pacientes diagnosticados de HTAID encontramos los cambios bioquímicos esperados en todo paciente que realiza sesión de HD: disminución pos-HD del potasio, glucosa y aumento de bicarbonato, pH, calcio y hematocrito, sin modificaciones en sodio.
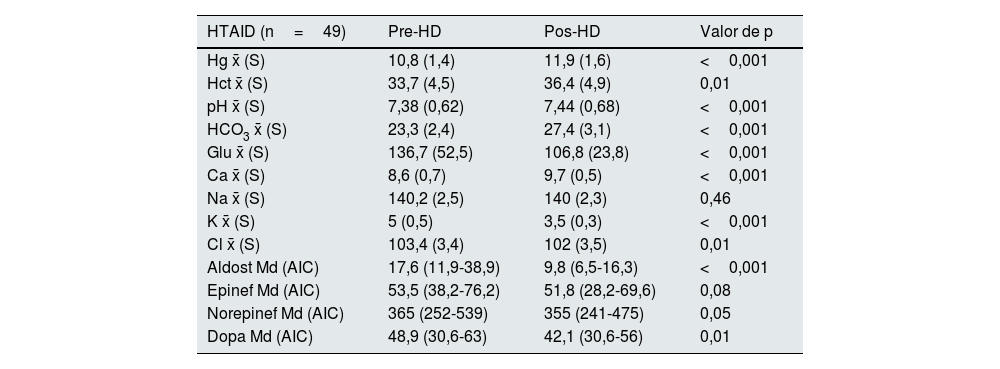
También valoramos si existe algún aumento de las hormonas relacionadas con cambios en la PA (dopamina, epinefrina, norepinefrina y aldosterona) y observamos reducción de todas ellas, siendo estadísticamente significativa, la aldosterona y dopamina (tabla 8).
Comparación bioquímica y hormonal pre y posdiálisis en los pacientes con HTAID
| HTAID (n=49) | Pre-HD | Pos-HD | Valor de p |
|---|---|---|---|
| Hg x̄ (S) | 10,8 (1,4) | 11,9 (1,6) | <0,001 |
| Hct x̄ (S) | 33,7 (4,5) | 36,4 (4,9) | 0,01 |
| pH x̄ (S) | 7,38 (0,62) | 7,44 (0,68) | <0,001 |
| HCO3 x̄ (S) | 23,3 (2,4) | 27,4 (3,1) | <0,001 |
| Glu x̄ (S) | 136,7 (52,5) | 106,8 (23,8) | <0,001 |
| Ca x̄ (S) | 8,6 (0,7) | 9,7 (0,5) | <0,001 |
| Na x̄ (S) | 140,2 (2,5) | 140 (2,3) | 0,46 |
| K x̄ (S) | 5 (0,5) | 3,5 (0,3) | <0,001 |
| Cl x̄ (S) | 103,4 (3,4) | 102 (3,5) | 0,01 |
| Aldost Md (AIC) | 17,6 (11,9-38,9) | 9,8 (6,5-16,3) | <0,001 |
| Epinef Md (AIC) | 53,5 (38,2-76,2) | 51,8 (28,2-69,6) | 0,08 |
| Norepinef Md (AIC) | 365 (252-539) | 355 (241-475) | 0,05 |
| Dopa Md (AIC) | 48,9 (30,6-63) | 42,1 (30,6-56) | 0,01 |
AIC: amplitud intercuartil; Aldost: aldosterona (ng/dl); Ca: calcio (mg/dl); Cl: cloro (mmol/l); Dopa: dopamina (pg/ml); Epinef: epinefrina (pg/ml); Glu: glucosa (mg/dl); Hb: hemoglobina (g/dl); HCO3: bicarbonato (mmol/l); Hct: hematocrito (%); HTAID: hipertensión arterial intradiálisis; K: potasio (mmol/l); Md: mediana; Na: sodio (mmol/l); Norepinef: norepinefrina (pg/ml); S: desviación estándar; x¯: media.
A los 18 meses, los pacientes que sufrieron un evento cardiovascular fueron 20 (11,8%), fallecieron 24 (14,2%), salieron de HD por otras causas 13 (7,7%) y continúa en HD 112 (66,3%). No detectamos ninguna diferencia significativa entre los que presentaban HTAID (acorde a Def 2 o Def 3) y los que no, en ninguno de los eventos estudiados (anexo tabla 5 y 6).
DiscusiónEl objetivo del estudio ha sido conocer un fenómeno controvertido y poco estudiado, como es el aumento de la PA durante la sesión de HD en nuestras unidades. Encontramos una gran diferencia en la prevalencia según el centro y en las diferentes definiciones, sin que hayamos podido detectar un perfil de paciente más claramente susceptible acorde a sus antecedentes, fármacos, pruebas bioquímicas ni un cambio hormonal que justifique la elevación de la PA. Tampoco en nuestra población con HTAID, en la revisión a los 18 meses, se ha detectado un aumento de la mortalidad o mayor incidencia de eventos cardiovasculares.
Una de las dificultades encontradas, como expone Chazot y Jean20, es la falta de una definición uniforme. Existen varias definiciones, teniendo en cuenta el aumento de la PAM mayor o igual a 15mmHg2,4, PAS mayor de 105,6 o cualquier aumento de PA con ultrafiltración3,7. Nosotros hemos aplicado las 3 definiciones para saber si existe alguna diferencia entre ellas, con relación a las variables estudiadas, a nivel pronóstico y sí podemos considerar una de ellas como prueba más válida. En la definición 3 establecemos un mínimo de ratio de ultrafiltración, de forma arbitraria, en 5ml/kg/h para considerar una ultrafiltración significativa.
La prevalencia según Def 1 es del 8,3%, similar a otras publicaciones que utilizan el mismo criterio2,4, sin embargo, cuando se utiliza Def 2 la prevalencia aumenta mucho (27,2%), superior a otras publicaciones que la sitúan entre 5-15%5,6,8. Nos llama la atención la diferencia encontrada entre los 2 centros, en HUIL es del 42,7% y en HCB del 14,9%. Se comporta de la misma manera la Def 3, tiene una prevalencia total del 29,59% y presenta una diferencia significativa entre centros (HUIL es del 49,3% y HCB es del 13,8%). Una explicación podría ser que la mayoría de los dispositivos de medición de la PA conectados a los monitores de HD disponibles no han sido validados clínicamente y presentan variaciones entre ellos27, la existencia de diferentes monitores entre las 2 unidades y el uso de diferentes protocolos de intervención intradialítica, como la infusión de líquido de HD ultrapuro, el uso de suero salino fisiológico, la modificación del ratio de ultrafiltración o la modificación de posición del paciente, podría influir en la diferencia de prevalencias26. La ausencia de información acerca de lo que ocurrió entre la medición de la PA previa a la HD y la posterior a la HD podría constituir un factor de confusión relevante en los resultados. Debido a que la hipótesis inicial del estudio no era analizar las diferencias entre centros no podemos establecer un motivo de por qué se producen estas diferencias, pero este resultado subraya dos aspectos: las enormes diferencias en la frecuencia, que ya se ve en la literatura y la necesidad de encontrar una definición única que clarifique que es HTAID.
Singh et al. realizaron un estudio observacional, con una muestra muy importante de pacientes en HD (n=3.198), investigaron la asociación entre diferentes definiciones de hipertensión intradialítica y la mortalidad a largo plazo. Usan 3 definiciones de hipertensión intradialítica: cualquier aumento en la PAS desde antes hasta después de la HD (Hyper0), cualquier aumento de >10mmHg (Hyper10) y cualquier aumento de >20mmHg (Hyper20) en ≥30% de las sesiones de HD durante un periodo seguimiento de 90 días. Durante el período de referencia, los porcentajes de pacientes que cumplían con las tres definiciones fueron del 47, 21,2 y 6,8%, respectivamente. Confirman que la definición Hyper0 se asoció significativamente con un mayor riesgo de muerte (HR: 1,32; IC del 95%: 1,05-1,66)25. Sus resultados sugieren que la HTAID debería definirse como cualquier aumento en la presión arterial al finalizar una sesión de diálisis, siempre que el fenómeno no sea esporádico y ocurra en más del 30% de las sesiones de hemodiálisis. Esta es una definición sencilla que se puede integrar fácilmente en la práctica clínica1, sin embargo, consideramos que puede tratarse de una definición con muy baja especificidad debido a que la medida de la presión arterial en las unidades de HD no es precisa, principalmente debido a que los esfigmómetros que disponen los monitores no están validados y los pacientes suelen variar de posición y modificar el ajuste de los manguitos durante la sesión27.
Nosotros hemos intentando averiguar cuál es la definición que consigue un mejor equilibrio entre la capacidad para detectar verdaderos positivos y evitar falsos positivos ya que no existir una definición gold standard para la HTA intradiálisis. Por ello, hemos realizado un análisis de sensibilidad y especificidad con curvas ROC. El resultado evidencia que existe diferencia entre las definiciones, siendo la definición 2 la que mejor clasifica la hipertensión intradiálisis, aunque con una diferencia no significativa respecto a la definición 3.
El hecho de encontrar que los pacientes con HTAID son más frecuentemente hipertensos puede hacer pensar que existe un factor predisponente, aunque cuando se usa la Def 3 la diferencia no es estadísticamente significativa, pero existe una clara tendencia. Estos resultados coinciden con los presentados por van Buren et al.6, por lo tanto, se asume que los pacientes que sufren HTAID son pacientes con HTA interdialítica. La asociación encontrada entre antecedentes de coronariopatía y la Def 3 precisaría un estudio más concreto de este grupo con ecocardiografía y valores de cambio para poder identificarlos más concretamente.
La sensación clínica de que aquellos que tienen FRR presentan más frecuentemente HTAID se confirma en nuestros resultados. Si el mecanismo es porque están más hipervolémicos debido a una reducción en la tasa de ultrafiltración o tienen mecanismos fisiopatológicos nefro-vasculares más intactos que pueden perderse con el deterioro de la función renal son explicaciones especulativas. Gunal et al. explican que el mecanismo de la HTAID es el aumento de gasto cardiaco al reducir parte de la congestión vascular, pero sin conseguir el peso seco ideal, es decir, manteniendo un estado congestivo menor aumenta el gasto cardiaco3, y quizás, en nuestras unidades seamos excesivamente cautelosos al realizar la ultrafiltración en pacientes con FRR, con el objetivo de prevenir posibles daños de hipoperfusión renal y ello explica dicha asociación. En cuanto a los fármacos que reciban más ISRA o calcio antagonistas y furosemida posiblemente va asociado a sus antecedentes de HTA y de conservar la FRR más que llevar a pensar que puedan ser causantes.
No esperábamos encontrar ninguna diferencia en los valores analíticos pre-diálisis entre los pacientes con HTAID y el resto de pacientes, y curiosamente se detecta una diferencia significativa en la Def 2 y tendencia en la Def 3 sobre los niveles de bicarbonato, pero la diferencia encontrada no tiene relevancia clínica. El resto de valores (sodio, potasio, calcio, PTH, hematocrito) no presentan diferencia como esperábamos.
Al estudiar la composición del LD, hay que tener en cuenta que estamos haciendo un análisis descriptivo y que, en muchos de estos pacientes, podrían haberse tomado medidas encaminadas a evitar la HTAID, por ese motivo, las concentraciones de sodio más bajo en LD podría ser una medida terapéutica sin que podamos determinar si es o no una medida efectiva para este fin, ya que no era el objetivo de nuestro trabajo. La pauta de líquido de HD con concentraciones de calcio superior a 1,25mEq/l también se ha asociado a la HTAID en ambas definiciones. Aquí sí podría existir una asociación causa/efecto ya que el aumento de la concentración de calcio en sangre favorece la contractilidad cardiaca, por lo que, mejora el gasto cardiaco, y aumenta de la vasoconstricción22,23 pudiendo aumentar la PA.
A pesar de existir varios estudios que relacionan la HTAID con el aumento de la actividad del SNS24, nosotros no detectamos un aumento de los neurotransmisores estudiados (epinefrina, norepinefrina, dopamina y aldosterona) en ninguna de las definiciones, igual que en el estudio de Chou et al.4. Aunque no hemos realizado un ajuste por la ultrafiltración. Estos resultados no van a favor de la teoría tradicional del aumento de la PA por estímulo del SRA o SNS, aunque nuestra muestra es pequeña13.
Con relación a los eventos valorados a los 18 meses, nosotros no hemos detectado ninguna asociación, en cualquiera de las definiciones, tanto en evento cardiovascular como en mortalidad. Existen varios estudios que relacionan la HTAID con la mortalidad; uno de ellos, resulta muy interesante ya que comenta un aumento de la mortalidad en los pacientes que sufren HTAID si la PA pre-diálisis es <120mmHg, ellos definen la HTAID como un incremento de la PAS>10mmHg5, es decir, delimita el grupo de pacientes con HTAID a los que tenemos que prestar más atención, nosotros no hemos categorizado a los pacientes por las cifras de PA inicial, pero entendemos que sus resultados son como los nuestros si consideran a todos los pacientes con HTAID. Un segundo estudio, ya comentado, que investiga la asociación entre diferentes aumentos de PAS (Hyper0 cualquier aumento, Hyper10 un aumento de 10mmHg e Hyper20 un aumento de 20mmHg) y la mortalidad a largo plazo25. Sorprende la asociación inversa que existe con el riesgo de muerte (en el grupo Hyper20, la tasa de riesgo de muerte fue menor que en el grupo Hyper0). Existe otro estudio donde sí que se aprecia un aumento de mortalidad conforme se incrementan las diferencias de PA, pero no realiza una evaluación de cada sesión de hemodiálisis, sino que realiza un promedio de todas las presiones arteriales pre-HD y pos-HD, por lo que, la diferencia de definición es tan grande que no podemos establecer una comparación con nuestro trabajo. Es necesario realizar más estudios o continuar el seguimiento de estos pacientes para aclarar si existe un peor pronóstico en estos pacientes.
Sobre las limitaciones que presenta nuestro trabajo, en primer lugar, hay que recordar que es un trabajo descriptivo en el que estudiamos asociaciones que no identifican causalidad. En segundo lugar, considerar que la PA registrada entre las 2 unidades se realiza con esfingomanómetros diferentes y no tenemos un registro de lo sucedido durante la sesión en caso de que se hayan realizado intervenciones que puedan modificar el resultado final. En tercer lugar, no incluimos el fósforo sérico en el estudio, a pesar de tratarse de un factor pronóstico en los pacientes de HD y no hemos podido comparar los cambios hormonales y bioquímicos que se producen pre- y pos-HD entre los pacientes con HTAID versus los pacientes sin HTAID. Por último, no se realiza un seguimiento de los pacientes, por lo que, no se puede hacer un estudio de supervivencia que aportaría más información sobre el pronóstico de estos pacientes. Sería necesario incluir a más centros de HD para poder aumentar el tamaño de la muestra y conocer mejor las diferencias poblacionales.
ConclusiónNuestro estudio pone de manifiesto la alta prevalencia de HTAID en las unidades de hemodiálisis, lo que indica su difícil control. Sin embargo, aún no se ha aclarado completamente su impacto y relevancia clínica. Consideramos que es crucial establecer una definición única de HTAID, basada en los posibles riesgos que presenta para el paciente. Esto nos permitirá una mejor delimitación de las poblaciones afectadas, una mayor comprensión de su fisiopatología y la identificación de las medidas de tratamiento más efectivas. Entre las definiciones consideradas, la más específica y sensible es la definición 2, aunque aún se requieren estudios adicionales para resolver definitivamente estos interrogantes.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A Marta por su generosidad a la hora de enseñarme y apoyarme en todo momento, y a Maite y Fabio porque sin ellos no podría haber llevado a cabo el trabajo.