El micofenolato de mofetilo se ha usado ampliamente como tratamiento de la nefritis lúpica. Varios ensayos clínicos y metaanálisis han demostrado que el micofenolato de mofetilo es un fármaco eficaz y seguro en el tratamiento de la nefritis lúpica grave (formas proliferativas y algunas membranosas) con función renal conservada, en varios entornos geográficos y en diferentes grupos étnicos (raza negra e hispanos), tanto en la fase de inducción como de mantenimiento. En general, el micofenolato de mofetilo es superior o al menos no inferior a la ciclofosfamida, aunque se necesita más tiempo para conocer el impacto del micofenolato de mofetilo sobre la supervivencia renal y la mortalidad. El micofenolato de mofetilo es el tratamiento de elección en los pacientes con riesgo de infección o malignidad, preferencia de administración oral y deseos de preservar la función ovárica. Las dosis superiores a 2 g/día no son recomendables y el papel de la monitorización con niveles no se conoce con detalle. Los efectos secundarios más importantes son intestinales y generalmente leves. La combinación de micofenolato de mofetilo con nuevos inmunosupresores posiblemente aumente su eficacia en el futuro. La incorporación del micofenolato de mofetilo como fármaco de primera línea de tratamiento de la nefritis lúpica ha supuesto un notable avance en su tratamiento.
La nefritis lúpica (NL) es una enfermedad frecuente en las unidades de nefrología. De hecho, según los datos del Registro Español de Glomerulonefritis (que recoge más de 15.000 biopsias desde 1994), supone el 9,4% del total de las biopsias renales, es la causa más frecuente de enfermedad renal secundaria biopsiada (43%) y cada año se comunican unos 100 casos1. Si a ello añadimos que la edad en el momento de la biopsia renal es de 32 años, el interés es aún mayor. La NL afecta a más del 60% de los pacientes con lupus sistémico a lo largo de su evolución y aumenta el riesgo de enfermedad renal crónica y de fallecimiento. Las formas más graves son las proliferativas (clases tipos III y IV) y algunas membranosas (clase V). A pesar de que su patogenia continúa siendo misteriosa en gran medida, se han hecho notables avances en la clasificación histológica, las correlaciones clínico-morfológicas (RNP/IS de 2003), los índices de supervivencia, que actualmente son superiores al 80% a los 10 años del diagnóstico y, sobre todo, en el tratamiento.
El tratamiento de la NL se basa en el uso de inmunosupresores y tiene dos fases: a) período de tratamiento intensivo para inducir la remisión, que no debe superar los 6 meses, y b) período de mantenimiento, más ligero, cuya duración suele durar años. Los objetivos del tratamiento son inducir y mantener emisiones parciales o completas, evitar las recaídas y reducir la evolución hacia la insuficiencia renal crónica y la tasa de fallecimientos. Si tenemos en cuenta que no hay tratamiento curativo y que ningún fármaco logra conseguir estos objetivos, el tema no ha perdido vigencia. En términos generales, el tratamiento de la NL tiene tres etapas. La primera de ellas se inició en Estados Unidos en los años ochenta, cuando los ensayos promovidos por los investigadores del National Institute of Health demostraron la eficacia de la asociación de esteroides y ciclofosfamida i.v. (CFiv) (0,5-1 g/m2) tanto en la fase de inducción como en la de mantenimiento; no obstante, no lograron reducir la tasa de mortalidad pese a la disminución del riesgo para duplicar la creatinina basal. Aun así, no había otras alternativas y se convirtió en el tratamiento estándar durante más de 20 años2,3. La segunda etapa viene dada cuando los investigadores de Euro-Lupus confirmaron, en un ensayo clínico controlado realizado en 90 pacientes europeos, que la administración de menos dosis de CFiv durante menos tiempo (6 pulsos i.v. de 500 mg, con dosis total acumulada de 3 g), seguida de azatioprina como tratamiento de mantenimiento, conseguía similares resultados a la pauta americana, con menos efectos secundarios4. No obstante, en ambos esquemas aparecen resultados decepcionantes: alrededor de un 16-20% de los casos no responden y hasta un 28-46% presentan recaídas en los 5 años siguientes al diagnóstico. Si a ello añadimos los efectos secundarios de la CF entre los que se encuentran la predisposición a las infecciones y a los tumores (sobre todo de vejiga), cistitis hemorrágica, leucemia, depresión medular y, especialmente, fallo ovárico precoz, se entiende que se hayan buscado otros fármacos alternativos con menos efectos secundarios5. Ente ellos se encuentra el micofenolato mofetil (MMF), que inaugura la tercera etapa y del que nos ocuparemos con más detalle.
MECANISMO DE ACCIÓN Y ANTECEDENTES
El MMF es un profármaco con excelente biodisponibilidad oral. En el hígado es hidrolizado a ácido micofénolico, producto activo que también se obtiene de la fermentación del Penicillium stoloniferum. El ácido micofenólico inhibe la enzima inosina 5-monofosfato deshidrogenasa que forma parte de la síntesis de novo de nucleótidos de guanosina. Los linfocitos T y B dependen en exclusiva de esta enzima para su proliferación dado que no tienen otras vías alternativas, como ocurre en otras células. Por tanto, disminuye la síntesis de anticuerpos y la aparición de células T citotóxicas. Además tiene propiedades antifibróticas, reduce la síntesis de moléculas de adhesión y disminuye la expresión de la sintetasa del óxido nítrico en la corteza renal.
Las dosis oscilan entre 500 y 3.000 mg/día, pero dosis superiores a 2.000 mg/día se asocian con más efectos secundarios. El papel de los niveles séricos de ácido micofenólico está por determinar, pero las concentraciones comprendidas entre 3,5 y 4,5 mg/l pueden ser adecuadas6. No se debe utilizar durante la gestación y su toxicidad aumenta si el filtrado glomerular está reducido. Los efectos secundarios son fundamentalmente de tipo digestivo (náuseas, diarrea) que se pueden reducir con espaciamiento de las dosis e inicio de forma progresiva.
El micofenolato sódico con cubierta entérica mejora la sintomatología intestinal7 (250 mg de MMF equivalen a 180 mg de micofenolato sódico). También predispone a las infecciones, leucopenia y anemia, pero con menos frecuencia que otros inmunosupresores. Recientemente se han comunicado casos de leucoencefalopatía multifocal progresiva.
Desde 1995 el MMF se viene utilizando con notable éxito en la prevención del trasplante renal, cardíaco y hepático. Por otro lado, se ha demostrado su eficacia en modelos experimentales de NL. Con estos antecedentes, al igual que ha ocurrido con otros inmunosupresores, el MMF se ha incorporado al grupo de fármacos potencialmente útiles en el tratamiento de la NL grave, especialmente las de tipo III (focal) y IV (difusa) y en menor proporción las de tipo V (membranosa).
A finales de los noventa se empezaron a publicar series de casos con buenos resultados, tanto en la fase de inducción como de mantenimiento. En los últimos 10 años se han publicado 11 ensayos clínicos de calidad8-18, de tal manera que la NL es la enfermedad glomerular que cuenta con el mayor número de ensayos controlados y donde se puede obtener un buen nivel de evidencia, especialmente en el uso de MMF.
Así, se han incluido más de 800 pacientes con este fármaco hasta la fecha. En la tabla 1 se resumen sus resultados, que detallaremos a continuación y que también se han revisado en publicaciones recientes19,20.
MICOFENOLATO DE MOFETILO COMO TRATAMIENTO DE INDUCCIÓN
En el año 2000, Chan et al.8 publicaron un ensayo clínico controlado en 42 pacientes de Hong-Kong en el que comparaban la eficacia de MMF (2 g/día durante 6 meses, seguidos de 1 g/día durante 6 meses) y esteroides frente a CF oral (2,5 mg/día) y esteroides durante 6 meses seguidos de azatioprina (1,5 mg/día): no encontraron diferencias significativas en el porcentaje de pacientes con remisión completa o parcial o recidivas al año, con una incidencia similar de efectos secundarios. Dos años más tarde, dos grupos también chinos9,10 comunicaron que la inducción con MMF comparada con CF se asociaba con una mayor disminución de la proteinuria, mejoría del sedimento urinario y disminución de los parámetros de actividad inmunológica, datos similares a los encontrados posteriormente en un grupo mexicano11.
En el año 2005, Ginzler et al.14 confirmaron en un nuevo ensayo, realizado en Estados Unidos con un número considerable de pacientes (140, la mitad afroamericanos), que la inducción con MMF es superior a la CFiv, con menos fracasos de tratamiento, mayor número de casos que alcanzan remisiones completas y parciales, así como menor incidencia de efectos adversos. Asimismo, el ensayo de Ong et al.15 encuentra que el MMF combinado con esteroides es un tratamiento eficaz en la inducción de la NL, similar a la conseguida con CFiv; por otro lado, el estudio de Wang et al.16 confirma que el MMF es superior a la CF en los casos con vasculopatía necrosante, con mayor reducción de la proteinuria y mayor porcentaje de pacientes que entran en remisión completa. A pesar de la disparidad de razas, grupos étnicos, dosis y diseños no del todo similares, se podía concluir que el MMF era un fármaco de primera línea en la fase de inducción, con una cierta superioridad a la CF en términos de eficacia y seguridad, al menos en pacientes con función renal preservada. No obstante, por las limitaciones de los ensayos anteriores se hacía necesario un estudio más ambicioso para confirmar estos resultados tan prometedores. Así, el grupo Aspreva diseñó el ensayo ALMS (Aspreva Lupus Maintenance Study) que se realizó en 370 pacientes (aproximadamente el mismo número que la suma de todos los pacientes anteriormente incluidos en ensayos clínicos) procedentes de 80 hospitales de Asia, Estados Unidos, Canadá, Sudamérica y Europa (cuatro de ellos españoles)18. El tratamiento de inducción consistía en MMF a dosis progresivas hasta 3 g/día combinado con esteroides durante 6 meses frente a CFiv a dosis de 0,5-1 g/m2 y esteroides. Los resultados, a primera vista, suponen una cierta decepción, pues no se logró alcanzar el objetivo principal que consistía en demostrar la superioridad de MMF frente a CFiv. Así, el porcentaje de pacientes que respondía fue similar en ambos grupos (56% en MMF y 53% en CFiv) con tasas de infecciones similares (69% MMF y 62% CFiv), así como de efectos secundarios y de fallecimientos. No obstante, en un análisis más detallado, los autores comprobaron que el MMF es más eficaz en pacientes de raza negra y en hispanos, de forma similar a lo encontrado anteriormente por Ginzler et al.14. Este trabajo, por la ambición de sus objetivos y los resultados menos brillantes de lo que se esperaba, ha suscitado múltiples comentarios y reflexiones. Una lectura detallada del trabajo puede no ser tan pesimista, puesto que se puede deducir que el MMF es al menos similar a la CF en la fase de inducción y que presenta un excelente perfil de seguridad en mujeres, que son el 80% del total de casos, con deseos de preservar la fertilidad, así como en determinados grupos étnicos. Las dosis tan elevadas de MMF y la inclusión de pacientes con un importante deterioro renal, pueden, en parte, explicar los resultados menos brillantes del ensayo y no reducen la importancia del MMF en el tratamiento de la NL.
MICOFENOLATO DE MOFETILO COMO TRATAMIENTO DE MANTENIMIENTO
Lógicamente, hay menos datos acerca de la eficacia de MMF en la fase de mantenimiento, dado que la evolución hacia la insuficiencia renal es lenta. El grupo de Chan et al.8,13 demostró que los pacientes tratados con MMF tienen índices similares a los tratados con CF acerca del desarrollo de insuficiencia renal crónica, aparición de recidivas y mortalidad a los 5 años de seguimiento, con menos efectos secundarios. En 2004, Contreras et al.12 realizaron un ambicioso estudio en 59 pacientes con NL clase III o IV en Estados Unidos, la mayoría afroamericanos e hispanos; tras la inducción con CFiv (7 meses), el período de mantenimiento se dividió en tres grupos: CFiv trimestral, azatioprina o MMF: tanto la azatioprina como el MMF tienen menos fallecimientos o desarrollo de insuficiencia renal crónica, pero con mayor número de efectos secundarios en el grupo de CFiv. Estos resultados fueron confirmados posteriormente por Sahin et al.17, quienes concluyen que tanto la azatioprina como el MMF, asociados a esteroides, son igual de eficaces para consolidar la fase de mantenimiento.
Con estos datos se puede concluir que el MMF y la azatioprina son excelentes fármacos en la fase de mantenimiento, quizá con mejor perfil de seguridad en el caso de MMF. No obstante, debemos esperar los resultados a largo plazo del estudio ALMS18 y también los del ensayo MAINTAIN (actualmente en fase de mantenimiento) para asegurar esta superioridad21.
En nuestro país hay cierta experiencia que demuestra, en estudios no controlados, la eficacia y seguridad de MMF en las formas refractarias o recidivantes22,23, resultados que se están intentando confirmar en un estudio multicéntrico24.
METAANÁLISIS
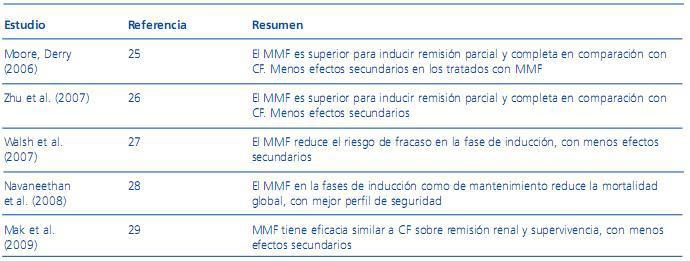
Como consecuencia de las limitaciones de los ensayos clínicos comentados, se han publicado 5 metaanálisis acerca del papel del MMF en la NL en los últimos 4 años25-29, resumidos en la tabla 2. Aunque no se incluyen los datos del ensayo ALMS, todos ellos concluyen que el MMF no es inferior a la CF o puede incluso ser superior, con menos efectos secundarios en todas las formas de NL proliferativas y membranosas, también con función renal conservada. Se confirma que su eficacia como fármaco de mantenimiento es similar o algo superior a la de la azatioprina. Como consecuencia de estos datos, el MMF se ha incorporado como un fármaco de primera línea en el tratamiento de la NL, tal y como recogen varias recomendaciones de expertos30,31.
CONSIDERACIONES FUTURAS
Con los datos anteriores podemos concluir que el MMF ha supuesto un avance considerable en el tratamiento de la NL, pero quedan varias cuestiones que no tienen respuesta adecuada en el momento actual y que serán objeto de futuras investigaciones: ¿qué dosis son las más adecuadas? ¿Cuánto tiempo se debe mantener el tratamiento? ¿Qué validez tienen los niveles plasmáticos de ácido micofenólico? ¿Cómo se deben tratar los casos refractarios al tratamiento de inducción? ¿Cómo se deben tratar las recaídas en la fase de mantenimiento? ¿Es eficaz en los casos con deterioro renal?
Es posible que nos encontremos en el inicio de una cuarta etapa en el tratamiento de la NL severa donde el MMF asociado a otros inmunosupresores pueda contribuir a despejar algunas de las dudas mencionadas y mejorar los resultados actuales. Así, en un reciente ensayo clínico controlado, realizado en un reducido número de pacientes en China32, se ha encontrado que la inducción con MMF, tacrolimus y esteroides (combinación muy utilizada en los pacientes sometidos a trasplantes) consigue mejores índices de remisión que la CFiv (el 50 frente al 5%, respectivamente). Además, en un trabajo reciente, Boletis et al.33 encuentran que la administración de MMF y rituximab es capaz de reducir la proteinuria y disminuir la actividad inmune en casos refractarios. Se puede presumir que el MMF puede mejorar su eficacia en regímenes de multiterapia, dados los resultados decepcionantes que se han encontrado al usar rituximab o abertimus de forma aislada en los ensayos LUNAR y ASPEN, respectivamente.
Como conclusión, la incorporación del MMF como fármaco de primera línea de tratamiento de la NL ha supuesto un notable avance y abre nuevas formas de tratamiento que pretenden superar y sustituir a los esquemas basados en ciclofosfamida con los que nadie estaba completamente de acuerdo y que durante mucho tiempo se ha aceptado como un mal menor.
Puntos clave
1. El MMF es un fármaco eficaz y seguro en el tratamiento de la NL grave (formas proliferativas y algunas membranosas) con función renal preservada que puede sustituir al tratamiento estándar con CFiv. Su papel en los casos con un importante deterioro de función renal puede ser peligroso y su eficacia no está suficientemente estudiada.
2. El MMF combinado con esteroides como tratamiento de inducción es, al menos, similar al tratamiento estándar con CFiv y esteroides, pero con menos efectos secundarios. En los casos de NL severa es recomendable utilizar la combinación estándar de CFiv y esteroides.
3. El MMF en la fase de mantenimiento es superior a la CFiv y similar a la azatioprina, pero faltan datos a largo plazo para conocer su impacto en el desarrollo de insuficiencia renal y mortalidad. El tratamiento puede durar varios años, pero no se ha establecido el tiempo máximo.
4. El MMF es de elección en los pacientes con riesgo de infección o malignidad, preferencia de administración oral y deseos de preservar la función ovárica. Está contraindicado en la gestación por sus efectos teratogénicos. Los pacientes de raza negra e hispanos parecen responder mejor que a la CFiv.
5. No se deben superar dosis de 2 g/día, por el riesgo de infecciones o malignidad. No se conoce el papel de los niveles sanguíneos.
6. Los efectos secundarios más importantes son intestinales, que suelen mejorar al cambiar a cápsulas con cubierta entérica (micofenolato sódico).
7. Posiblemente su efecto se potencie con otros inmunosupresores: tacrolimus, rituximab u otros agentes biológicos, pero sólo hay datos preliminares.
8. La incorporación del MMF como fármaco de primera línea de tratamiento de la NL ha supuesto un notable avance y abre nuevas formas de tratamiento que pretenden superar y sustituir a los esquemas basados en ciclofosfamida.
Tabla 2. Metaanálisis de micofenolato de mofetilo en nefritis lúpica
Tabla 1. Ensayos clínicos controlados de micofenolato de mofetilo en nefritis lúpica