Revisión del artículo: Schrier RW, Abebe KZ, Perrone RD, Torres VE, Braun WE, Steinman TI, et al. Blood pressure in early autosomal dominant polycystic kidney disease. N Engl J Med 2014;371:2255-66.
¿Objetivo
Evaluar si el control intensivo de la presión arterial (PA) (95-110/60-75 mmHg) frente a un control estándar (120-130/70-80 mmHg) mediante auto-medición de la PA (AMPA) y el doble bloqueo del sistema renina-angiotensina-aldosterona (SRAA) con inhibidores de la enzima de conversión de la angiotensina (IECA) + antagonistas del receptor de la angiotensina II (ARA II), frente al bloqueo simple con IECA, ofrece beneficios renales, cardíacos y de calidad de vida en pacientes con poliquistosis renal autosómica dominante (PQRAD) en fase precoz.
¿Tipo de diseño
Ensayo clínico aleatorizado multicéntrico, doble ciego y controlado con placebo con un diseño factorial 2 x 2.
¿Ámbito
Siete centros nefrológicos de los Estados Unidos de América.
¿Pacientes
Criterios de inclusión
Pacientes con PQRAD con edades comprendidas entre los 15 y los 49 años y con filtrado glomerular estimado (FGe) por MDRD > 60 ml/min/1,73 m2 y PA normal-alta o hipertensión (HTA) y que firmaran consentimiento informado.
Criterios de exclusión
Enfermedad vascular renal, albuminuria > 0,5 g/24 h, diabetes, embarazo o intención de embarazo durante el estudio, K > 5 mEq/l, antecedente de edema angioneurótico con toma de IECA o ARA II, indicación de recibir betabloqueante o bloqueante de los canales del calcio por otra patología, necesidad de tratamiento con antiinflamatorios no esteroideos, inmunosupresores o inmunomoduladores, hospitalización en los dos últimos meses, enfermedad sistémica con afectación renal, ausencia congénita de riñón o antecedente de nefrectomía, esperanza de vida < 2 años, haber recibido otro fármaco de estudio en los 30 días previos, antecedentes de incumplimiento terapéutico, dependencia del alcohol u otras drogas o antecedente psiquiátrico en el último año, presencia de aneurisma cerebral de más de 7 mm no clipado o toma de suplementos de creatinina en los últimos tres meses.
¿Intervenciones
Los pacientes fueron aleatorizados en una ratio 1:1 a recibir lisinopril + telmisartán frente a lisinopril + placebo y también en una ratio 1:1 a conseguir un control intensivo de la PA frente a un control estándar. Para conseguir el control de la PA preestablecido, se permitía la asociación de otros fármacos antihipertensivos de forma controlada. Se realizó un seguimiento a 5 años.
¿Variables de resultado
Variable principal
Porcentaje de cambio de volumen renal al final del seguimiento determinado por resonancia magnética nuclear (RMN) renal.
Variables secundarias
– Velocidad de cambio de la función renal medido por FGe por MDRD.
– Cambios en la excreción urinaria de albúmina y en el índice de masa ventricular izquierda (IMVI) (mediante RMN cardíaca).
– Otras: excreción urinaria de aldosterona, flujo sanguíneo renal, frecuencia de hospitalización por cualquier causa y por causa cardiovascular, calidad de vida, frecuencia de dolor relacionado con síntomas de la enfermedad y efectos adversos.
¿Tamaño muestral y estadística
Asumiendo ausencia de interacción en el diseño 2 x 2, se estimó que se requerían 466 pacientes para detectar una reducción del 25 % en la velocidad de crecimiento del volumen renal total, esto es, de 5,4 % a 4,1 % por año, con una potencia del 90 % al 5 % de significación estadística. Teniendo en cuenta unas pérdidas del 15 %, este número se incrementó hasta 548 pacientes. Con el diseño final, el estudio tuvo una potencia superior al 95 % para detectar una reducción del 25 % en la velocidad de crecimiento renal. Todos los análisis se desarrollaron basados en el análisis por intención de tratar.
¿Promoción y conflicto de intereses
Los fármacos antihipertensivos fueron cedidos por las farmacéuticas Merck (lisinopril) y Boehringer Ingelheim (telmisartán y placebo), pero ninguna de las dos compañías participó en el diseño del estudio, la recolección de datos, el análisis o la redacción del artículo. El estudio se llevó a cabo con financiación derivada de becas del National Institute of Diabetes and Digestive and Kidney Diseases, National Center for Research Resources General Clinical Research Centers, National Center for Advancing Translational Sciencies Clinical and Translational Science Awards, y con financiación procedente de The Zell Family Foundation y de la PKD Foundation.
Varios de los autores reconocen recibir retribución económica como miembros de advisory boards o consultores de Otsuka, Janssen, Sanofi, Vertex Pharmaceuticals, Wyeth-Pfizer, Novartis y Kadmon.
¿ RESULTADOS PRINCIPALES
Análisis basal de los grupos
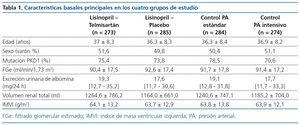
Se aleatorizaron 558 pacientes. Los cuatro grupos resultaron ser homogéneos para todas las variables. En la tabla 1 se muestran las características basales de las principales variables estudiadas. Hubo un 18,1 % de pérdidas de seguimiento, con proporciones similares en los cuatro grupos.
¿ RESULTADOS DEL ESTUDIO DE CONTROL INTENSIVO FRENTE A CONTROL ESTÁNDAR DE LA PRESIÓN ARTERIAL
Se consiguieron mantener las diferencias de PA a lo largo del estudio, de manera que las diferencias de PA sistólica y PA diastólica medidas por AMPA fueron de 13,4 mmHg y 9,3 mmHg, respectivamente. El grupo de control intensivo requirió una media de dos fármacos antihipertensivos adicionales frente a uno en el grupo de control estándar. La proporción de pacientes que requirieron varios fármacos antihipertensivos en el grupo de control intensivo frente al grupo de control estándar fue significativamente mayor (diuréticos 44,9 % frente a 26,8 %, p < 0,001; beta o alfabloqueantes 31,4 % frente a 14,4 %, p < 0,001; calcioantagonistas 10,2 % frente a 5,3 %, p = 0,03). La dosis media de lisinopril fue más de 8 mg/día mayor en el grupo de control intensivo respecto al grupo de control estándar de la PA.
Variable principal
Los pacientes con control intensivo de la PA presentaron un 14,2 % menos de incremento en el volumen renal total anualmente (5,6 % frente a 6,6 %, p = 0,006). El volumen renal total se incrementó un 38 % respecto al basal en el grupo de control intensivo y un 44,2 % en el de control estándar (1636 ml [intervalo de confianza (IC) al 95 % 1489-1782 ml] y 1788 ml [IC 95 % 1639-1938 ml]). El control intensivo fue más beneficioso en los subgrupos de pacientes: > 30 años, varones, volumen renal basal percentil ≥ 75 y FGe basal ≥ 80 ml/min/1,73 m2.
Variables secundarias
En relación con la reducción del FGe en el seguimiento a corto plazo (4 meses), el grupo de control intensivo experimentó una mayor pérdida de función renal respecto al grupo de control estándar de la PA (-3,1 frente a 0,5 ml/min/1,73 m2 en 4 meses, p < 0,001).
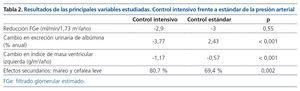
Los principales resultados en relación con las variables secundarias al final del seguimiento se muestran en la tabla 2.
¿RESULTADOS DEL ESTUDIO DE LISINOPRIL + TELMISARTÁN FRENTE A LISINOPRIL + PLACEBO
Variable principal
El volumen renal total se incrementó a velocidad similar en el grupo lisinopril + telmisartán y en el de lisinopril + placebo (6,0 % y 6,2 %/año, respectivamente, p = 0,52). El volumen renal total se incrementó un 40,5 % en el grupo lisinopril + telmisartán y un 42,2 % en el de lisinopril + placebo (1777 ml [IC 95 % 1617-1937 ml] y 1655 ml [IC 95 % 1518-1792 ml]) al final del seguimiento.
Variables secundarias
El filtrado glomerular se redujo de forma similar en el grupo lisinopril + telmisartán y en el grupo lisinopril + placebo (-3,0 ml/min/1,73 m2/año y -2,86 ml/min/1,73 m2/año, p = 0,55). No se encontraron diferencias relevantes entre grupos en relación con las otras principales variables secundarias.
¿CONCLUSIONES DE LOS AUTORES
El doble bloqueo del SRAA no tiene efecto en relación con la velocidad de crecimiento renal ni con la velocidad de pérdida de la función renal. El control intensivo de la PA es seguro en pacientes poliquísticos hipertensos jóvenes con función renal preservada. El control intensivo de la PA, comparado con un control estándar, se asocia a una modesta reducción del volumen renal total sin diferencias en la velocidad de pérdida de la función renal. La mejoría en el IMVI y la excreción urinaria de albúmina también sugiere beneficios a favor de un control intensivo de la PA.
¿COMENTARIOS DE LOS REVISORES
La PQRAD es la enfermedad genética con afectación renal más común y representa la causa de entrada en tratamiento renal sustitutivo de aproximadamente el 10 % de los pacientes que lo requieren. La HTA (siendo la actividad del SRAA su principal determinante) es altamente prevalente en los pacientes con PQRAD y, junto al tipo de mutación, la edad y el volumen renal, representa uno de los principales factores de progresión de la enfermedad. Por otro lado, la HTA está directamente implicada en la mortalidad cardiovascular, que es la principal causa de muerte de estos pacientes. En el momento actual, no existe ningún tratamiento específico aprobado para esta enfermedad, con lo que conocer el tipo de tratamiento antihipertensivo más indicado y el grado de control tensional que más beneficios ofrece es fundamental1,2.
Este estudio, realizado en pacientes poliquísticos en fases muy precoces de la enfermedad con función renal conservada, demuestra que ni el doble bloqueo del SRAA ni un control muy estricto de la PA ofrecen beneficios en relación con un enlentecimiento en la pérdida de la función renal. Sin embargo, el control intensivo de la PA proporciona beneficios evidentes en relación con una menor velocidad de crecimiento renal (que se ha descrito como el principal factor pronóstico de pérdida de función renal) y en la lesión subclínica de órgano diana a nivel renal y cardíaco, lo cual conferiría a estos pacientes un menor riesgo cardiovascular en relación con un mejor perfil cardiovascular.
Desde el punto de vista metodológico, se trata de un ensayo clínico aleatorizado, doble ciego, con tamaño muestral adecuado en un grupo de población homogéneo, lo que le confiere validez tanto interna como externa.
¿CONCLUSIONES DE LOS REVISORES
Ni el control intensivo de la PA ni el doble bloqueo del SRAA se asocian a un enlentecimiento en la pérdida de función renal en poliquistosis precoz, aunque el control intensivo de la PA sí se relaciona con una reducción en la velocidad de aumento en el tamaño renal. Por lo tanto, de nuevo, en un ensayo en PQRAD existe una disociación entre el efecto sobre el crecimiento renal y la pérdida de función renal, lo que enfatiza la importancia de proponer outcomes fuertes en ensayos clínicos en PQRAD. Debería plantearse si con más tiempo de seguimiento el enlentecimiento en el crecimiento renal se puede acompañar también de una menor pérdida de función renal en estadios precoces de la enfermedad.
¿CLASIFICACIÓN
Tema: Poliquistosis renal autosómica dominante (PQRAD)
Subtema: Evolución PQRAD precoz en relación con la HTA y su tratamiento
Tipo de artículo: Tratamiento antihipertensivo, pronóstico
Palabras clave: Ensayo clínico aleatorizado. PQRAD. Volumen renal. Hipertensión arterial
NIVEL DE EVIDENCIA: Alta
GRADO DE RECOMENDACIÓN: Fuerte
(GRADE [www.gradeworkinggroup.org] divide la calidad de la evidencia en cuatro grupos: alta, moderada, baja y muy baja; y divide el grado de recomendación en dos grupos: fuerte y débil).