La hiperpotasemia (HK) es frecuente en pacientes con enfermedad renal crónica (ERC) tratados con inhibidores del sistema renina-angiotensina-aldosterona (iSRAA) y antagonistas del receptor de mineralocorticoides (ARM). Aunque los nuevos quelantes han mostrado eficacia en ensayos clínicos, falta evidencia en práctica clínica real.
Materiales y métodosPresentamos un estudio retrospectivo observacional, multicéntrico, no intervencionista con el objetivo de evaluar el uso de patirómero en pacientes con HK en condiciones de práctica clínica habitual en la Comunidad Valenciana. Se incluyeron pacientes que habían recibido patirómero al menos tres meses por haber presentado HK. El objetivo primario del estudio fue evaluar la evolución del potasio sérico a los meses 1, 3, 6 y 12 del inicio del tratamiento. Los objetivos secundarios fueron definir las características basales de los pacientes, las modificaciones en el tratamiento con iSRAA y ARM y los efectos secundarios relacionados con patirómero.
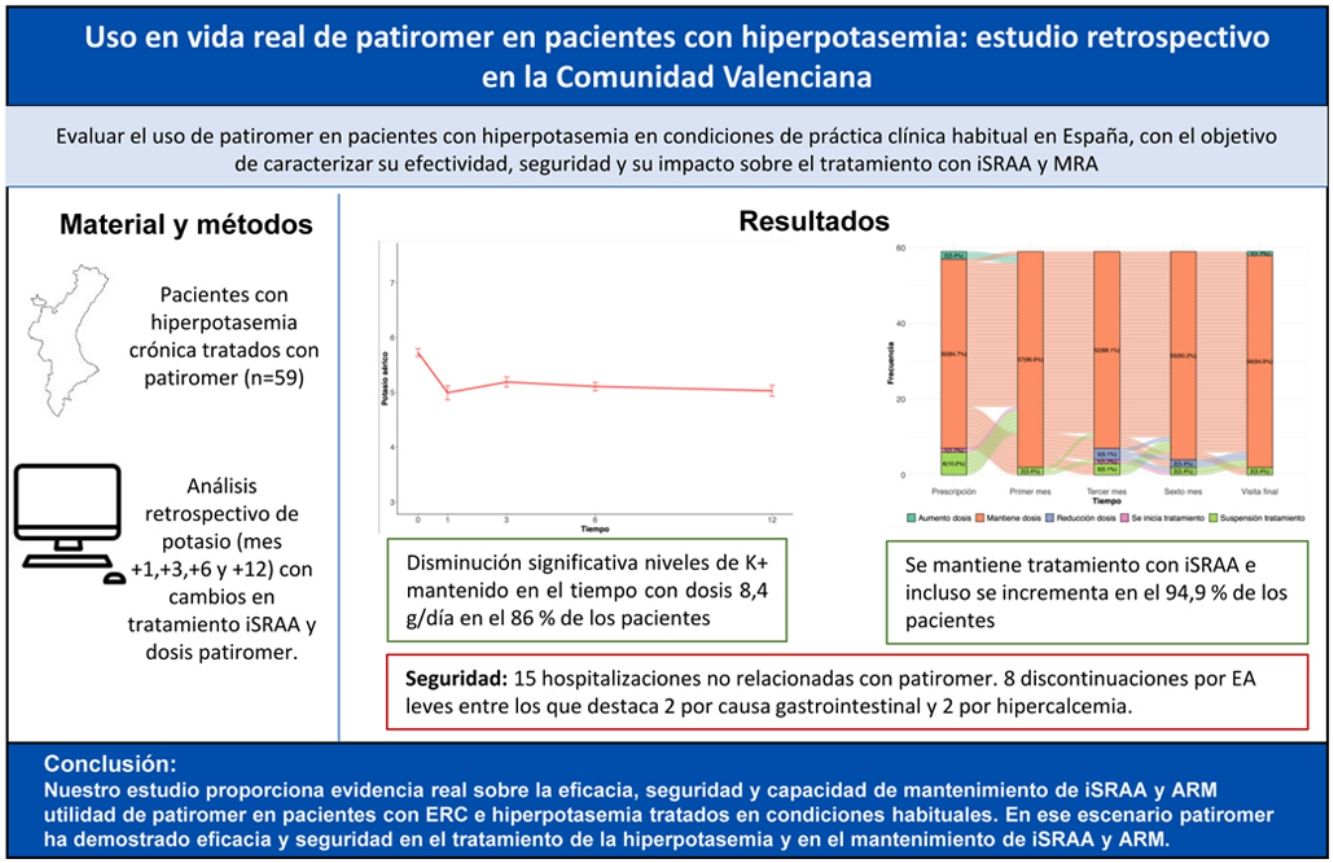
ResultadosSe incluyeron 59 pacientes. El valor inicial de potasio sérico fue de 5,72 mmol/L, mostrando descensos significativos al mes, 3, 6 y 12 meses (5,02 mmol/L, 5,17 mmol/L, 5,11 mmol/L y 5,01 mmol/L, respectivamente. Todos p<0,001). El tratamiento con patirómero permitió mantener los iSRAA en el 94,9% de los pacientes y los ARM en el 83,3%. Los efectos adversos más frecuentes fueron de carácter gastrointestinal. El patirómero fue suspendido en ocho pacientes (13,5%), siendo la causa los efectos adversos solo en la mitad de ellos.
ConclusionesNuestro estudio proporciona evidencia real sobre la eficacia, seguridad y capacidad de mantenimiento de iSRAA y ARM de patirómero en pacientes con ERC e HK tratados en condiciones de práctica clínica habitual.
Hyperkalaemia is common in patients with chronic kidney disease (CKD) treated with renin-angiotensin-aldosterone system inhibitors (RAASi) and mineralocorticoid receptor antagonists (MRAs). Although new potassium binders have demonstrated efficacy in clinical trials, evidence from real-world clinical practice remains limited.
Materials and methodsWe present a retrospective, observational, multicentre, non-interventional study aimed at evaluating the use of patiromer in patients with hyperkalaemia under routine clinical conditions in the Valencian Community. Patients who received patiromer for at least 3 months due to hyperkalaemia were included. The primary objective was to assess the evolution of serum potassium at 1, 3, 6, and 12 months after initiation of treatment. Secondary objectives included describing baseline patient characteristics, changes in RAASi and MRA therapy, and patiromer-related adverse events.
ResultsA total of 59 patients were included. The baseline serum potassium level was 5.72 mmol/L, showing significant reductions at 1, 3, 6, and 12 months (5.02, 5.17, 5.11, and 5.01 mmol/L, respectively; all p <0.001). Patiromer treatment enabled continuation of RAASi in 94.9% of patients and MRAs in 83.3%. The most frequent adverse events were gastrointestinal. Patiromer was discontinued in 8 patients (13.5%), with adverse effects accounting for half of these cases.
ConclusionsOur study provides real-world evidence on the effectiveness, safety, and RAASi/MRA maintenance potential of patiromer in patients with CKD and hyperkalaemia under routine care. In this setting, patiromer proved effective and well tolerated for managing hyperkalaemia and preserving RAASi/MRA therapy.
La hiperpotasemia (HK) se define como una concentración sérica de potasio superior al límite de la normalidad que se sitúa en torno a los 5 mmol/L, aunque se considera clínicamente relevante por encima de 5,5 mmol/L. Es un trastorno grave ya que puede provocar arritmias potencialmente mortales1. La HK es especialmente frecuente en pacientes con enfermedad renal crónica (ERC) y/o insuficiencia cardiaca (IC). Se estima que en torno al 28% de los pacientes con filtrado glomerular estimado (FGe) <60mL/min/1,73 m2 presentan HK durante el seguimiento2.
Los tratamientos recomendados para pacientes con IC y/o ERC incluyen inhibidores del sistema renina-angiotensina-aldosterona (iSRAA), así como, en determinados casos, antagonistas del receptor mineralocorticoide (ARM). Estas terapias han demostrado reducir la morbilidad cardiovascular, ralentizar la progresión de la enfermedad renal y mejorar la supervivencia global en estos pacientes3,4. No obstante, su uso se asocia a un aumento del riesgo de HK2, por ello, a pesar de sus beneficios nefroprotectores y cardioprotectores, su mantenimiento a largo plazo no siempre es posible, especialmente en pacientes con disfunción renal grave o comorbilidades avanzadas que elevan el riesgo de HK5.
Históricamente, el único tratamiento disponible para el manejo crónico de la HK eran las resinas de intercambio catiónico, como el poliestireno sulfonato sódico o cálcico. No obstante, su uso presenta importantes limitaciones clínicas como frecuentes efectos gastrointestinales, especialmente estreñimiento, incluyendo casos graves de necrosis intestinal, riesgo de hipopotasemia y la falta de ensayos controlados y de datos robustos sobre su eficacia y seguridad a largo plazo6,7.
Es evidente que persiste una necesidad clínica no cubierta en pacientes con HK, especialmente en aquellos que no pueden recibir o mantener dosis óptimas de iSRAA o ARM. La reducción o interrupción de estos fármacos por riesgo de HK se asocia a un aumento significativo de la morbimortalidad cardiovascular y renal8. En los últimos años han emergido nuevas alternativas terapéuticas, entre ellos, ciclosilicato de sodio y zirconio (Lokelma®) y patirómero (Veltassa®). Patirómero es un polímero no absorbible que intercambia calcio por potasio en el colon, facilitando su eliminación y reduciendo eficazmente los niveles séricos de potasio. Ha demostrado eficacia sostenida y un perfil de seguridad favorable en estudios clínicos y en práctica real, permitiendo la optimización del tratamiento con iSRAA con un control adecuado de potasio sérico. En este contexto, nos proponemos evaluar el uso de patirómero en pacientes con HK en condiciones de práctica clínica habitual en la población estudiada, con el objetivo de caracterizar su efectividad, seguridad y su impacto sobre el tratamiento con iSRAA y MRA9,10. Para ello ha realizado un estudio de vida real analizando la evolución del potasio sérico en los meses posteriores al inicio de patirómero, como objetivo primario. Como objetivos secundarios se analizarán 1) las características basales del paciente, 2) las modificaciones en el tratamiento con iSRAA y ARM, 3) efectos secundarios relacionados con patirómero.
Material y métodosDiseño del estudioSe trata de un estudio observacional, retrospectivo, multicéntrico y no intervencionista para evaluar el uso en vida real de patirómero (Veltassa®) en pacientes con HK crónica tratados en condiciones de práctica clínica habitual en la Comunidad Valenciana (España). El estudio se diseñó siguiendo las recomendaciones del Real Decreto 957/2020 sobre estudios observacionales con medicamentos.
Tamaño muestralEl tamaño muestral mínimo se estimó en 45 pacientes para detectar una diferencia media de 0,5 mmol/L en los niveles de potasio sérico, con una desviación estándar de 0,9, mediante una prueba t pareada bilateral para una sola muestra, asumiendo un riesgo alfa de 0,05 y una potencia estadística del 95%. Este cálculo se basó en datos de variabilidad procedentes de estudios previos de prevención y tratamiento de la HK11,12 y en la consideración de una diferencia clínicamente relevante definida por el equipo investigador. Considerando una tasa de pérdidas del 10%, se estimó necesario incluir al menos 50 pacientes para analizar el objetivo primario del estudio. El cálculo se realizó utilizando el software G*Power versión 3.1.9.713.
Población y criterios de inclusiónSe incluyeron pacientes adultos (≥ 18 años) que hubieran iniciado tratamiento con patirómero entre el 1 de septiembre de 2019 y el 20 de enero de 2021. Se exigió una duración mínima del tratamiento de tres meses y la presencia de HK crónica, definida como ≥ 2 episodios de potasio sérico ≥ 5,0 mmol/L separados por al menos dos semanas en los 12 meses previos. Se excluyeron pacientes con pseudohiperpotasemia (leucocitosis marcada, trombocitosis o hemólisis en la muestra), hiperplasia suprarrenal congénita, enfermedad de Addison, grandes quemaduras o en tratamiento con suplementos de potasio. La información necesaria para aplicar estos criterios se obtuvo mediante un cuestionario específico y la revisión de la historia clínica en el momento de la inclusión en la base de datos.
Recogida de datosLos datos clínicos se obtuvieron de forma retrospectiva a partir de las historias clínicas electrónicas de los pacientes en una base de datos web elaborada por el instituto de investigación INCLIVA con las características de seguridad y anonimización según legalidad vigente. Se recogieron variables sociodemográficas, antropométricas, comorbilidades, parámetros analíticos, y tratamientos concomitantes, especialmente iSRAA y ARM.
La evolución del potasio sérico se evaluó longitudinalmente en distintos puntos de seguimiento (meses 1, 3, 6 y 12). Asimismo, se documentaron los cambios en el régimen terapéutico con iSRAA y ARM, así como la dosis y adherencia al tratamiento con patirómero cuando esta información estaba disponible.
Variables del estudioLa variable principal fue la evolución del potasio sérico en los meses posteriores al inicio de patirómero. Como variables secundarias se analizaron: 1) características basales del paciente, 2) modificaciones en el tratamiento con iSRAA y ARM, 3) efectos secundarios relacionados con patirómero. Para la redacción de este manuscrito, los datos del estudio han sido descritos de acuerdo con la normativa STROBE para estudios retrospectivos14.
Análisis estadísticoLas variables cuantitativas se presentaron como media y desviación estándar o mediana e intervalo intercuartílico, según su distribución. Los cambios a lo largo del tiempo (prescripción, primer mes, tercer mes, sexto mes y visita final) de la variable principal y el resto de los parámetros analíticos se estudiaron mediante un modelo lineal de efectos mixtos con el valor en cada tiempo como variable dependiente, el tiempo como variable independiente y el indicador del individuo como factor aleatorio. El análisis estadístico se realizó utilizando el software R (versión 3.6.1). Se consideraron estadísticamente significativos los valores de p <0,05.
Consideraciones éticasEl estudio fue aprobado por el Comité de Ética de la Investigación con medicamentos (CEIm) del Hospital Clínico Universitario de Valencia (Código: HK-01-21, número: 17/22). Todos los procedimientos se llevaron a cabo de acuerdo con la Declaración de Helsinki y las directrices de buena práctica clínica. Se obtuvo consentimiento informado por escrito para el uso de los datos clínicos. En casos de pacientes fallecidos o perdidos en el seguimiento, se eximió este requisito conforme a la normativa vigente.
ResultadosCaracterísticas de los pacientesSe incluyeron un total de 59 pacientes con diagnóstico de HK que iniciaron tratamiento con patirómero durante el periodo de seguimiento pertenecientes a seis hospitales de la Comunidad Valenciana. La edad media fue de 73,8±11,6, mediana de 76 (67-83) y el 59% eran hombres. Las etiologías de la ERC de los pacientes fueron de origen vascular/otras o desconocidas en 26 (44%) pacientes, enfermedad renal diabética en 22 (37%) pacientes y glomerulopatía en 11 (19%) pacientes. El seguimiento medio fue de 11,1±4,7 meses (rango: 3-28), mediana 11,9 (7,3-13).
La mayoría de las prescripciones procedieron de Nefrología (45 [76%] pacientes), de los cuales 15 estaban en seguimiento compartido con Cardiología o Unidades Cardiorrenales, uno en seguimiento común con Medicina Interna y Cardiología, y uno con Medicina Interna. Cardiología fue la especialidad prescriptora en 8 (14%) pacientes y Medicina Interna en 6 (10%), ambos dentro de Unidades Cardiorrenales. Las características basales de los pacientes, así como los datos analíticos basales se resumen en la tabla 1. Antes de iniciar el estudio, nueve pacientes recibían ARM. En tres de ellos se suspendió dicho tratamiento en el momento de iniciar patirómero. De esta manera, en el estudio solo seis pacientes recibían ARM (10%). En un caso se suspendió en la visita del tercer mes y otro paciente inició tratamiento con ARM en la visita del sexto mes. El tratamiento con patirómero permitió mantener el 85% de los pacientes que recibían ARM y además permitió reiniciarlo en un nuevo paciente al que se la había suspendido antes de iniciar el estudio.
Características basales de los pacientes del estudio
| Características | n=59 |
|---|---|
| Edad (años), mediana (RIQ) | 76 (67-83) |
| Sexo masculino, n (%) | 35 (59) |
| Seguimiento medio, meses (media±DE) | 11,1±4,7 |
| IMC, media±DE (n=51) | 28,5±4,2 |
| Especialista prescriptor | |
| Nefrología | 45 (76) |
| Cardiología | 8 (14) |
| Medicina Interna | 6 (10) |
| Etiología ERC n (%): | |
| Glomerular | 11 (19) |
| Vascular | 14 (24) |
| Nefropatía diabética | 22 (37) |
| Otras | 12 (20) |
| Fumadores, n (%) | 11 (19) |
| DM, n, (%) | 37 (63) |
| Antecedente de IC con hospitalización, n (%) | 19 (32) |
| Tramos de FGe, n (%) | |
| FGe <15, n (%) | 6 (10) |
| FGe 15-29, n (%) | 23 (39) |
| FG FGe 30-59, n (%) | 27 (46) |
| FGe> 60, n (%) | 3 (5) |
| FGe, mL/min/m2, media±DS | 32,3±16,4 |
| Creatinina, mg/dL (media±DS) | 2,3±0,9 |
| Hiperkalemia basal (> 5,5 mmol/L), n (%) | 33 (56) |
| K+sérico basal, mmol/L, media±DS | 5,7±0,5 |
| Ultima cifra de K+antes del estudio, media±DS | 5,3±0,6 |
| Número de determinaciones de K+en los últimos 2 años, media±DS | 18±13 |
| NYHA Grado II-IV, n (%) | 21 (36) |
| FEVI, %, n (%) | |
| Normal (≥ 50%) | 28 (48) |
| Media (41-49%) | 5 (8) |
| Reducida (≤ 40%) | 5 (8) |
| No disponible | 21 (36) |
| FEVI, %, mediana, RIQ | 60 (37) |
| Cardiopatía isquémica, n (%) | 20 (34) |
| AcxFA, n (%) | 12 (20) |
| Enfermedad vascular periférica, n (%) | 15 (25) |
| HTA, n (%) | 55 (93) |
| Seguimiento previo de los pacientes, n (%) | Nefrología 48 (81) |
| Cardiología 30 (51) | |
| Medicina interna 13 (22) | |
| Prescripción previa de resinas de intercambio, n (%) | 37 (63) |
| Bloqueo del SRAA o ARNI, n (%) | 59 (100) |
| BSRAA Dosis máxima, n % | 16 (27) |
| Tratamiento con ARM, n (%) | 6 (10) |
| Dosis máxima de ARM, n (%) | 4 (7) |
| Prescripción previa de quelantes (resinas) | 23 (39) |
| Presión arterial sistólica, mmHg, (media±DS) | 138±15 |
| Presión arterial diastólica, mmHg, (media±DS) | 70±8 |
| Colesterol total, mg/dL (media±DS) | 151±32 |
| LDL-c, mg/dL (media±DE) | 86±26 |
| HDL-c, mg/dL (media±DE) | 45±11 |
| Triglicéridos, mg/dL (media±DE) | 155±83 |
| Ácido úrico, mg/dL (media±DE) | 6,6±1,7 |
| Sodio, mmol/L (media±DE) | 140±3,6 |
| Hemoglobina, g/dL (media±DE) | 12,3±1,6 |
| Calcio, mg/dL (media±DE) | 9,4±0,5 |
| Magnesio, mg/dL (media±DE) | 2,1±0,2 |
| Cociente albúmina/creatinina en orina, mg/g (mediana, RIQ), (n=31) | 170 (5-537) |
| NtProBNP, pg/mL (mediana, RIQ), (n=21) | 1.433 (822-4.383) |
Los resultados se muestran como frecuencia y porcentaje o como media±desviación estándar (DE) o mediana y rango intercuartílico (RIQ) dependiendo de la distribución de las variables.
ERC: enfermedad renal crónica; FGe: filtrado glomerular estimado; K: potasio; IMC: índice de masa corporal; HTA: hipertensión arterial; SRAA: sistema renina-angiotensina-aldosterona; BSRAA: bloqueo del sistema renina angiotensina-aldosterona; ARNI: inhibidores del receptor de angiotensina-neprilisina; ARM: antagonistas del receptor mineralocorticoide; DM: diabetes mellitus; IC: insuficiencia cardiaca; FEVI: fracción de eyección del ventrículo izquierdo; NYHA: escala de disnea de la «New York Heart Association»; AcxFA: fibrilación auricular; LDL-c: colesterol de lipoproteínas de baja densidad; HDL-c: colesterol de lipoproteínas de alta densidad.
El número de pacientes de aquellas variables que no se recogieron en la totalidad de los pacientes se muestra entre paréntesis.
Solo un paciente había presentado antecedente de HK que motivara la hospitalización, en cambio 33 (56%) pacientes habían presentado HK en el seguimiento previo el último año. Previamente al inicio del periodo de estudio, 23 (39%) pacientes habían recibido resinas de intercambio de los cuáles en 20 (87%) se suspendieron por intolerancia o falta de eficacia.
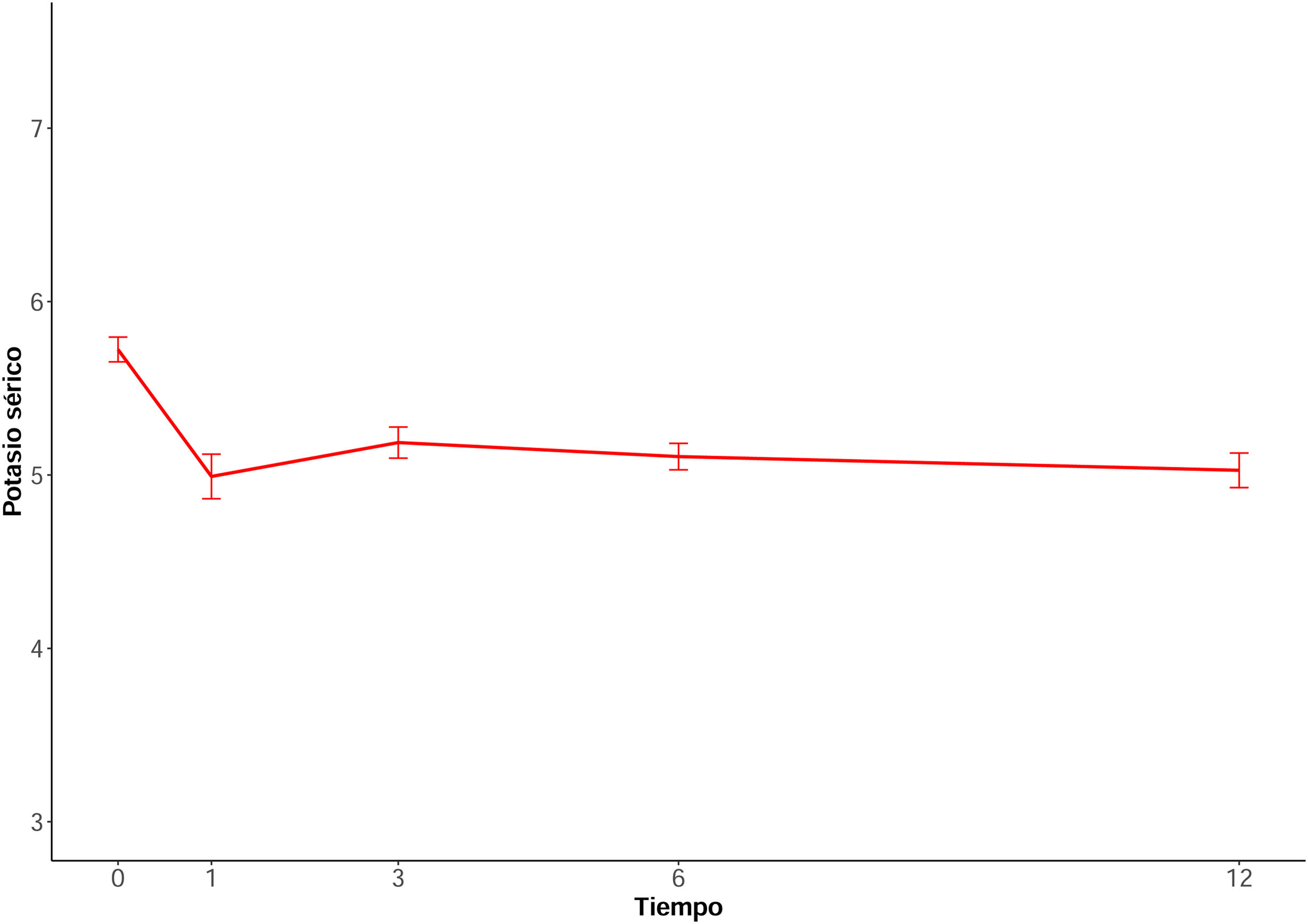
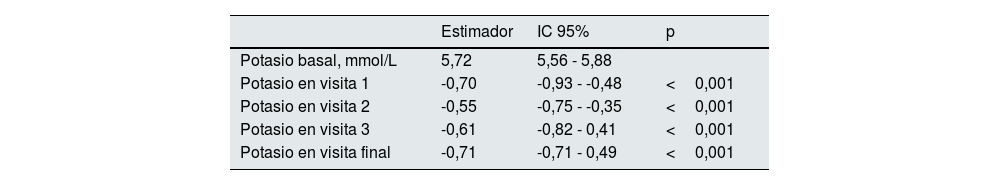
Evolución niveles de potasio y parámetros bioquímicosTodos los pacientes iniciaron tratamiento con patirómero 8,4g/día. El tratamiento con patirómero logró una disminución significativa de los niveles de potasio sérico durante el seguimiento (valor p <0,001) (fig. 1). En el análisis mediante modelo lineal mixto (tabla 2), el valor estimado inicial fue de 5,72 mmol/L, y se observaron descensos significativos (p <0,001) en la cifra de potasio sérico respecto a la cifra basal, siendo de 5,02 mmol/L al mes, 5,17 mmol/L a los tres meses, 5,11 mmol/L a los seis meses y 5,01 mmol/L al año (p <0,001 en todos los casos frente al valor basal). Estos resultados reflejan una disminución media de entre 0,55 y 0,71 mmol/L respecto al inicio, con una eficacia sostenida a lo largo del seguimiento.
Cambios en la cifra de potasio sérico durante la evolución del estudio. Análisis mediante modelo lineal de efectos mixtos con el valor en cada tiempo como variable dependiente (fig. 1)
| Estimador | IC 95% | p | |
|---|---|---|---|
| Potasio basal, mmol/L | 5,72 | 5,56 - 5,88 | |
| Potasio en visita 1 | -0,70 | -0,93 - -0,48 | <0,001 |
| Potasio en visita 2 | -0,55 | -0,75 - -0,35 | <0,001 |
| Potasio en visita 3 | -0,61 | -0,82 - 0,41 | <0,001 |
| Potasio en visita final | -0,71 | -0,71 - 0,49 | <0,001 |
En el análisis con trayectorias individuales, un 83% de los pacientes consiguió niveles de potasio menores a 5,5 mmol/L al finalizar el estudio.
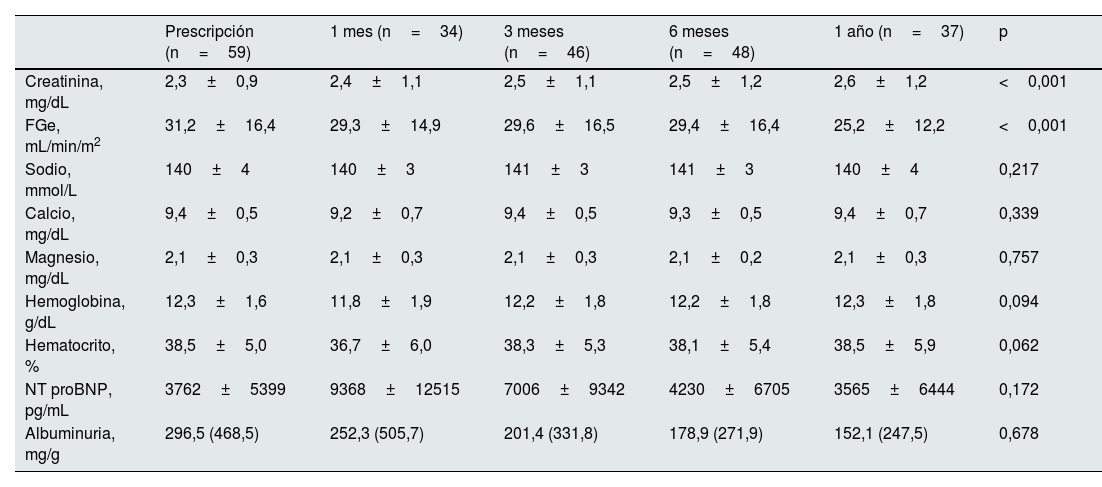
La evolución de los parámetros analíticos se muestra en la tabla 3. No hubo incremento significativo de los niveles de calcio ni sodio en plasma. Además, los niveles de NtproBNP se mantuvieron estables durante el seguimiento.
Evolución de los distintos parámetros analíticos durante el seguimiento
| Prescripción (n=59) | 1 mes (n=34) | 3 meses (n=46) | 6 meses (n=48) | 1 año (n=37) | p | |
|---|---|---|---|---|---|---|
| Creatinina, mg/dL | 2,3±0,9 | 2,4±1,1 | 2,5±1,1 | 2,5±1,2 | 2,6±1,2 | <0,001 |
| FGe, mL/min/m2 | 31,2±16,4 | 29,3±14,9 | 29,6±16,5 | 29,4±16,4 | 25,2±12,2 | <0,001 |
| Sodio, mmol/L | 140±4 | 140±3 | 141±3 | 141±3 | 140±4 | 0,217 |
| Calcio, mg/dL | 9,4±0,5 | 9,2±0,7 | 9,4±0,5 | 9,3±0,5 | 9,4±0,7 | 0,339 |
| Magnesio, mg/dL | 2,1±0,3 | 2,1±0,3 | 2,1±0,3 | 2,1±0,2 | 2,1±0,3 | 0,757 |
| Hemoglobina, g/dL | 12,3±1,6 | 11,8±1,9 | 12,2±1,8 | 12,2±1,8 | 12,3±1,8 | 0,094 |
| Hematocrito, % | 38,5±5,0 | 36,7±6,0 | 38,3±5,3 | 38,1±5,4 | 38,5±5,9 | 0,062 |
| NT proBNP, pg/mL | 3762±5399 | 9368±12515 | 7006±9342 | 4230±6705 | 3565±6444 | 0,172 |
| Albuminuria, mg/g | 296,5 (468,5) | 252,3 (505,7) | 201,4 (331,8) | 178,9 (271,9) | 152,1 (247,5) | 0,678 |
Los valores se muestran con media±desviación estándar o mediana y (RIQ) según distribución de la variable.
FGe: filtrado glomerular estimado.
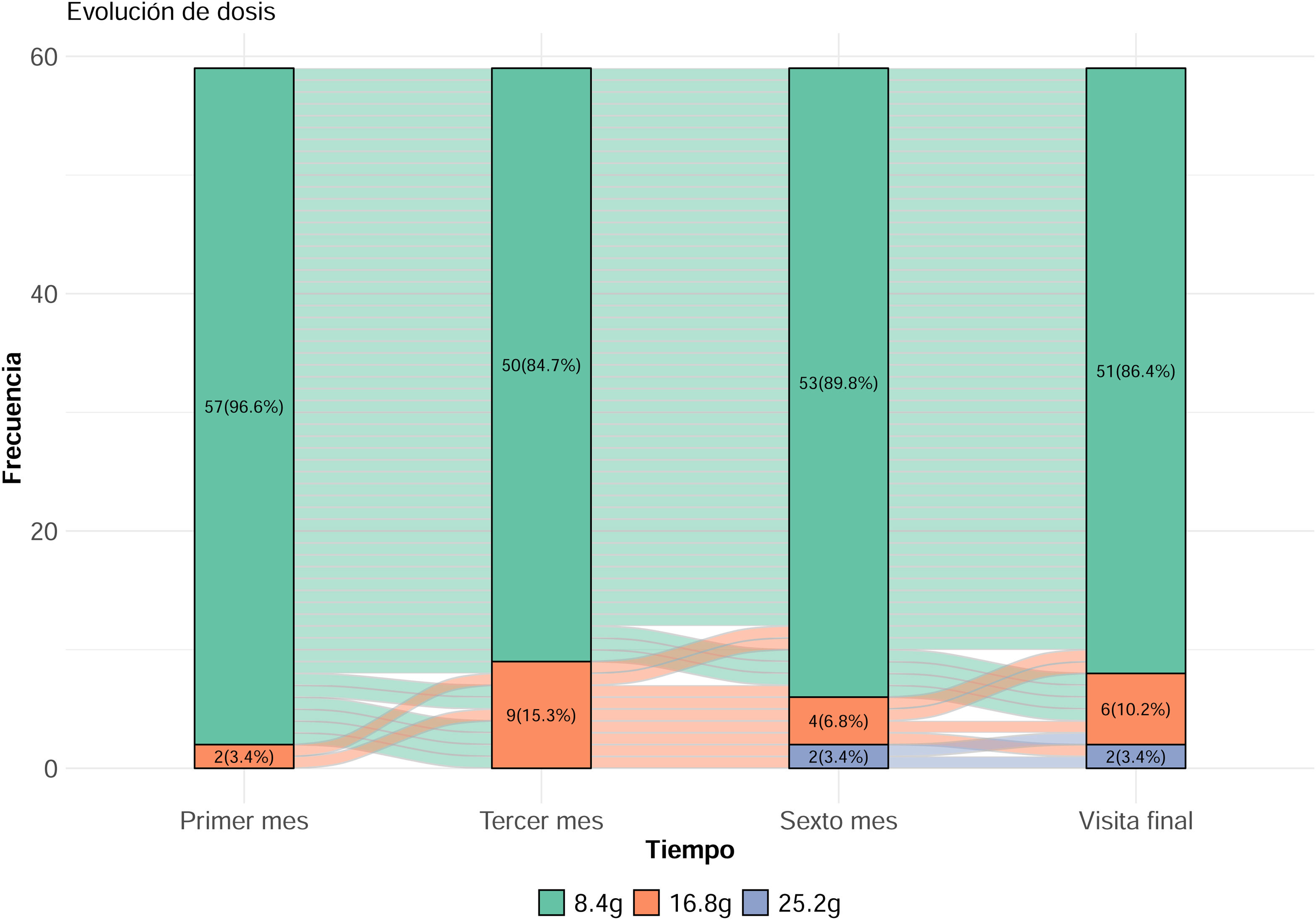
La dosis inicial de patirómero fue de 8,4g en 57 (96%) pacientes y 16,8g en dos (4%) pacientes. La dosis inicial de patirómero se mantuvo en 47 (79,8%) pacientes. Se aumentó en 3 (5%) pacientes, se disminuyó en un (1,6%) paciente y se suspendió en 8 pacientes. En la figura 2 se muestran la evolución de la dosis de patirómero en los pacientes.
Evolución de la dosis de patiromer entre las visitas. La mayoría de los pacientes se mantuvo con dosis de patiromer de 8,4g a lo largo del estudio. Al final del estudio el 86,4% de los pacientes lograron control de la hiperpotasemia con 8,4mg/día. El 10,2% precisaron la dosis de 16,8g/día y solo el 3,4% precisaron la dosis de 25,2g/día.
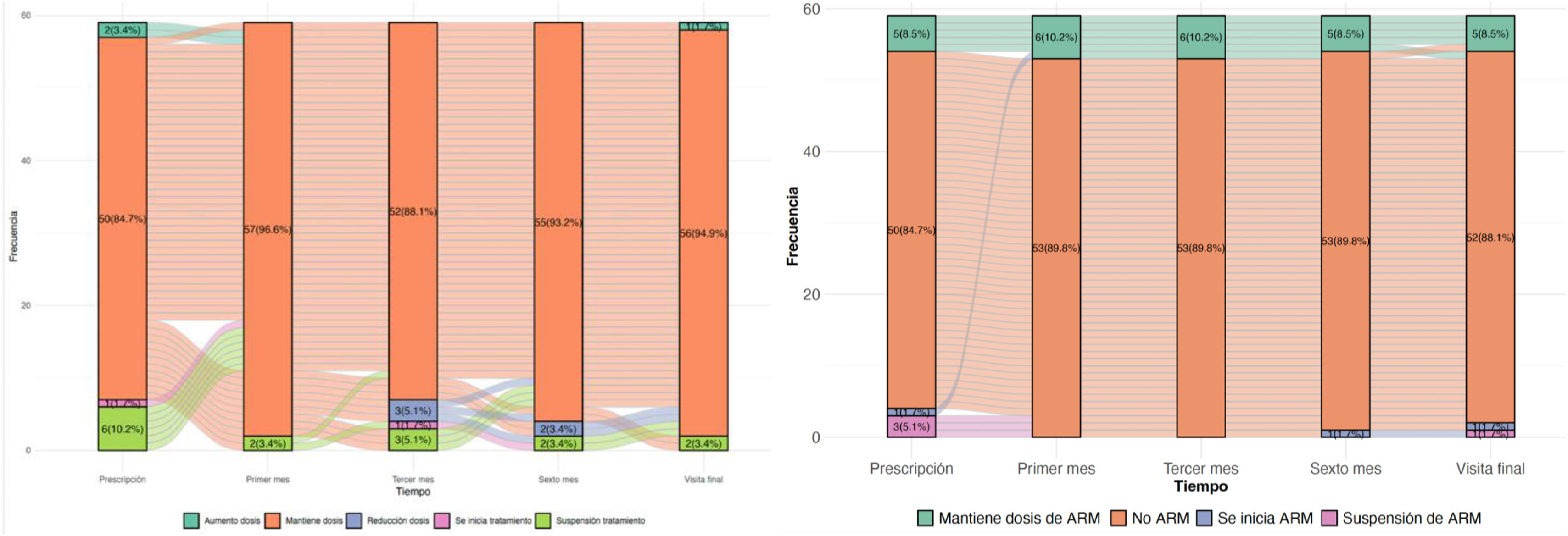
En la figura 3 se observa los cambios en los tratamientos con iSRAA y ARM detectados en los pacientes del estudio. Se observa que el tratamiento con patirómero permitió mantener los iSRAA en el 94,9% de los pacientes y los ARM en el 83,3%. Los iSRAA solo se suspendieron en 2 (3,4%) pacientes en el caso de ARM solo se suspendió en un (1,7%) paciente y se inició el ARM en un paciente al que se le había suspendido antes de la visita basal del estudio. Este aspecto es de interés en un estudio de vida real retrospectivo en los que un elevado porcentaje de pacientes presentan suspensión de los farmacos cardio y nefroprotectores15,16.
Cambios en los tratamientos con iSRAA (izquierda) y ARM (derecha). Al final del estudio se consiguió el mantenimiento de la dosis de iSRAA en el 94,9 de los pacientes, pudiendo aumentar la dosis en el 1,7% y suspendiendo el tratamiento solo en el 3,4%. En el panel derecho se observa que el 83,3 de los pacientes del estudio mantuvieron la dosis de ARM y solo se suspendió en un paciente.
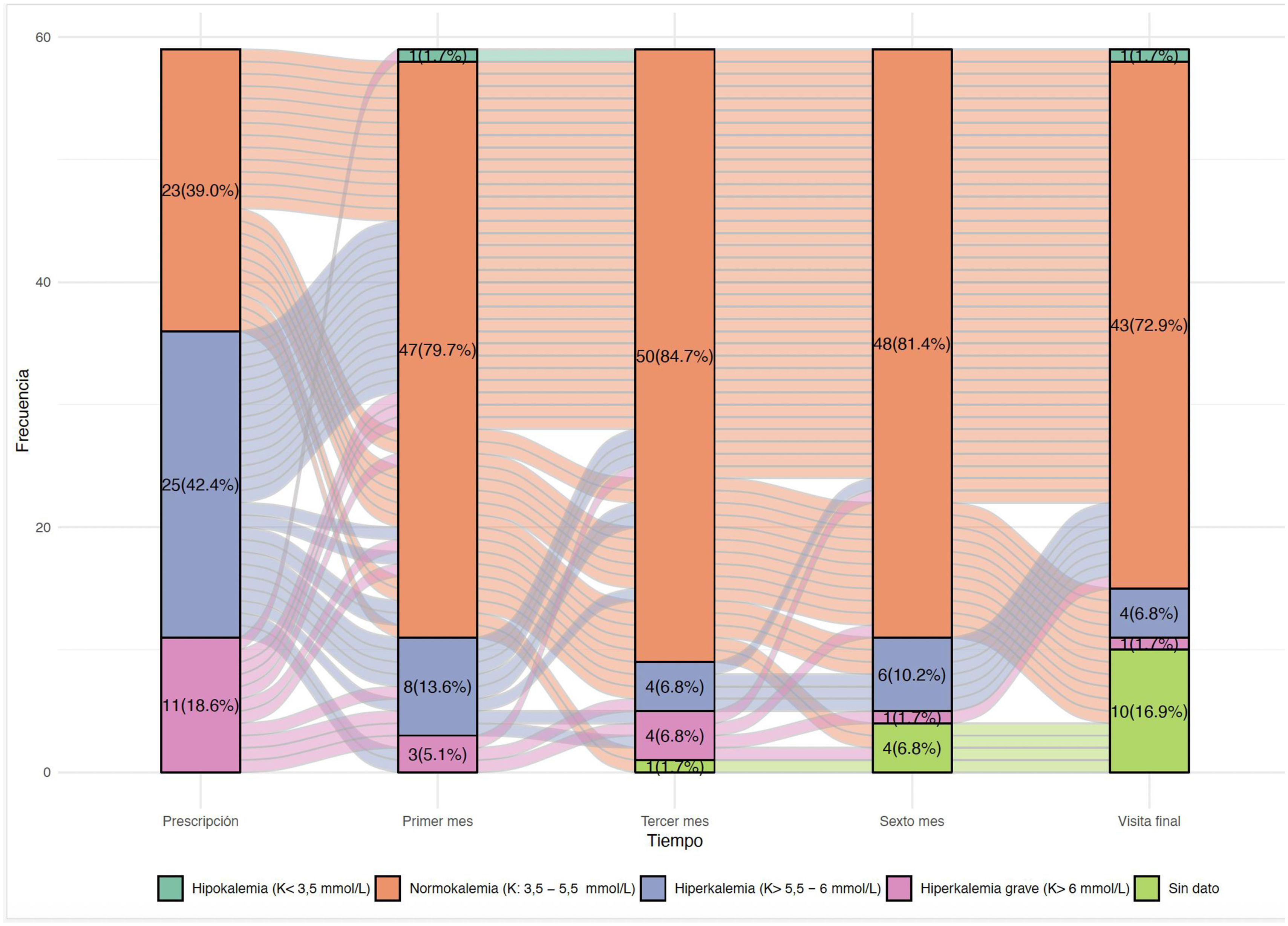
La figura 4 muestra la proporción de los rangos de potasio sérico durante las distintas visitas del estudio.
Proporción de los rangos de potasio sérico durante las distintas visitas del estudio. Rangos: <3,5 mmol/L (hipokalemia); 3,5-5,5 (normlkalemia); 5,5-6 mmol/L (hiperkalemia);> 6 mmol/L hiperkalemia grave. Sin dato: pacientes que no tenían determinación de potasio o habían finalizado el estudio por algún motivo.
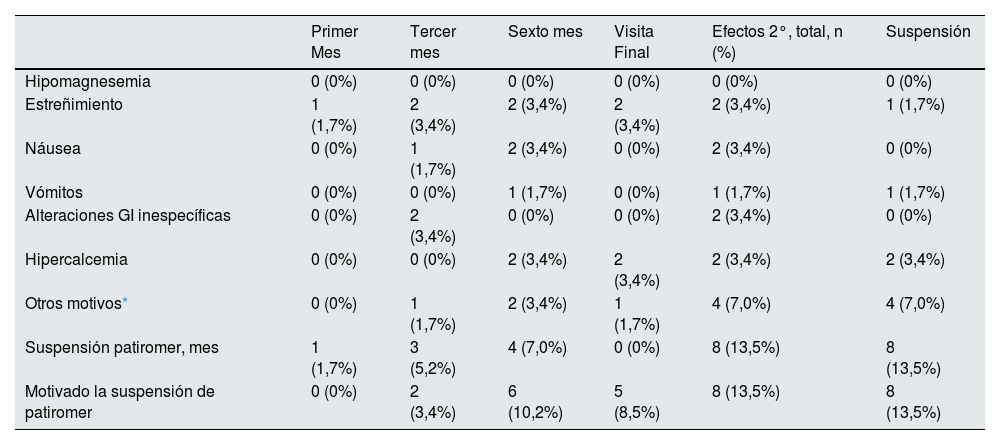
En la tabla 4 se muestran los efectos secundarios que se presentaron durante el seguimiento, el momento de la evolución en que se presentaron y si motivaron o no la suspensión del tratamiento con patirómero.
Efectos secundarios recogidos durante el seguimiento y causas de suspensión de patiromer
| Primer Mes | Tercer mes | Sexto mes | Visita Final | Efectos 2°, total, n (%) | Suspensión | |
|---|---|---|---|---|---|---|
| Hipomagnesemia | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Estreñimiento | 1 (1,7%) | 2 (3,4%) | 2 (3,4%) | 2 (3,4%) | 2 (3,4%) | 1 (1,7%) |
| Náusea | 0 (0%) | 1 (1,7%) | 2 (3,4%) | 0 (0%) | 2 (3,4%) | 0 (0%) |
| Vómitos | 0 (0%) | 0 (0%) | 1 (1,7%) | 0 (0%) | 1 (1,7%) | 1 (1,7%) |
| Alteraciones GI inespecíficas | 0 (0%) | 2 (3,4%) | 0 (0%) | 0 (0%) | 2 (3,4%) | 0 (0%) |
| Hipercalcemia | 0 (0%) | 0 (0%) | 2 (3,4%) | 2 (3,4%) | 2 (3,4%) | 2 (3,4%) |
| Otros motivos* | 0 (0%) | 1 (1,7%) | 2 (3,4%) | 1 (1,7%) | 4 (7,0%) | 4 (7,0%) |
| Suspensión patiromer, mes | 1 (1,7%) | 3 (5,2%) | 4 (7,0%) | 0 (0%) | 8 (13,5%) | 8 (13,5%) |
| Motivado la suspensión de patiromer | 0 (0%) | 2 (3,4%) | 6 (10,2%) | 5 (8,5%) | 8 (13,5%) | 8 (13,5%) |
GI: gastrointestinales.
La mayoría de los efectos adversos fueron de carácter leve y no motivaron la suspensión del fármaco. Durante el seguimiento se suspendió patirómero en 8 (13,5%) pacientes. Las causas fueron: normopotasemia mantenida con niveles de potasio en el rango bajo de la normalidad en dos casos, hipercalcemia en dos casos (decisión facultativa en ambos casos), progresión renal con necesidad de diálisis (inicio de diálisis y corrección de la HK) en un caso, falta de cumplimiento terapéutico en un caso y en alteraciones gastrointestinales en dos casos (en un caso estreñimiento y en otro vómitos).
Durante el seguimiento en el periodo del estudio, los pacientes presentaron 15 (25,4%) hospitalizaciones. Diez de ellas por causa cardiovascular y el resto por neoplasia (1), infección (1), deterioro renal con inicio de diálisis (1), hepatopatía (1) y coma hiperosmolar (1). Durante la evolución, 2 (3,4%) pacientes fallecieron, uno de ellos por causa infecciosa y otro por deterioro renal con fallo multiorgánico. En ninguno de los dos casos la HK fue la causa del fallecimiento.
DiscusiónEste estudio multicéntrico retrospectivo, realizado en condiciones de práctica clínica habitual en la Comunidad Valenciana, demuestra que el uso de patirómero en pacientes con ERC logra una reducción significativa, sostenida y clínicamente relevante del potasio sérico con un perfil de seguridad favorable. Además, se observó un alto grado de mantenimiento de las terapias con iSRAA y ARM, con buena tolerancia al tratamiento y escasa necesidad de modificación posológica o suspensión.
Nuestro trabajo aporta evidencia adicional sobre la utilidad de patirómero en práctica clínica habitual en España en medicina ambulatoria y en pacientes con indicación clara de bloqueo del SRAA y/o ARM y riesgo elevado de progresión de enfermedad renal o eventos cardiovasculares. En este contexto los datos publicados sobre la experiencia real con este fármaco son aún escasos. Independientemente de los datos de los ensayos clínicos, solo se han publicado dos estudios que hayan analizado datos de vida real del uso de patirómero en pacientes con ERC con datos específicos de eficacia en la reducción potasio y valoración de los efectos adversos. Uno de ellos en una población con ERC no en diálisis similar a la nuestra17 y estudio en población en hemodiálisis18, ambos analizando la base de datos de veteranos en los EE.UU.
Tanto en nuestro estudio como en los otros dos estudios de vida real, el uso de patirómero se asoció a una reducción significativa en las cifras de potasio sérico en la primera visita de seguimiento, siendo de - 1 mmol/L en el estudio de Kovesdy et al.17, de -1,03 mmol/L en el estudio de Pinnell et al.18 y de –0,55 a –0,71 mmol/L en el nuestro. Estos datos de reducción de potasio respecto a la basal son consistentes con los observados en los estudios AMETHYST-DN12 y OPAL-HK10.
Este efecto se alcanza en la mayoría de los casos con una dosis inicial estándar de 8,4g/día, sin necesidad frecuente de ajustes, lo que refuerza su utilidad clínica. En el estudio de Kovesdy et al.17 el 96% recibió la dosis de 8,4g/día y el 4% recibió 16,8g/día. En nuestro estudio el 86,4% recibió 8,4g/días, el 10,2% recibió 16,8g/día y el 3,4% 25,2g/día. En el estudio de Pinnel et al, al tratarse de pacientes en hemodiálisis, las dosis fueron más variables, pero solo el 15,3% recibieron más de 8,4g/día. El 69% recibió 8,4g/día y el resto recibió dosis menores al recibir tratamientos días alternos.
Los datos de porcentaje de comorbilidades de los pacientes de los tres estudios fueron muy similares, pero nuestro estudio muestra una población más envejecida (73,8 años en nuestro estudio vs. 70 y 66 años de media en los otros dos estudios de vida real). Este aspecto refuerza la aplicabilidad de nuestros resultados a escenarios asistenciales reales.
Es de destacar en nuestro estudio que la terapia con iSRAA y ARM se mantuvo en el 94,9% y 96,3% de los pacientes, respectivamente. Este dato contrasta de forma positiva con series retrospectivas como la de Trevisan que analizó 36.011 pacientes con ERC estadios 3-5, donde la HK motivó la suspensión del tratamiento bloqueador en más del 30% de los casos19.
Tanto nuestro estudio como el de Kovesdy et al.17, presentan una baja tasa de discontinuación del tratamiento con patirómero (13,5% y 20%, respectivamente), que contrasta con la elevada tasa de discontinuación en el estudio que analizó pacientes en hemodiálisis, que alcanzó el 50% a pesar de una reducción media sostenida de potasio de 1 mmol/L. Esto último puede estar relacionado con los importantes cambios en la kalemia en los pacientes en hemodiálisis, muchos de ellos influidos por la de dosis de diálisis entre otros factores que hacen la normalización de la HK sea rápida incluso pudiendo presentar hipopotasemia. El criterio de inclusión de nuestro estudio de estar recibiendo al menos tres meses patirómero puede haber excluido aquellos pacientes con suspensión precoz del tratamiento. La contribución de patirómero al mantenimiento de terapias nefroprotectoras de base es especialmente relevante en este contexto, donde la supresión de iSRAA/ARM representa una causa frecuente de progresión de la enfermedad renal16,19.
La seguridad es un aspecto de gran relevancia en los tratamientos con quelantes o intercambiadores del potasio, donde los efectos secundarios, especialmente gastrointestinales han limitado el uso de fármacos cardio y nefroprotectores con sus implicaciones en la morbimortalidad y progresión renal de los pacientes con ERC20 donde el uso de polestireno sulfonato cálcico o sódico ha presentado un uso limitado por su escasa efectividad y problemas relacionados con la seguridad21. Los principales efectos secundarios descritos en los estudios pivotales con patirómero (AMETHYST-DN12 y OPAL-HK10) han sido estreñimiento (4,6-11%), diarrea 2,7 -5%, hipomagnesemia hasta el 7,2% y otros efectos secundarios gastrointestinales menores como náuseas y dolor abdominal en el 2-4%. En nuestro estudio la presencia de efectos secundarios gastrointestinales fue menor que la descrita en los ensayos pivotales, dato que puede estar influido por la naturaleza retrospectiva del análisis. No se detectaron casos de hipomagnesemia, a pesar de que en la mayoría de los pacientes se monitoriza el magnesio en los seguimientos en nefrología.
Por una parte, llama la atención la detección de dos casos de hipercalcemia, que, aunque fue leve, motivó la suspensión de patirómero. Aunque la hipercalcemia no fue destacada en los ensayos pivotales con patirómero, se han descrito algunos casos clínicos de carácter aislado con esta complicación, especialmente en pacientes con ERC avanzada22–24.
El mecanismo propuesto se basa en las propiedades intercambiadoras de iones del propio fármaco: patirómero (patirómero cálcico) libera calcio al unirse al potasio en el lumen intestinal, lo que puede incrementar la absorción sistémica de calcio en pacientes susceptibles, especialmente con filtrado glomerular reducido en los que la eliminación urinaria de calcio está comprometida, lo que favorece su acumulación. Pueden asociarse otros factores como el uso de diuréticos tiazídicos, hiperparatiroidismo secundario y la suplementación con vitamina D, que puede aumentar la absorción de calcio. En los casos publicados, la hipercalcemia se resolvió al suspender patirómero y recidivó al reintroducirlo. Aunque infrecuente, este efecto adverso debe considerarse y monitorizarse el calcio sérico en tratamientos prolongados22–24.
Igualmente llama la atención en nuestro estudio que la mayoría de las discontinuaciones de los tratamientos no fueron debidas per se a efectos secundarios, sino a otras situaciones como el deterioro renal con inicio de diálisis, falta de cumplimiento por parte del paciente o suspensión por parte del médico por presencia de normokalemia. Todo esto hace que la prevalencia real de suspensión de patirómero por efectos secundarios adversos, sea realmente menor de la reportada, siendo pues, la mayoría de los efectos secundarios de carácter leve y que no motivaron la suspensión del tratamiento, con reforzamiento de la tolerancia del fármaco.
Nuestro estudio presenta bastantes limitaciones. Una de ellas es la inherente a su diseño retrospectivo y observacional, lo que impide establecer relaciones causales firmes entre el uso de patirómero y los cambios observados en el potasio sérico o en la continuidad del tratamiento con iSRAA/ARM, asi como la posible omisión de alguno de los efectos adversos, especialmente los de carácter leve al no estar reportados en la historia clínica. En segundo lugar, el tamaño muestral relativamente limitado (59 pacientes) podría restringir la generalización de los hallazgos, en comparación con estudios previos con mayor volumen poblacional, como el de Kovesdy et al.17 (n=288) o Pinnell et al.18 (n=458). Aun así, se trata de una cohorte representativa del paciente nefrológico ambulatorio con ERC avanzada, lo que otorga valor clínico y aplicabilidad a los hallazgos. Otra limitación es la ausencia de un grupo control, situación que impide establecer relaciones causales directas entre el tratamiento con patirómero y la evolución de los niveles de potasio. Aunque se observaron reducciones significativas y sostenidas del potasio sérico, no puede descartarse la influencia de otros factores concomitantes, como ajustes dietéticos, cambios en la medicación o variabilidad clínica espontánea, que puedan haber contribuido al efecto observado.
A pesar de estas limitaciones, el estudio presenta varias fortalezas relevantes. En primer lugar, ofrece una evaluación detallada de la seguridad de patirómero en condiciones de práctica clínica habitual, recogiendo los efectos adversos de los pacientes. Además, el seguimiento prolongado con una mediana de 12 meses, que permite no solo valorar la eficacia inicial, sino también la persistencia terapéutica y la estabilidad del control del potasio a largo plazo, aportando información de gran utilidad para la toma de decisiones clínicas.
Finalmente, conviene destacar que se trata de uno de los primeros estudios realizados en Europa en el contexto del paciente ambulatorio con ERC y síndrome cardiorrenal tratados con patirómero, lo que contribuye a ampliar la evidencia disponible y apoya su implementación en la práctica nefrológica en nuestro entorno.
Nos gustaría destacar que la mayoría de los centros participantes formaban parte de Unidades Cardiorrenales donde existe un abordaje más integrado y alineado con las guías clínicas. Desde un punto de vista clínico, los resultados refuerzan la utilidad de patirómero como herramienta para facilitar un abordaje integral de la enfermedad cardiorrenal. Su uso puede evitar decisiones terapéuticas forzadas, como la reducción o supresión del bloqueo del eje renina-angiotensina en pacientes que podrían beneficiarse de estos tratamientos, especialmente en estadios avanzados de ERC donde el margen terapéutico es limitado. Esta estrategia está en línea con las recomendaciones actuales de las guías KDIGO y de IC, que subrayan la importancia de mantener el tratamiento optimizado siempre que sea posible4,25,26, en este caso mediante el uso de patirómero. Además de las recomendaciones de las guías, el uso de patirómero en HK de la ERC o de la IC se ha asociado a una reducción de los costes generando un ahorro anual entre 3.127 y 3.466 € por paciente27.
Debe tenerse en cuenta que la financiación no siempre se corresponde con la indicación clínica. En España, patiromer está reembolsado solo en pacientes con ERC avanzada e IC grado III-IV con HK leve-moderada (5,5–6,4 mmol/L), en tratamiento con inhibidores del SRAA cuya continuación sea imprescindible y con fracaso o intolerancia a resinas de intercambio iónico. Dado que los criterios de financiación difieren entre países y sistemas sanitarios, la generalización de nuestros resultados puede ser limitada.
Creemos que los nuevos intercambiadores de potasio, en este caso patirómero, podría jugar un papel preventivo en la estabilización del potasio y facilitar el mantenimiento de fármacos cardiorrenales, incluso antes de episodios de HK grave. En este sentido, sería deseable contar con estudios prospectivos diseñados específicamente para evaluar el impacto clínico de esta estrategia.
En conclusión, este estudio proporciona evidencia real sobre la eficacia, seguridad y utilidad de patirómero en pacientes con ERC e HK tratados en condiciones habituales. Su capacidad para reducir y estabilizar el potasio sérico de forma sostenida, junto con su buen perfil de tolerancia y su contribución al mantenimiento del tratamiento con iSRAA y ARM, lo posicionan como una herramienta valiosa en la nefroprotección. En este sentido, sería deseable contar con estudios prospectivos diseñados específicamente para evaluar el impacto clínico de esta estrategia.
FinanciaciónEste es un estudio iniciado por investigadores, patrocinado por una subvención sin restricciones de CSL VIFOR FARMA. La ayuda para el estudio se ha realizado a través del Instituto de Investigación INCLIVA del hospital Clínico Universitario de Valencia. El diseño del estudio ha sido realizado por los autores. CSL VIFOR no ha intervenido ni en el diseño del estudio mi en la realización del manuscrito.
Conflictos de interesesBGC declara haber recibido honorarios por ponencias de CSL VIFOR, AstraZeneca y Laboratorios Rubió. JPS declara haber recibido honorarios por ponencias de CSL VIFOR y de AstraZeneca. MS declara haber recibido honorarios por ponencias AstraZeneca. PSP ha recibido ayuda de CSL VIFOR para asistencia a congresos. JP declara haber recibido honorarios por ponencias AstraZeneca. MJP declara haber recibido honorarios por ponencias AstraZeneca y CSL VIFOR, ayudas para asistencia a congresos de CSL VIFOR y ayudas para investigación a través del Instituto de investigación INCLIVA. RGM declara haber recibido honorarios por ponencias AstraZeneca y ayudas para asistencia a congresos de CSL VIFOR, y colaboración de Laboratorios Rubió. RDLE declara haber recibido honorarios por ponencias de Astrazeneca y CSL VIFOR, honorarios por asesorías y ayudas para la investigación de Astrazeneca.
JN declara haber recibido honorarios por ponencias de Astrazeneca y CSL VIFOR, honorarios por asesorías y ayudas para la investigación de Astrazeneca (a través del instituto de investigación INCLIVA). JLG declara haber recibido honorarios por ponencias y por asesorías de CSL VIFOR y Astrazeneca, así como ahudas a la investigación a través del instituto de investigación INCLIVA. FMF, JACA, EGC declaran no tener conflicto de intereses en este proyecto.