Introducción La preeclampsia (PE) es una importante causa de morbimortalidad fetal, que en el mundo occidental afecta al 2-7% de los embarazos y es responsable de 50.000 muertes anuales. La detección precoz es prioritaria, ya que puede cambiar su curso clínico, pero no se dispone de biomarcadores ni métodos instrumentales de alta sensibilidad y especificidad, solamente el índice hiperbárico tiene una sensibilidad y una especificidad del 99% para la identificación precoz de las gestantes en riesgo de desarrollo de PE, pero está escasamente difundido.
ObjetivoValorar la utilidad del índice hiperbárico en la prevención primaria de las complicaciones hipertensivas del embarazo en un área sanitaria.
Material y métodosEstudio retrospectivo realizado entre los embarazos habidos en nuestra área durante el periodo 2007-2012 (N=11.784). El diagnóstico se estableció mediante el índice hiperbárico y las gestantes en riesgo fueron tratadas con AAS nocturno.
ResultadosEn las gestantes remitidas a consulta de Nefrología (38,2%), diagnosticadas de alto riesgo de PE y tratadas con AAS 100mg nocturno (desde la semana 17) se redujo la incidencia de episodios de PE un 96,94%.
Preeclampsia (PE) is a major cause of fetal morbidity and mortality. In the Western World, PE affects 2-7% of pregnancies and is responsible for 50,000 deaths annually. Early detection is a priority as it can change the clinical course, but there are no biomarkers or instrumental methods with high sensitivity and specificity. Only the hyperbaric index has a sensitivity and specificity of 99% for early identification of pregnant women at risk of developing PE, but its use is not widespread.
ObjectiveTo assess the usefulness of the hyperbaric index in the primary prevention of hypertensive pregnancy complications in a public healthcare area.
Material and methodsThis is a retrospective study of pregnancies that occurred in our area during the period 2007-2012 (N=11,784). The diagnosis was established by the hyperbaric index and pregnant women at risk were treated with ASA at night.
ResultsIn pregnant patients referred to the nephrology clinic (38.2%), diagnosed as high-risk for PE, and treated with 100mg ASA/night (from week 17), the incidence of PE episodes was reduced by 96.94%
La hipertensión arterial (HTA) es la complicación médica más habitual del embarazo, y la preeclampsia (PE) es una importante causa de morbimortalidad fetal (bajo peso al nacer, o prematuridad), pudiendo variar las complicaciones maternas desde el fracaso renal agudo, el síndrome de HELLP, el fallo hepático o el edema cerebral, hasta convulsiones o muerte1. La PE en el mundo occidental afecta al 2-7% de todos los embarazos, y el fenómeno patogénico básico es la disfunción endotelial condicionada por un «disbalance» de factores angiogénicos que producen anomalías de la placentación e isquemia placentaria. No es un proceso limitado que se resuelve con el parto, ya que la disfunción endotelial puede persistir y convertirse en un factor de riesgo cardiovascular futuro2.
El objetivo, por tanto, es el diagnóstico precoz de la PE, pero los factores angiogénicos no tienen la sensibilidad y la especificidad necesarias para su uso en la clínica diaria3,4. Tampoco la hiperuricemia, aunque algunos autores la relacionaron con la severidad y la precocidad de la PE; 2 recientes revisiones sistemáticas concluyen no solo que no existe evidencia suficiente que correlacione la hiperuricemia con la PE5, sino que además el ácido úrico en un pobre predictor de las complicaciones maternofetales6. En nuestra experiencia, y utilizando el índice hiperbárico (IHB) como «gold standard», factores de riesgo como ser primigesta añosa, el uso de anticonceptivos orales o tener antecedentes familiares de HTA son predictivos de PE7.
Entre los métodos «instrumentales», los expertos no recomiendan el ecodoppler de arteria uterina8, pero el IHB o área de exceso de presión arterial (PA) por encima del límite superior del intervalo de tolerancia tiene una sensibilidad y una especificidad del 99% para la identificación precoz de las gestantes en riesgo de desarrollo de PE9; solamente la determinación de serpina1 por proteómica urinaria10 o la evaluación de podocituria tienen una sensibilidad y una especificidad del 100%11. Una vez detectada, la administración precoz y nocturna de AAS12 y vitamina D reduce de forma significativa su riesgo13.
En conclusión, el diagnóstico se establece, además de mediante los factores de riesgo convencionales, con un IHB>12, y la prevención primaria es con AAS a dosis altas, entre 100-300mg, nocturno, y antes de la semana 17 reduce de forma significativa el riesgo de las complicaciones hipertensivas del embarazo.
Valorar la utilidad del IHB en la prevención primaria del desarrollo de PE en nuestra área sanitaria.
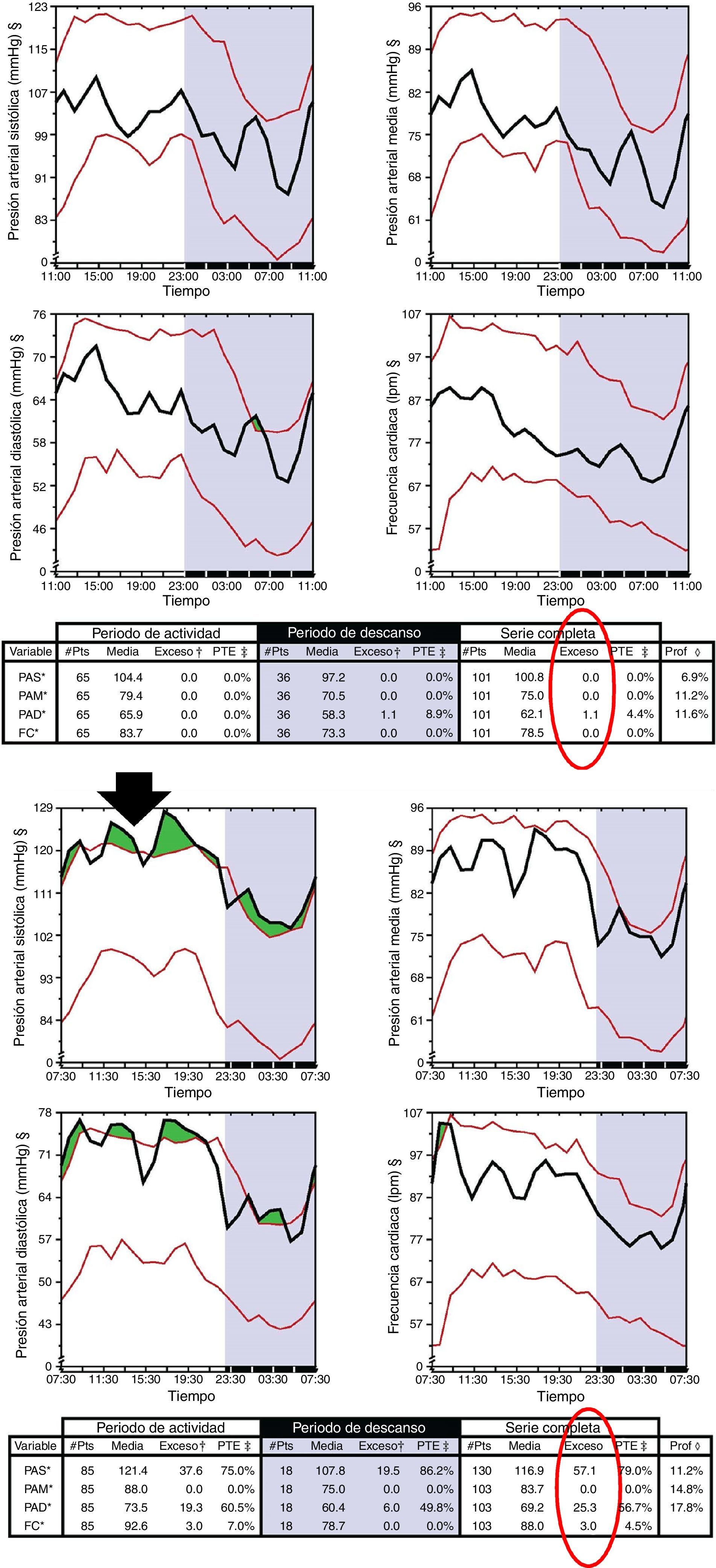
Material y métodosEstudio retrospectivo realizado entre los embarazos seguidos en nuestra área durante el periodo 2007-2012 (N=11.784). Se revisó la incidencia de PE en la población gestante de las consultas de alto riesgo (AR) y «no AR» de los 3 hospitales del área (Complejo Hospitalario Universitario de Ourense [CHUOU]), Hospital Comarcal [HC] de Verín y HC de Valdeorras) y entre aquellas gestantes que fueron derivadas por AR a la Consulta de Nefrología (CN). A las gestantes remitidas a la CN (antes de la semana 17 de gestación) se les realizó una monitorización ambulatoria de la PA de 48h mediante monitor Spacelab 92007. Se consideró el IHB>12 como marcador de riesgo de PE (fig. 1), y las gestantes con IHB patológico fueron tratadas con AAS 100mg nocturno y suplementos de vitamina D si existía deficiencia. Estas gestantes fueron seguidas durante todo el embarazo en la CN.
Se consideró gestantes de AR a las que cumplían alguno de los criterios siguientes: primigesta añosa, obesidad mórbida, PE previa, diabetes mellitus, HTA, enfermedad sistémica (LED, síndrome antifosfolipídico), cardiopatía, antecedentes familiares de enfermedad cardiovascular, tabaquismo, embarazo gemelar o uso de anticonceptivos orales.
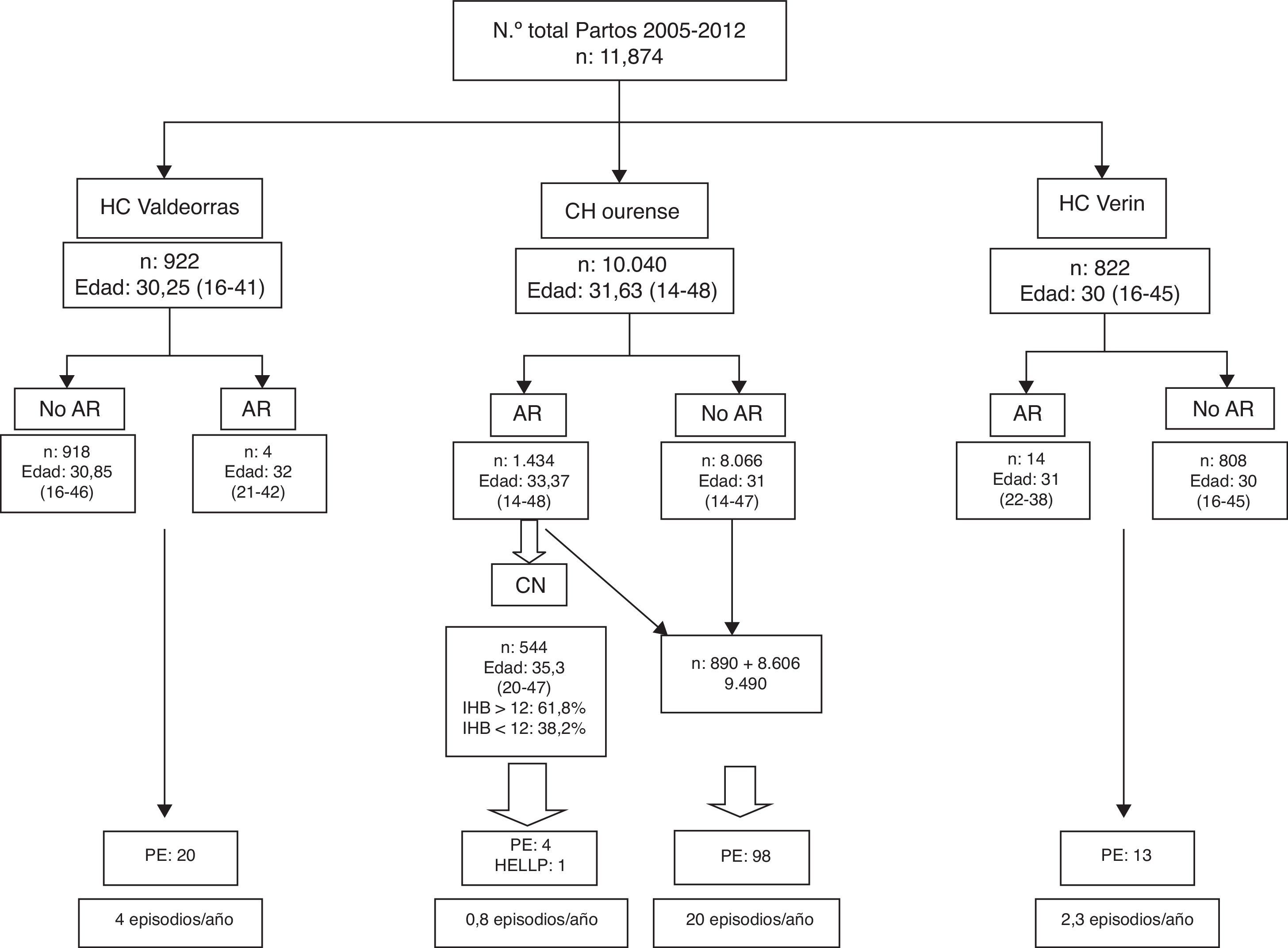
ResultadosEl número total de partos durante el periodo 2005-2012 fue de 11.784 (fig. 2), de los cuales el 85,20% corresponden al CHUOU, el 7,82% al HC de Valdeorras y el 6,91% al HC de Verín, y la media de edad de las gestantes osciló entre 30 y 31,63 años (fig. 2). La derivación desde la consulta de Obstetricia a sus consultas de AR fue excepcional en los centros comarcales: 0,4% en el HC de Valdeorras y 1,70% en el HC de Verín, mientras que en el CHUOU el porcentaje de derivación fue de un 14,28%. De estas gestantes, fueron remitidas a la CN solamente el 34,93%, y de ellas, el 61,8% tenían un IHB>12; en el 32,8%, el IHB fue normal.
La incidencia de PE fue de 4 episodios/año en el HC de Valdeorras y 2,3 episodios/año en el HC de Verín. En el CHUOU, entre las gestantes «no remitidas» a la CN, la tasa de PE fue de 20 episodios/año, mientras que entre aquellas que fueron atendidas en la CN, la incidencia de PE fue de 0,8 episodios/año, que corresponden a 4 gestantes, 2 de ellas con LED, la tercera era intolerante a AAS y la cuarta desarrolló un síndrome de HELLP.
DiscusiónLa PE es un síndrome definido por HTA y proteinuria después de la semana 20 de gestación, en embarazadas previamente sin HTA ni proteinuria, y en el mundo occidental afecta al 2-7% de todos los embarazos, aunque en otras áreas geográficas esta cifra se puede triplicar14. La mortalidad es del 10-15%, y aproximadamente es responsable de 50.000 muertes anuales, por lo que su detección precoz es prioritaria y podría cambiar su curso clínico.
El mecanismo básico es un defecto de implantación de la placenta. En el embarazo normal, el citotrofoblasto suprarregula la expresión de metaloproteinasas, promoviendo la transformación de epitelio en endotelio, y este proceso está controlado por el factor de crecimiento vascular (VEGF), el factor de crecimiento placentario (PIGF) y la angiopoyetina.
En la PE, sFlt-1, factor circulante antiangiogénico, está incrementado en la placenta y en el suero, se adhiere al PIGF y al VEGF e inhibe la interacción con sus receptores endoteliales (FIt1); en consecuencia, también se activa NOSe y se produce estrés oxidativo e isquemia placentaria. En la PE se comienza a elevar entre las semanas 9 y 11, y PIGF desciende durante ese mismo periodo, antes del inicio de la PE15.
Otros factores implicados en el desarrollo de PE, además de la angiopoyetina16, son las bajas tasas de oxígeno, la resistencia a la insulina17 y la deficiencia de vitamina D. Esta regula el VEGF18, y en la PE, la deficiencia-insuficiencia de vitamina D contribuye a la disfunción endotelial y al desarrollo de HTA. Finalmente, las anomalías de la placenta en la madre condicionan, entre otros problemas, el aumento de las resistencias periféricas debido a la acción de anticuerpos agonistas de AT119 y a la elevada tasa de endoglina, correceptor de TGF B1 y TGF B3, que actúa como una potente proteína antiangiogénica, «secuestrando» el PIGF y el VEGF.
Paradójicamente ninguno de estos factores tienen la sensibilidad-especificidad y disponibilidad necesaria para su aplicación clínica3 en el diagnóstico precoz de la PE, como tampoco los factores de riesgo vascular convencionales5,6 o los métodos instrumentales8, excepto la PA. Clásicamente se consideraba que la PA en etapas precoces del embarazo podría servir de detección de PE, pero la mayor aproximación era cuando la PA media superaba los 90mmHg, pero su valor predictivo era bajo20. Estos pobres resultados de la medida estática de la PA eran consecuencia de utilizar el umbral que define la HTA esencial. Es bien conocido que el patrón de PA en mujeres con PE o HTA es diferente y predecible; así, las diferencias de PA entre una embarazada normotensa y una embarazada con complicaciones (PE o HTA gestacional) son detectadas desde el primer trimestre con diferencias significativas en el MESOR circadiano de PA sistólica (12mmHg) y diastólica (7mmHg). Por tanto, la «cuantificación» del «exceso» del umbral de PA o IHB, con una sensibilidad-especificidad del 99%, nos permite detectar a aquellas gestantes en riesgo de desarrollar PE9.
En nuestra serie, el IHB fue patológico en el 61,9% de las gestantes remitidas desde AR, mientras que el 38,2% fue normal, lo cual indica que el IHB discrimina más que los criterios de AR convencionales9. Se identificó «precozmente» a las gestantes en riesgo elevado de PE, y con tratamiento, se redujo su incidencia de 26,3 a 0,8 episodios/año, principalmente en el CHUOU, del que recibimos al 34% de las gestantes de AR. De los 2 HC no recibimos ninguna gestante de AR, y mantuvieron una tasa de PE similar a la de las áreas donde no existe prevención primaria14. Los protocolos son comunes y posiblemente esta situación sea consecuencia de la «inercia clínica».
Como consecuencia del daño isquémico placentario en la PE, se produce una activación de las plaquetas y del sistema de coagulación que induce un disbalance entre la síntesis de prostaciclinas y la de tromboxano A2. En función de ello surgieron múltiples estudios para valorar la utilidad de los agentes antiagregantes en la prevención primaria de la PE, pero los primeros resultados fueron desalentadores21–23, aunque un informe de revisión24 muestra cómo el uso de antiplaquetarios reduce el riesgo de PE un 17%. Todos estos estudios tienen un problema metodológico: la dosis de AAS y el momento de su administración. Diferentes estudios demostraron que las dosis de 100-150mg/dl de AAS son eficaces en comparación con dosis más bajas (50 a 80mg/dl)25 y que se debe administrar antes de la semana 17 y por la noche12, habida cuenta de que la inhibición de la síntesis de tromboxano A2 por AAS es dependiente de la dosis y administrada por la noche. En consecuencia, todas las gestantes remitidas a CN (34,92%) y con un IHB>12 (61,8%) (fig. 2) fueron tratadas con AAS 100mg nocturno durante todo el embarazo, y la incidencia de episodios de PE se redujo un 96,94%.
En conclusión, la colaboración de la CN en la prevención primaria de las complicaciones de la HTA del embarazo y a través de la metodología diagnóstica de IHB es altamente eficiente, por lo que debería ser una prestación asistencial rutinaria entre las consultas de embarazo de AR y Nefrología.
Conflicto de interesesNo existe conflicto de intereses.