INTRODUCCIÓN
En España, en el año 2013, el porcentaje de pacientes con injerto funcionante fue del 52% del total de pacientes con tratamiento renal sustitutivo. Este porcentaje se ha incrementado paulatinamente de forma que en el año 2000 los pacientes con trasplante renal representaban solo el 42% y, considerando el incremento anual del número de trasplantes renales, es de suponer que este porcentaje seguirá aumentando en los años venideros1.
La inmunosupresión del paciente trasplantado renal ha sido y sigue siendo el pilar básico para mantener el injerto funcionante y ha evolucionado de manera notable desde los inicios del trasplante renal. Sin embargo, los fármacos inmunosupresores no están exentos de efectos secundarios y la monitorización de estos fármacos mediante medición de niveles en la sangre o la determinación directa o indirecta de su acción farmacológica es importante para mantener el delicado equilibrio entre su acción inmunosupresora y sus efectos adversos.
El clínico que usa habitualmente estos fármacos necesita herramientas que le ayuden a utilizarlos de manera adecuada en cada individuo y por ello el grupo Prometeo realizó en el año 2015 una revisión de la monitorización de los aspectos inmunológicos, histológicos y farmacológicos del trasplante renal.
En el presente artículo, se revisa la situación actual de la monitorización farmacológica de los inmunosupresores, realizando, para cada uno de ellos, una breve introducción de su metabolismo y mecanismo de acción.
METODOLOGÍA
La metodología ha sido la habitual del grupo Prometeo:
a) Revisión bibliográfica en PubMed, Medline, Cochrane Database of Systematic Reviews, etc., con las siguientes palabras clave para cada inmunosupresor: niveles, AUC, farmacocinética.
b) Selección bibliográfica según criterios de calidad metodológica, antigüedad de la publicación y cobertura de los diferentes aspectos del tema revisado, realizando finalmente una selección de 73 artículos.
c) Revisión bibliográfica por los miembros del grupo.
d) Debate en el grupo y recogida final de evidencias en un consenso valorado según la escala GRADE (por sus siglas en ingles, grading of recommendations assessment, development, and evaluation).
GLOSARIO DE TÉRMINOS
AUC (area under the curve o área bajo la curva): es un parámetro farmacocinético que refleja la cantidad total de fármaco que alcanza la circulación sistémica. Es la medida más importante de la biodisponibilidad y relaciona las variaciones de la concentración plasmática de un fármaco en función del tiempo. Se determina mediante una función integral de las concentraciones plasmáticas en distintos puntos.
C0: concentración en niveles valle. Habitualmente a las 12 horas de la toma del fármaco.
C2: determinación a las dos horas de la toma del fármaco. No tiene por qué coincidir con la concentración máxima.
Cmax: máximo nivel alcanzado tras la toma oral.
AZATIOPRINA
Es un derivado imidazólico de la 6-mercaptopurina, que bloquea el metabolismo de las purinas. Tiene una biodisponibilidad cercana al 50% y se ha usado desde los inicios del trasplante renal en inmunosupresión doble asociada a prednisona y, más tarde, en inmunosupresión triple asociada a ciclosporina.
Es un fármaco inmunosupresor clásico que prácticamente no se indica de novo en los protocolos de inmunospresión actual. Desde sus inicios en trasplante renal, se ha utilizado sin monitorizar su acción farmacológica; sin embargo, se han descrito varias dianas de monitorización terapéutica en distintas patologías, entre ellas en trasplante renal. Las dianas de monitorización farmacológica a las que nos referimos son la actividad de la tioguanina metiltransferasa en hematíes y la tiopurina metiltransferasa, también en hematíes. La actividad de esta última depende de su expresión génica, que tiene cuatro fenotipos distintos y que también puede ser monitorizada2-4.
En la tabla 1 se resumen los datos publicados recientemente en trasplante renal.
Como se puede comprobar, los estudios realizados midiendo la actividad de las dos enzimas son observacionales, están realizados con escaso número de pacientes y, aunque se ha descrito una cierta relación con la incidencia de rechazo agudo, los datos publicados son insuficientes, en algunos estudios, contradictorios y aportan escaso nivel de evidencia científica, por lo que no recomendamos la monitorización sistemática de la azatioprina en el trasplante renal. En otras enfermedades como la enfermedad de Crohn, leucemia etc., se ha utilizado la expresión de los genes que regulan la actividad de la tiopurina metiltransferasa para identificar la falta de adherencia, predecir mielotoxicidad y evaluar la resistencia terapéutica5.
ANTICALCINEURÍNICOS
Ciclosporina en microemulsión
La ciclosporina es un fármaco lipofílico que se introdujo en el ámbito del trasplante renal en la década de los ochenta. Actúa como un profármaco que se activa al unirse a un receptor intracelular (la inmunofilina) e inhibe la actividad fosfatasa de la calcineurina. Tiene una biodisponibilidad variable y se metaboliza por el citocromo P450. Cuando se comenzó a utilizar en el campo del trasplante renal supuso un auténtico avance, puesto que se redujo de manera notable la tasa de rechazo agudo6,7.
A mediados de los noventa se introdujo una modificación en la formulación de la ciclosporina que se presentó en forma de microgotas (ciclosporina neoral), lo que aumentó su biodisponibilidad y redujo la variabilidad farmacocinética y los inconvenientes derivados de su administración oral. Desde entonces, es la formulación de ciclosporina de uso convencional.
Con respecto a la monitorización farmacológica de la ciclosporina en microemulsión, los ensayos clínicos que incluyen estudios de farmacocinética (que se han realizado siempre en los 3 primeros meses postrasplante) concluyen lo siguiente:
– El AUC a las 12 horas es un buen predictor de rechazo agudo y de pérdida del injerto.
– La Cmax se correlaciona bien con su efecto inmunosupresor.
– Las primeras 4 horas tras la toma del fármaco son las de mayor variabilidad intraindividual, por lo que la determinación del AUC a las 4 horas se correlaciona bien con el AUC a las 12 horas.
– La C2 predice mejor que la C0 el AUC a las 4 horas.
Como consecuencia de estos estudios, a finales de los noventa y a comienzos de la década del 2000, diversos grupos, como el comité de expertos de Vancouver, el grupo de consenso internacional y el grupo de expertos europeos, recomendaron la utilización de la C2 para monitorizar clínicamente la ciclosporina neoral8-12.
Sin embargo, la utilización de la C2 solo está respaldada por la evidencia en ensayos clínicos en el postrasplante inmediato, a lo que se unen varios inconvenientes de índole práctica, puesto que los niveles bajos de C2 no permiten discernir entre los pacientes que adsorben lentamente la ciclosporina, los que la adsorben poco o los que tienen baja dosificación del fármaco, por lo que si un paciente tiene niveles bajos, requiere una determinación adicional para conocer su situación y tomar una decisión terapéutica. Además, solo hay 15 minutos de margen para la extracción, que debe hacerse siempre entre los 105 y los 135 minutos después de la toma de la dosis por la mañana.
Estos inconvenientes, unidos a la falta de evidencia de monitorización de la C2 en el trasplante tardío y a la aparición posterior de algunos estudios observacionales contradictorios, han llevado a su abandono progresivo. Más aún, los ensayos clínicos posteriores se han basado en la monitorización de la C0, que es la que se usa actualmente13-15.
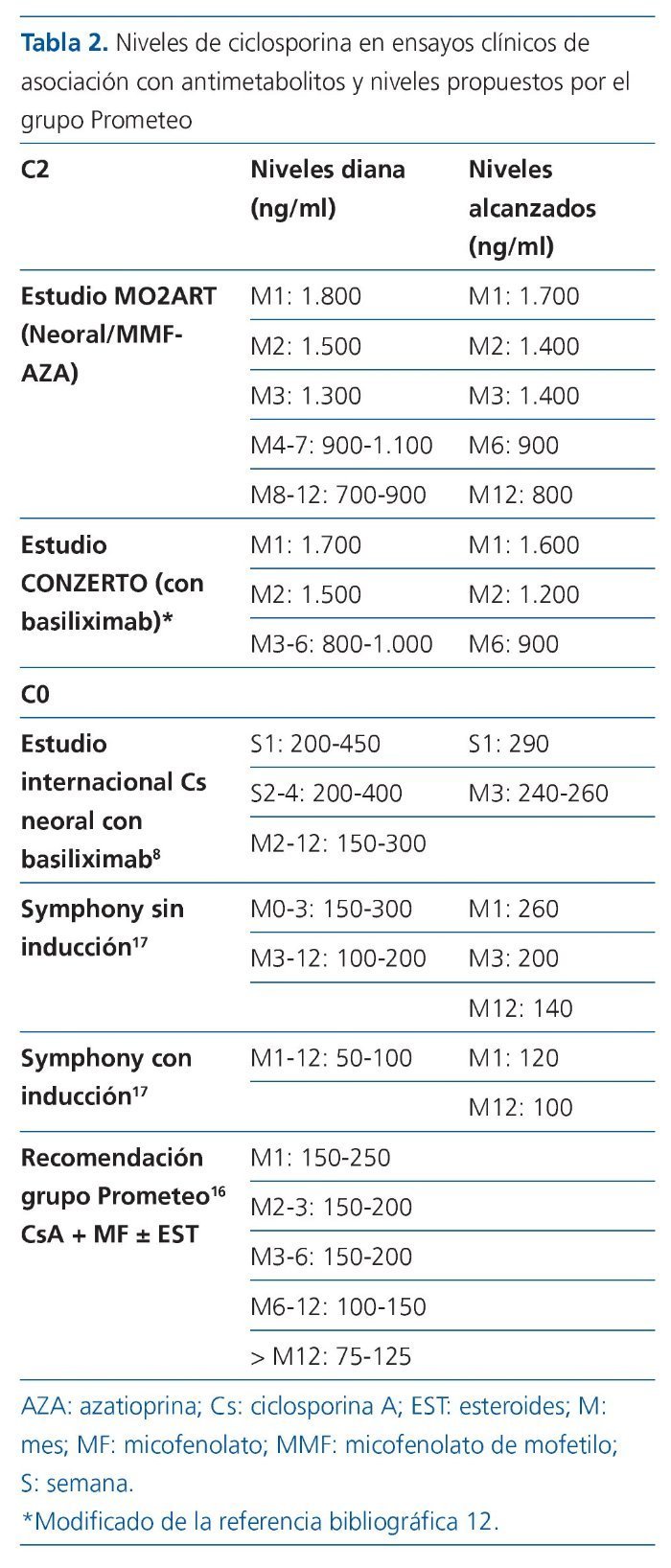
En la tabla 2 se muestran los niveles de C2 y de C0 empleados en distintos ensayos cuando se han usado asociadas a antimetabolitos. Además, en dicha tabla se incluyen las recomendaciones sobre los niveles de ciclosporina realizadas por el grupo Prometeo, que analizó la influencia de la inmunosupresión en la función renal y que han sido recientemente publicadas16. En cuanto a los niveles terapéuticos que se deben utilizar en asociación con antimetabolitos, es de gran importancia conocer los niveles empleados en el estudio Symphony durante el postrasplante inmediato y en el primer año postrasplante17.
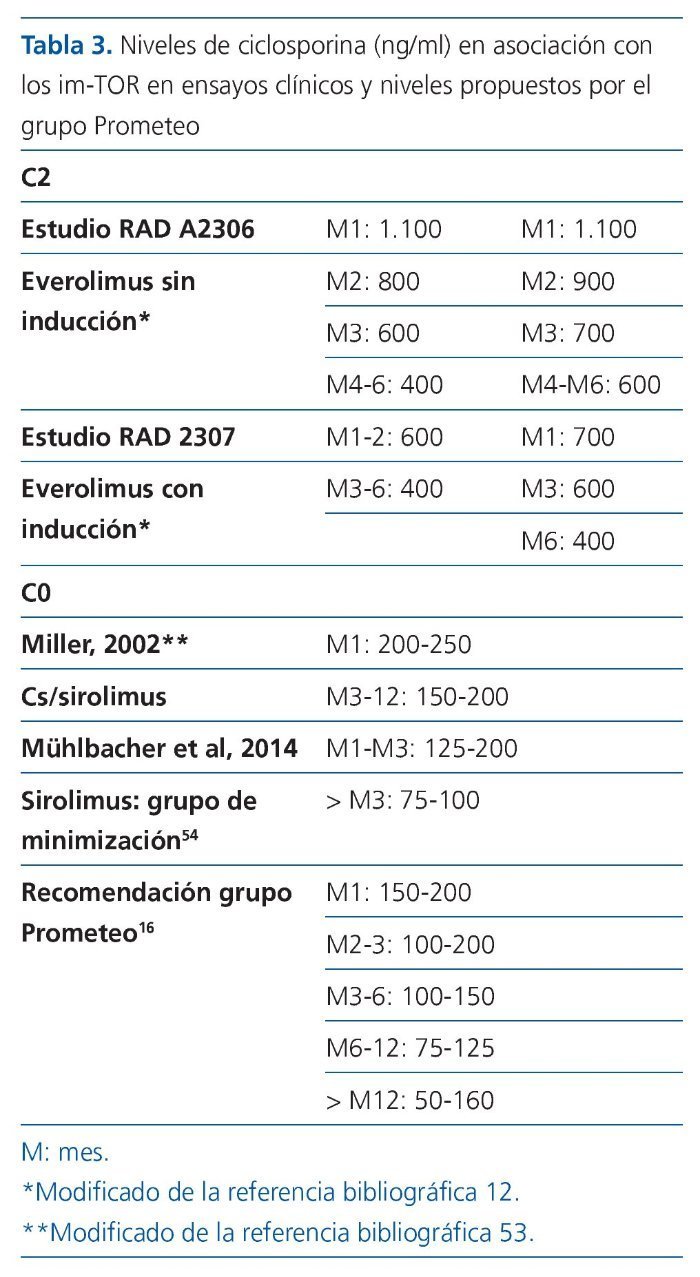
En la tabla 3 se muestran los niveles en asociación con los inhibidores de la diana de la rapamicina en mamíferos (m-TOR por sus siglas en inglés, mammalian target of rapamycin), los im-TOR.
Como se puede observar en dicha tabla, los niveles de ciclosporina de inicio eran más elevados que los actuales. Esta tendencia es común desde el inicio de la ciclosporina y viene refrendada por el metaanálisis realizado por Sharif que compara el rechazo agudo y la supervivencia de pacientes e injerto en estrategias de minimización asociando anticalcineurínicos con micofenolato de mofetilo (MMF) e im-TOR o usándolos en asociación con esteroides, y concluye textualmente: «Las estrategias de reducción de anticalcineurínicos se asocian con menos función renal retrasada, mejoría en la función renal y menos diabetes de novo. Los estudios más recientes no muestran aumento de la tasa de rechazo. En conclusión, este metaanálisis sugiere que reducir la exposición al anticalcineurínico inmediatamente después del trasplante puede mejorar los objetivos clínicos»18.
Tacrolimus y tacrolimus de liberación prolongada
El tacrolimus es un potente inhibidor de la calcineurina que tiene una amplia variabilidad intraindividual, que oscila entre el 10 y el 40% según los estudios, e interindividual, que se ha estimado entre el 20 y el 60%. Tiene una biodisponibilidad del 25-40% y, al igual que la ciclosporina, se metaboliza por el citocromo P450 3A4. La exposición al fármaco aumenta con el tiempo postrasplante19-21.
Con muy pocas excepciones, está ampliamente aceptado en la literatura que la C0 tiene buena correlación con el AUC, de forma que la determinación de los niveles valle se usa en la práctica clínica habitual. Aunque la C0 tiene buena correlación con el AUC, algunos autores han encontrado que esta correlación se modifica y disminuye con el tiempo22,23.
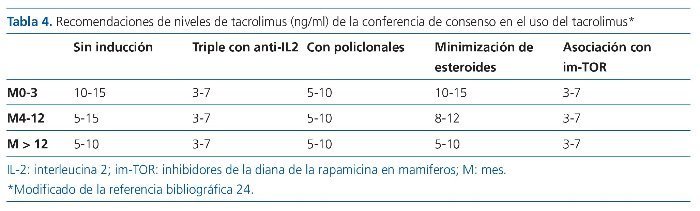
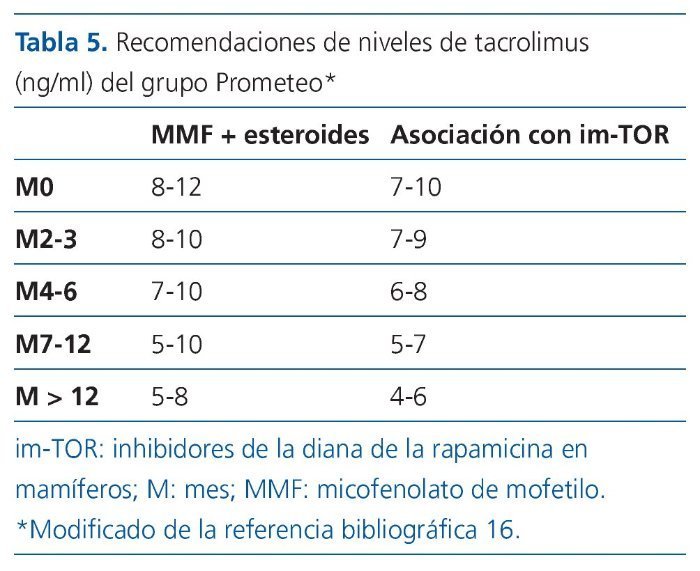
Al igual que con otros inmunosupresores, los niveles óptimos del fármaco dependen de la asociación inmunosupresora utilizada, del estado inmunológico del receptor y del tiempo pasado desde el trasplante. En la tabla 4 se muestran los niveles propuestos por la conferencia de consenso para el uso de tacrolimus y en la tabla 5 las recomendaciones del comité de expertos del grupo Prometeo al que se ha hecho referencia previamente16,17, 24.
Sin embargo, la utilidad de la monitorización del tacrolimus ha quedado recientemente cuestionada por los resultados publicados por Bohuamar et al, que han realizado un análisis de tres ensayos clínicos (el FDCC [fixed dose vs. concentration controlled], el Symphony y el Opticept) en los que se reúnen 1.304 pacientes con monitorización de los niveles de tacrolimus en distintos puntos. En este análisis post hoc se ha evaluado la capacidad para predecir el rechazo agudo de las concentraciones de tacrolimus en los días 3, 6 y 14, y en los meses 1 y 6, separando a los pacientes según los niveles de tacrolimus y analizando el porcentaje de rechazo agudo en cada uno de los grupos. En los pacientes de estos ensayos clínicos, no han encontrado mayor incidencia de rechazo en los que tenían niveles más bajos; tampoco en el análisis multivariante los niveles de tacrolimus influyeron significativamente en la aparición de rechazo25. Además, al igual que ocurre con la ciclosporina, la monitorización del fármaco a largo plazo tampoco ha sido evaluada en ensayos clínicos, por lo que el nivel de evidencia de las recomendaciones de monitorización a largo plazo es bajo.
Variabilidad terapéutica del tacrolimus y resultados a largo plazo
La monitorización de los niveles de tacrolimus a largo plazo viene condicionada por la clara relación existente entre la adherencia y la pérdida del injerto.
Se ha estimado que la variabilidad intraindividual en pacientes estables se encuentra entre el 15 y el 30%, y, en una revisión realizada por Shuker, se ha encontrado que puede estar condicionada por distintos factores, entre ellos la técnica de medición, el período de ayuno corto o nulo, la diarrea, las interacciones con otros fármacos, la adherencia y el uso de fármacos genéricos26.
Un estudio realizado en el Hospital General de Toronto en 356 pacientes estables con más de un año de trasplante renal, seguidos entre los años 2000 y 2011, ha encontrado un incremento del 27% del riesgo de rechazo agudo, glomerulopatía o pérdida del injerto por cada aumento de la variabilidad superior a una desviación estándar27. Otros estudios han hallado los mismos resultados28.
Varios estudios han mostrado que la forma de liberación prolongada aumenta la adherencia al fármaco y disminuye los costes derivados de la pérdida del injerto, y posiblemente también disminuya la variabilidad terapéutica del tacrolimus, como sugiere el amplio estudio de conversión realizado en España29-31. Pero el efecto a largo plazo necesita ser demostrado.
Recomendaciones KDIGO (kidney disease: improving global outcomes) para la monitorización de los anticalcineurínicos32
Se recomienda medir los niveles de anticalcineurínicos (nivel de evidencia 1B) y se sugiere medirlos al menos:
– Cada 2 días en el postrasplante inmediato hasta que se haya logrado el objetivo terapéutico (nivel de evidencia 2C).
– En cualquier momento en que haya un cambio en la medicación del paciente que pueda afectar a los niveles sanguíneos.
– En cualquier momento en que haya un deterioro de la función renal que pueda indicar nefrotoxicidad o rechazo.
Métodos de monitorización farmacológica:
– Ciclosporina: se sugiere monitorizar la ciclosporina mediante la C2, la C0 o el AUC abreviada (0-4 horas) (nivel de evidencia 2D).
– Tacrolimus: se sugiere monitorizar el tacrolimus usando niveles valle a las 12 horas (C0) (nivel de evidencia 2C).
El grupo Prometeo asume estas recomendaciones, pero, además, propone monitorizar a largo plazo ambos fármacos, tal como se hace en la práctica clínica habitual.
Esta recomendación se basa en la amplia variabilidad intraindividual de ambos fármacos, en la relación de su adsorción con la comida, en su nefrotoxicidad, en sus frecuentes interacciones medicamentosas y en el creciente papel de la adherencia al tratamiento como causa de pérdida del injerto, por lo que creemos que la monitorización en fase estable debe ir dirigida a disminuir la variabilidad interindividual y a mejorar la adherencia, con el objetivo último de mejorar la supervivencia del injerto a largo plazo.
MICOFENOLATO DE MOFETILO Y ÁCIDO MICOFENÓLICO
El principio activo es el ácido micofenólico, pero los primeros ensayos clínicos se hicieron con micofenolato de mofetilo (MMF). Actúan inhibiendo selectivamente la proliferación de los linfocitos B y T, porque inhiben la acción de la inositol monofosfato deshidrogenasa (IMPDH), que es fundamental para la síntesis del nucleótido guanosina. Desde los primeros ensayos clínicos en trasplante renal se han empleado dosificándolos de manera fija, sin monitorización de los niveles en sangre. Aunque su biodisponibilidad es alta, en diversos estudios se ha encontrado que disminuye al aumentar la dosis, quizás en relación con la saturación del proceso de adsorción33.
Los determinantes más importantes de su variabilidad son la función renal, los niveles de albúmina y el anticalcineurínico asociado, observándose un aumento del AUC del MMF que depende del tiempo cuando se asocia a tacrolimus, por lo que, pasados 3 meses desde el trasplante, la dosis plena del MMF/ácido micofenólico es inferior cuando se asocia a tacrolimus34.
Para monitorizar la actividad del fármaco se ha analizado en diversos estudios el AUC, que se ha correlacionado con parámetros de eficacia y seguridad, con lo que se han establecido unos valores del AUC entre 30 y 60. También se han realizado estudios con monitorización de los niveles valle, en los que se han relacionado los niveles con el rechazo agudo, así como con efectos hematológicos34-37.
Sin embargo, la utilidad de los niveles valle para monitorizar la eficacia del fármaco no ha sido corroborada en todos los estudios, por lo que se han publicado múltiples intentos de simplificación del AUC, en los que se ha encontrado que existe mejor correlación con el AUC cuando se utiliza la determinación con tres o cuatro puntos: 1-3-9 horas o 1-2-3-6 horas37-39.
La conferencia de consenso sobre monitorización de micofenolato que publicó sus conclusiones en 2010 estima que la monitorización con el AUC con un número de extracciones limitadas es mejor modo de determinación que los niveles valle, ya que se asocia con la eficacia en el postraplante inmediato, aunque no es suficientemente válida para predecir los efectos adversos40.
Recientemente se han publicado los resultados de un metaanálisis de cuatro ensayos clínicos realizados entre 2007 y 2011 en los que se reúnen 1.755 pacientes en los que se ha comparado la utilización de MMF en dosis fijas con la utilización con monitorización terapéutica, en tres ensayos con el AUC y en uno con niveles valle.
Los resultados de este metaanálisis favorecen la utilización de MMF con dosis fijas, puesto que no se ha conseguido demostrar un aumento de la eficacia del fármaco cuando se ha monitorizado el AUC o los niveles y, en cambio, se ha observado un aumento significativo de la incidencia de procesos infecciosos en los grupos de monitorización41.
Dada la escasa relación de los niveles de MMF y de ácido micofenólico con la eficacia y la seguridad del fármaco, se ha intentado en diversos estudios medir la actividad de la IMPDH y correlacionarla con parámetros de eficacia y seguridad.
Hemos revisado los datos de tres estudios, realizados por Bremer, Molinaro y Raggi respectivamente, que analizan la actividad de esta enzima en pacientes trasplantados renales tratados con micofenólico. En estos estudios se concluye que existe una gran variabilidad intra e interindividual en la actividad de la IMPDH, que existe poca relación entre la actividad de la enzima y los niveles del fármaco, y que parece existir una relación negativa entre la actividad de la IMPDH pretrasplante y el riesgo de rechazo agudo. Todas estas conclusiones son preliminares y no permiten afirmar que la IMPDH sea útil en la monitorización de estos fármacos. También se ha analizado la expresión del ácido ribonucleico mensajero (mRNA por sus siglas en inglés, messenger ribonucleic acid) de la IMPDH con unos resultados similares, sin que se haya conseguido demostrar relación entre la expresión de m-RNA y la actividad de IMPDH42 -44.
Como consecuencia de todos estos estudios, podemos concluir que, en la actualidad, no disponemos de una buena herramienta de monitorización del ácido micofenólico y, en consecuencia, no recomendamos la monitorización sistemática del fármaco. La utilidad de la monitorización de sus niveles podría quedar reducida a la valoración de la adherencia.
FÁRMACOS INHIBIDORES DE LA M-TOR: EL SIROLIMUS Y EL EVEROLIMUS
Se unen a la ciclofilina proteína de unión a FK506 (FK-BP por sus siglas en inglés, FK506 binding protein), que también es utilizada por el tacrolimus, y a través de esta unión inhiben la m-TOR. La inhibición de la m-TOR, entre otras muchas acciones, bloquea la acción de la interleucina 2 (IL-2) y detiene el ciclo de división celular en la fase G1 (gap 1). Ambos fármacos se metabolizan por el citocromo P450 3A4 y por la glicoproteína P, lo que condiciona en parte que aumente su exposición cuando se usan asociados a anticalcineurínicos. El aumento de exposición cuando se asocian a anticalcineurínicos es mayor con el sirolimus y la ciclosporina45,46.
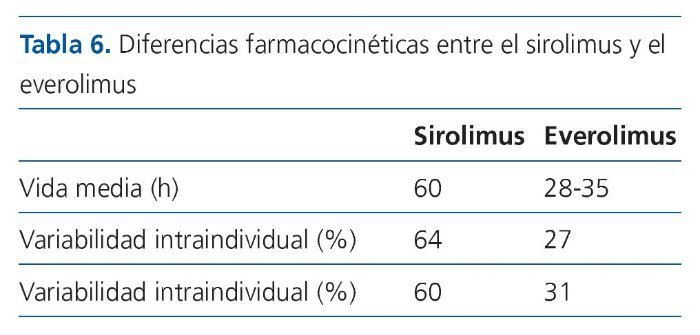
Tanto el everolimus como el sirolimus tienen el mismo mecanismo de acción. Sin embargo, existen algunas diferencias farmacocinéticas entre ambos fármacos que se describen en la tabla 6.
En la clínica, la monitorización de los im-TOR se hace usando la C0, que ha mostrado buena correlación con el AUC, tanto con la rapamicina como con el everolimus. No obstante, los métodos de determinación de estos fármacos están en continua renovación y llama la atención la gran cantidad de artículos aparecidos en la literatura evaluando diversos métodos de determinación de niveles en sangre, algunos de ellos comunes a la rapamicina y el everolimus47-50. Este año se han publicado los primeros resultados de la monitorización farmacodinámica de los im-TOR midiendo a través de la citometría la actividad quinasa de la p70S6K. Esta determinación se encuentra aún en fase experimental y desconocemos si se incorporará a la práctica clínica rutinaria51.
ASOCIACIÓN CON ANTICALCINEURÍNICOS
La asociación de la ciclosporina y el sirolimus aumenta notablemente el AUC de ambos fármacos, lo que obliga a administrar el sirolimus de forma retardada con respecto a la administración de la ciclosporina (4 horas).
La asociación del sirolimus con el tacrolimus también provoca un aumento de la exposición de ambos fármacos, de forma que el aumento de dosis del sirolimus ocasiona un aumento de exposición al tacrolimus y viceversa: el aumento de dosis del tacrolimus aumenta la exposición al sirolimus. En cualquier caso, la interacción que tiene el sirolimus con el tacrolimus es inferior a la que tiene con la ciclosporina.
En cuanto a la asociación del everolimus con el tacrolimus, no hay acuerdo en todos los estudios. En unos, el everolimus parece hacer descender mínimamente la exposición al tacrolimus de forma dependiente de la dosis, precisándose dosis mayores de tacrolimus al aumentar la dosis de everolimus. De modo inverso, la reducción de la dosis de tacrolimus reduce en un 14% la exposición al everolimus. En otros estudios no se ha encontrado ninguna interacción relevante47.
Cuando el everolimus se asocia a la ciclosporina, tiene 2,5 veces más exposición que cuando se asocia al tacrolimus, por lo que la dosis estándar de everolimus asociado al tacrolimus es mayor que cuando se asocia a la ciclosporina47.
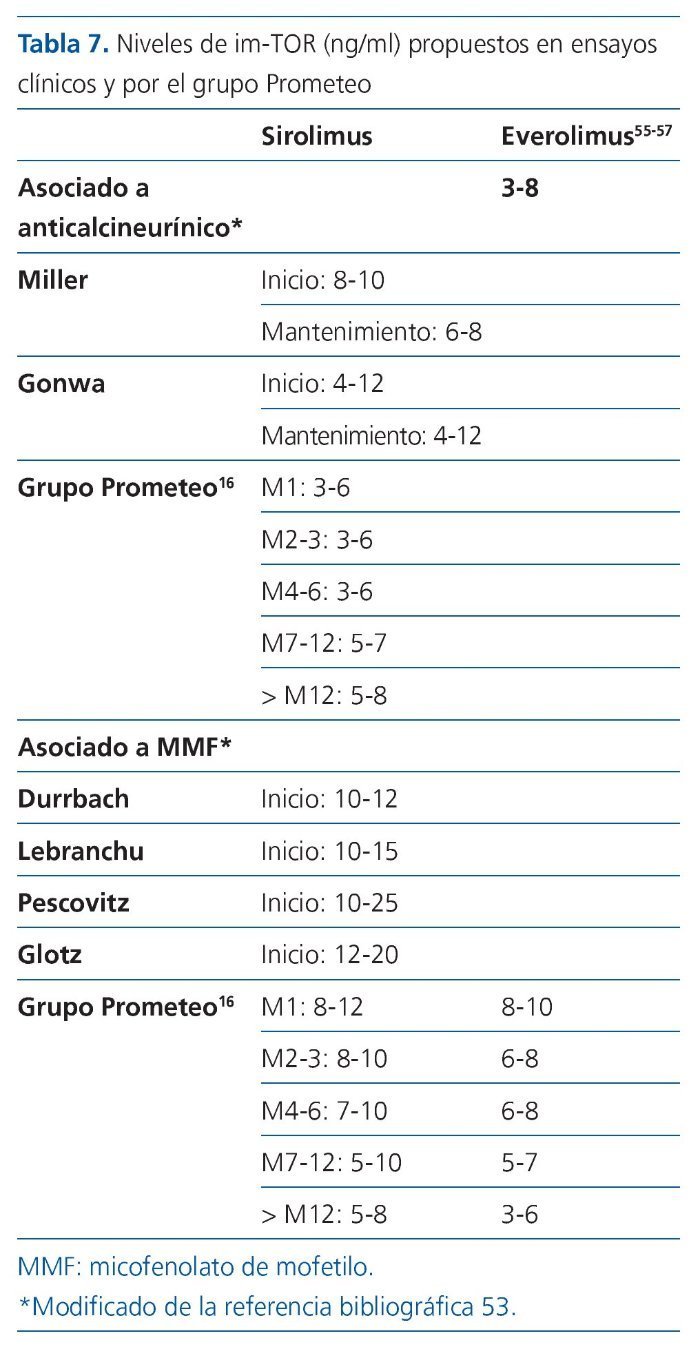
Los primeros ensayos clínicos con sirolimus se llevaron a cabo en comparación con la ciclosporina y la dosificación se estableció sobre la base de unos niveles terapéuticos de 30 ng/ml en el postrasplante inmediato, seguidos de 15 ng/ml en dosis de mantenimiento52. En la actualidad sabemos que estos niveles son muy elevados y que se acompañan de una tasa importante de efectos adversos. En ensayos posteriores se han utilizado dos estrategias: la estrategia de asociar con dosis plena de anticalcineurínico y la de la minimización del anticalcineurínico53,54. El metaanálisis previamente comentado realizado por Sharif concluye que las estrategias de minimización del anticalcineurínico favorecen la supervivencia del paciente y del injerto. Los niveles de rapamicina en estos estudios son notablemente inferiores y oscilan entre 3 y 12 ng/ml. En la tabla 7 se muestran los niveles de distintos ensayos clínicos y los propuestos por el grupo Prometeo.
Con el everolimus, las estrategias de desarrollo del fármaco han sido con minimización de la ciclosporina, con la que se han establecido unos niveles terapéuticos de everolimus entre 3 y 8 ng/ml. En asociación con el tacrolimus, los estudios US09 y ASSET han comparado dos estrategias de minimización del tacrolimus con buenos resultados. Hay en marcha un ensayo clínico con gran número de pacientes que creemos que ayudará a establecer de forma definitiva la dosificación y los niveles de everolimus en asociación con el tacrolimus55-57.
La mayoría de los ensayos clínicos realizados con estos fármacos se han llevado a cabo con pacientes de riesgo inmunológico bajo, por lo que las recomendaciones de los niveles que se muestran en la tabla solo son aplicables a este grupo de enfermos.
Las KDIGO recomiendan monitorizar los im-TOR con un nivel de evidencia 2C. Desde el grupo Prometeo asumimos estas recomendaciones.
CONSIDERACIONES ESPECIALES DE APLICACIÓN A TODOS LOS INMUNOSUPRESORES
Creemos que, para valorar correctamente los niveles de un fármaco, el clínico debe estar habituado y conocer el manejo de las muestras y el método de determinación de su laboratorio y sus controles de calidad, puesto que un porcentaje desconocido de la variabilidad al fármaco podría estar en relación con los métodos de laboratorio.
Asimismo, es importante conocer el tiempo exacto de la determinación valle que estamos evaluando interrogando al paciente sobre la hora de la última toma.
Conflicto de intereses
Los autores declaran que no tienen conflictos de intereses potenciales relacionados con los contenidos de este artículo.
Correspondencia:
Ana María Fernández
Servicio de Nefrología.Hospital Universitario Ramón y Cajal, Madrid.
afrodriguez@salud.madrid.org