El tratamiento renal conservador (TRC) se ha convertido en una opción terapéutica en la enfermedad renal crónica avanzada en ancianos. Se sabe poco sobre la evolución pronóstica de estos pacientes en términos de supervivencia y calidad de vida relacionada con la salud (CVRS).
ObjetivoEstablecer variables predictivas de mortalidad y analizar la CVRS en los pacientes en TRC.
Pacientes y métodosEstudio de cohortes prospectivo. Se realizó una valoración de parámetros de función renal y evaluación geriátrica integral: análisis de comorbilidad, situación funcional, cognitiva, fragilidad, nutricional, social y CVRS.
ResultadosSe evaluaron 82 pacientes, con una edad media de 84 años e importante pluripatología: el 56% tenía antecedentes de evento vascular y Charlson >8. La tasa de mortalidad fue de 23/1.000 pacientes-mes, con un ritmo de mortalidad homogéneo a partir de los 6 meses.
La supervivencia difirió significativamente si presentaban evento vascular previo (36,7 vs. 14,8; p=0,028), Charlson ≥10 (42 vs. 17; p=0,002), grado de dependencia (48,4 vs. 19; p=0,002) y fragilidad (27 vs. 10; p=0,05).
Fueron predictores de mortalidad: eFG y proteinuria, presencia de evento vascular previo, comorbilidad de Charlson, parámetros de malnutrición-inflamación (albúmina y puntuación MNA), grado de dependencia, CVRS física y aumento de PTH. La presencia de evento vascular previo, comorbilidad, albúmina descendida y elevación de PTH fueron predictores independientes de mortalidad. La CVRS se mantuvo estable y no se produjo empeoramiento significativo durante el tratamiento.
ConclusionesEl conocimiento de los factores asociados con mortalidad y la evaluación de la CVRS puede ser útil como herramienta en la toma de decisiones en TRC. La presencia de evento vascular previo, comorbilidad, albúmina disminuida y el aumento de PTH fueron predictores independientes de mortalidad.
Conservative Management (CM) has become a therapeutic option in Advanced Chronic Kidney Disease in the elderly. However, there is a lack of evidence about prognosis of these patients in terms of survival and health related quality of life (HRQoL).
ObjectiveEstablish predictive variables associated with mortality and analyse HRQoL in CM patients.
Patients and methodsProspective cohort study. An assessment of renal function parameters and a comprehensive geriatric assessment were made, including: analysis of comorbidity, functional, cognitive, fragility, nutritional, social and HRQoL status.
Results82 patients with a mean age of 84 years and significant pluripathology were studied: 56% had history of vascular event and Charlson >8. The mortality rate was 23/1,000 patients per month, with a homogeneous mortality rate after 6 months.
Survival differed significantly depending on whether they presented with a previous vascular event (36.7 vs. 14.8; p=0.028), Charlson score ≥10 (42 vs. 17; p=0.002), functional status (48.4 vs. 19; p=0.002) and fragility (27 vs. 10; p=0.05).
Mortality predictors included eGFR and proteinuria, the presence of previous vascular events, Charlson comorbidity score, malnutrition-inflammation parameters (albumin and MNA score), degree of dependency, physical HRQoL and increase of PTH level. The presence of previous vascular event, comorbidity, decreased albumin and elevated PTH were independent predictors of mortality. HRQoL remained stable over time and no significant worsening occurred during treatment.
ConclusionsHaving knowledge of the factors associated with mortality and HRQoL assessment can be a useful tool to helping decision making during CM. Previous vascular events, comorbidity, decreased albumin and increased PTH were independent predictors of mortality.
La prevalencia de la enfermedad renal crónica (ERC) en España ha crecido un 20% en la última década y aumenta de forma progresiva con la edad1. Según datos del Registro Español de Enfermos Renales del año 2016, la prevalencia de ERC es del 25% en mayores de 64 años y del 22% en mayores de 75 años2.
Además del envejecimiento poblacional, enfermedades de alta prevalencia como la hipertensión arterial (HTA), la diabetes o la enfermedad cardiovascular son factores que contribuyen a este incremento de ERC3, y favorecen que se presente en pacientes con importante comorbilidad.
Por lo tanto nos enfrentamos, cada vez con más frecuencia, a la decisión clínica de iniciar tratamiento renal sustitutivo (TRS) o tratamiento renal conservador (TRC) en pacientes ancianos con elevada comorbilidad, haciéndose necesario valorar los beneficios de ambas actuaciones4.
Aunque la supervivencia global suele ser superior en los pacientes que se dializan frente a los que no, esta ventaja se pierde en los mayores de 80 años que presentan mayor comorbilidad, fundamentalmente si asocian cardiopatía isquémica5,6. Además, la carga de síntomas (dolor, fatiga, anorexia, disnea) que presentan estos pacientes en diálisis es alta7,8, la calidad de vida relacionada con la salud (CVRS) a menudo es deficiente9,10 y muchos de ellos presentan un progresivo deterioro funcional secundario11.
Ante las evidentes limitaciones en el TRS de estos pacientes surge en la actualidad un interés creciente por conocer si el TRC o manejo activo sin diálisis de la ERC avanzada (ERCA) es una opción terapéutica válida.
El TRC supone un manejo integral que debe incluir: intervenciones para retrasar la progresión de la enfermedad renal y minimizar el riesgo de eventos adversos, toma de decisiones compartida, manejo activo de los síntomas, comunicación detallada, planificación de atención avanzada, soporte psicológico, apoyo social, familiar y espiritual12.
Los nefrólogos podemos tener dificultades para establecer estas conversaciones13, en parte debido a la ausencia de información pronóstica que nos ayude a aconsejar a nuestros pacientes en el proceso de decisión.
La mayoría de los estudios señalan que los pacientes en TRC tienen peor pronóstico, menor supervivencia14,15 y CVRS reducida. La mayoría son estudios trasversales y retrospectivos16.
Con la finalidad de proporcionar información sobre la utilidad del TRC a pacientes y profesionales y facilitar el proceso de decisión compartida, realizamos un análisis detallado de los pacientes que eligen TRC. Los objetivos fueron:
- 1.
Establecer variables predictivas de mortalidad en los pacientes en que se decide TRC.
- 2.
Analizar la evolución de la CVRS en esta población de manejo conservador.
Estudio de cohortes observacional, prospectivo, analítico de pacientes atendidos en el Servicio de Nefrología del Hospital Universitario Miguel Servet de Zaragoza.
Criterios de inclusiónPacientes mayores de 75 años, incidentes en TRC.
El proceso de decisión compartida fue llevado a cabo por el nefrólogo responsable del paciente, teniendo en cuenta los siguientes criterios:
- -
Diagnóstico de ERCA con filtrado glomerular (FG) inferior a 20ml/min/1,73m2 (en 2 determinaciones analíticas separadas en 3 meses).
- -
Pacientes en quienes no hay una indicación clínica de tratamiento activo sustitutivo por parte de su médico responsable.
No se incluyeron aquellos pacientes con incapacidad para realizar la entrevista clínica y ausencia de apoyo familiar.
SeguimientoEl reclutamiento se realizó desde el 1 de enero del 2015 hasta el 1 de mayo del 2017. El seguimiento concluyó con el fallecimiento del paciente o con la fecha de cierre del estudio el 31 de diciembre de 2017. Se realizaron visitas programadas a los 0, 12 y 24 meses del seguimiento, con recogida de valores analíticos y test específicos que analizan diferentes esferas de salud: comorbilidad, situación funcional, cognitiva, fragilidad, nutricional, CVRS y social.
Fuentes de datosLas valoraciones fueron realizadas por el equipo investigador mediante entrevista clínica. Los antecedentes personales, datos analíticos y fallecimiento (fecha y causa de la muerte) se recogieron de la historia clínica hospitalaria e historia clínica electrónica del paciente.
Consideraciones éticasEste estudio fue aprobado por el Comité Ético de Investigación Clínica de Aragón (CEICA) y todos los pacientes firmaron un consentimiento informado antes de la inclusión en el estudio.
Variables recogidas- -
Variables demográficas: edad y sexo.
- -
Variables clínicas:
- •
Peso y talla con cálculo de índice de masa corporal (IMC): peso(kg)/talla2(m).
- •
Antecedentes de patología previa: HTA, diabetes, causa de ERC, evento vascular previo (antecedentes de cardiopatía isquémica, enfermedad cerebrovascular o enfermedad vascular periférica).
- •
Comorbilidad: índice de Charlson.
- •
Situación funcional: índice de Barthel.
- •
Situación cognitiva: Test de Pfeiffer.
- •
Fragilidad: Cuestionario FRAIL.
- •
Valoración nutricional: test Mini-Nutritional Assessment Short-Form
- •
CVRS: Cuestionario de Salud SF-36 v2.
- •
Situación social: Escala de Gijón.
- -
Variables analíticas: eFG (CKD-EPI ml/min/1,73m2), proteinuria (g/l), albúmina (mg/dl), proteína C reactiva ultrasensible ([PRCu] mg/dl), NT-proBNP (pg/ml), potasio (mEq/l), hemoglobina (g/l), PTH (pg/ml), calcio (mg/dl) y fósforo (mg/dl).
- -
La comorbilidad se clasificó de acuerdo con el índice de Charlson ajustado a la edad17,18, según las definiciones establecidas en el artículo original publicado en 1987, y añadiendo un punto por cada década por encima de los 50 años al valor obtenido en el índice. Se consideran altas las puntuaciones entre 6-7 puntos y muy altas si son iguales o superiores a 8 puntos.
- -
La situación funcional para actividades básicas de la vida diaria fue valorada mediante el índice de Barthel18-20. Se definen: independencia, puntuaciones entre 100-91 puntos; dependencia ligera, entre 90-61 puntos; dependencia moderada, 60-41 puntos; dependencia severa, 40-21 puntos; totalmente dependiente, por debajo de 20 puntos.
- -
La valoración cognitiva se realizó mediante el Test de Pfeiffer18,21. Es un test rápido de cribado en el cual una puntuación de 3 puntos o superior indica que puede existir deterioro cognitivo.
- -
Para identificar la fragilidad, utilizamos el Cuestionario FRAIL22. Consta de 5 preguntas sencillas relativas a fatigabilidad, resistencia, deambulación, comorbilidad y pérdida de peso; cada una se valora con un punto. A diferencia de los criterios de Fried, no requiere dinamómetro para valorar la fuerza muscular, y al igual que en estos, los pacientes se clasifican como frágiles cuando suman 3-5 puntos.
- -
La evaluación nutricional se realizó mediante el test Mini-Nutritional Assessment Short-Form (MNA-SF)23. El MNA es una herramienta de cribado validada que ayuda a identificar a ancianos desnutridos o en riesgo de desnutrición. Una puntuación total igual o mayor de 12 indica que la persona se encuentra bien nutrida, entre 8 y 11 refleja que la persona está en riesgo de desnutrición, e igual o menor a 7 indica que la persona se encuentra desnutrida.
- -
La situación social se objetivó mediante la Escala Sociofamiliar de Gijón (versión abreviada de Barcelona)24: una puntuación de menos de 7 puntos indica una situación social buena; entre 8-9 puntos, situación intermedia; y más de 10 puntos, deterioro social.
- -
La calidad de vida fue evaluada utilizando el Cuestionario de Salud SF-36 v225. Es un instrumento genérico de evaluación de CVRS, traducido al castellano, que consta de 36 ítems agrupados en 8 dimensiones: función física (PF), limitaciones en rol físico (RP), dolor (BP), percepción salud general (GH), vitalidad (VT), función social (SF), limitaciones rol problemas emocionales (RE) y salud mental (MH).
Para cada dimensión los ítems son codificados, agregados y transformados en una escala que tiene un recorrido desde 0 (peor estado de salud) hasta 100 (mejor estado de salud). Permite el cálculo de dos puntuaciones resumen: una sobre el estado de salud física y otra de salud mental. Las puntuaciones se han obtenido a través del QualityMetric Incorporated Health Outcomes Scoring Software 5.0.
La consistencia interna (alfa de Cronbach) de las diferentes escalas oscila entre 0,71 y 0,95.
Métodos estadísticosLas variables cuantitativas se describen con su media y desviación estándar (DE) o con su mediana y rango intercuartílico (RIC), mientras que las cualitativas se expresan con su distribución de frecuencias. Las variables cuantitativas se comparan con la t de Student o prueba no paramétrica de Mann-Whitney. Para la comparación de variables cualitativas se utiliza el test de la χ2 con evaluación de tendencia lineal en variables con categorías ordenadas. La significación estadística del cambio de las variables cuantitativas en los distintos momentos temporales se determinó con el test no paramétrico de Friedman.
Como variable primaria de resultado se consideró la mortalidad total. Se realizó seguimiento de los pacientes desde su inclusión hasta su salida del estudio por alcanzar la fecha de cierre del mismo, por muerte o por pérdida de contacto. Las tasas de mortalidad se expresan por cada 1.000 pacientes-mes. Se llevó a cabo la determinación de las funciones de supervivencia (con método de Kaplan-Meier) y de riesgo (evaluación de la dinámica de mortalidad). La comparación de tasas entre grupos se efectuó con el test log rank.
La evaluación de la contribución independiente de las variables iniciales a la mortalidad se constató en modelos de regresión de Cox, con estimación de las hazard ratios (HR) y sus intervalos de confianza (IC) del 95%. Se eligieron las variables para ser introducidas en los modelos multivariantes según su sentido clínico o su asociación estadística en análisis univariante con p<0,1. Finalmente, se seleccionó el mejor modelo predictivo de mortalidad mediante el procedimiento de exclusión secuencial.
Las asociaciones con p<0,05 fueron consideradas significativas. Se utilizó como programa informático SPSS versión 22.0.
ResultadosSe incluyeron en el estudio un total de 82 pacientes en TRC: 56 pacientes en el año 2015, 23 pacientes en el 2016 y 3 en el año 2017. A lo largo del seguimiento un paciente fue excluido del análisis al decidir abandonar el TRC e iniciar hemodiálisis y 2 pacientes por pérdida de seguimiento.
Las causas de la ERCA fueron: nefroangioesclerosis (57,4%), nefropatía diabética (25,7%), nefropatía tubulointersticial crónica (6,1%), síndrome cardiorrenal (4,9%), glomerulonefritis (2,4%) y otras (3,7%).
De los 82 pacientes del estudio, la causa principal de optar por TRC fue: en 61 pacientes, enfermedad grave no subsidiaria de mejorar con la TRS; en 8 pacientes, dependencia funcional severa; en 5 pacientes, deterioro cognitivo avanzado; en 5 pacientes, decisión propia; en 2 pacientes, enfermedad psiquiátrica limitante, y en un paciente, enfermedad neoplásica diseminada.
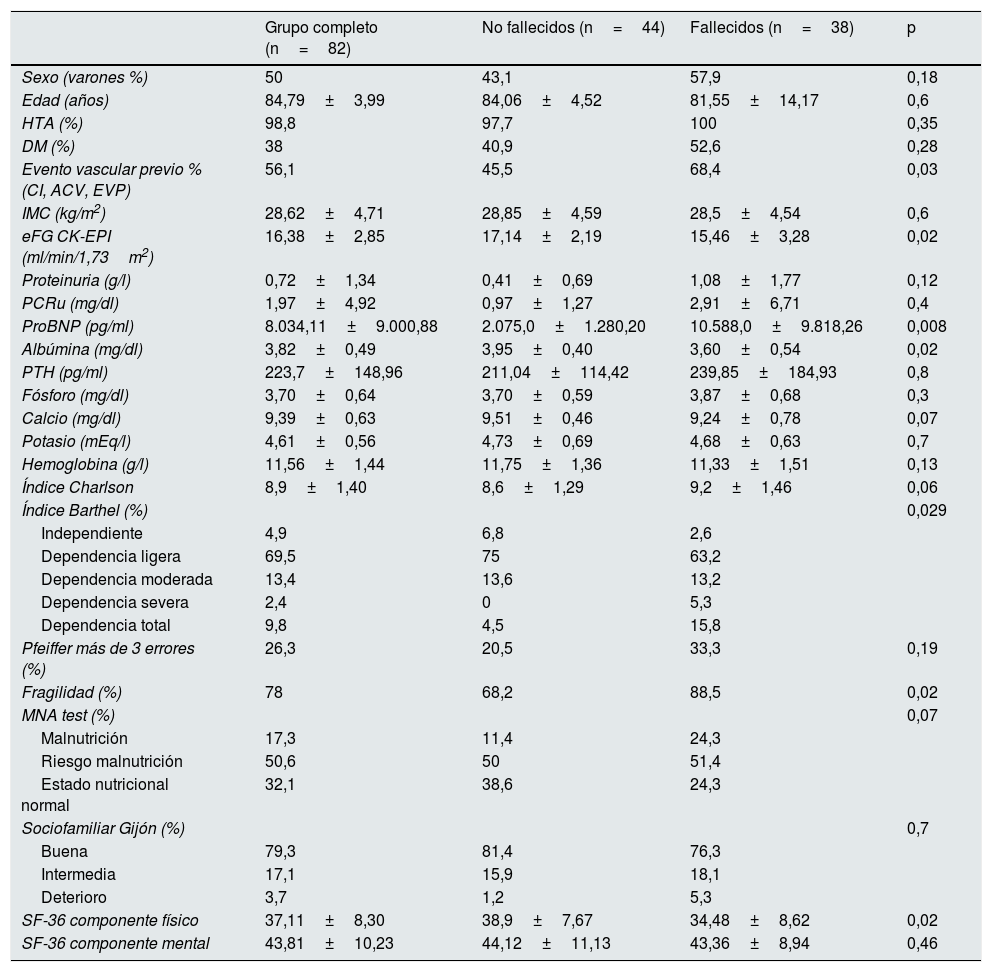
Las características basales de la muestra completa y de los pacientes fallecidos y no fallecidos se plasman en la tabla 1.
Características basales de la muestra completa y de los pacientes fallecidos y no fallecidos
| Grupo completo (n=82) | No fallecidos (n=44) | Fallecidos (n=38) | p | |
|---|---|---|---|---|
| Sexo (varones %) | 50 | 43,1 | 57,9 | 0,18 |
| Edad (años) | 84,79±3,99 | 84,06±4,52 | 81,55±14,17 | 0,6 |
| HTA (%) | 98,8 | 97,7 | 100 | 0,35 |
| DM (%) | 38 | 40,9 | 52,6 | 0,28 |
| Evento vascular previo % (CI, ACV, EVP) | 56,1 | 45,5 | 68,4 | 0,03 |
| IMC (kg/m2) | 28,62±4,71 | 28,85±4,59 | 28,5±4,54 | 0,6 |
| eFG CK-EPI (ml/min/1,73m2) | 16,38±2,85 | 17,14±2,19 | 15,46±3,28 | 0,02 |
| Proteinuria (g/l) | 0,72±1,34 | 0,41±0,69 | 1,08±1,77 | 0,12 |
| PCRu (mg/dl) | 1,97±4,92 | 0,97±1,27 | 2,91±6,71 | 0,4 |
| ProBNP (pg/ml) | 8.034,11±9.000,88 | 2.075,0±1.280,20 | 10.588,0±9.818,26 | 0,008 |
| Albúmina (mg/dl) | 3,82±0,49 | 3,95±0,40 | 3,60±0,54 | 0,02 |
| PTH (pg/ml) | 223,7±148,96 | 211,04±114,42 | 239,85±184,93 | 0,8 |
| Fósforo (mg/dl) | 3,70±0,64 | 3,70±0,59 | 3,87±0,68 | 0,3 |
| Calcio (mg/dl) | 9,39±0,63 | 9,51±0,46 | 9,24±0,78 | 0,07 |
| Potasio (mEq/l) | 4,61±0,56 | 4,73±0,69 | 4,68±0,63 | 0,7 |
| Hemoglobina (g/l) | 11,56±1,44 | 11,75±1,36 | 11,33±1,51 | 0,13 |
| Índice Charlson | 8,9±1,40 | 8,6±1,29 | 9,2±1,46 | 0,06 |
| Índice Barthel (%) | 0,029 | |||
| Independiente | 4,9 | 6,8 | 2,6 | |
| Dependencia ligera | 69,5 | 75 | 63,2 | |
| Dependencia moderada | 13,4 | 13,6 | 13,2 | |
| Dependencia severa | 2,4 | 0 | 5,3 | |
| Dependencia total | 9,8 | 4,5 | 15,8 | |
| Pfeiffer más de 3 errores (%) | 26,3 | 20,5 | 33,3 | 0,19 |
| Fragilidad (%) | 78 | 68,2 | 88,5 | 0,02 |
| MNA test (%) | 0,07 | |||
| Malnutrición | 17,3 | 11,4 | 24,3 | |
| Riesgo malnutrición | 50,6 | 50 | 51,4 | |
| Estado nutricional normal | 32,1 | 38,6 | 24,3 | |
| Sociofamiliar Gijón (%) | 0,7 | |||
| Buena | 79,3 | 81,4 | 76,3 | |
| Intermedia | 17,1 | 15,9 | 18,1 | |
| Deterioro | 3,7 | 1,2 | 5,3 | |
| SF-36 componente físico | 37,11±8,30 | 38,9±7,67 | 34,48±8,62 | 0,02 |
| SF-36 componente mental | 43,81±10,23 | 44,12±11,13 | 43,36±8,94 | 0,46 |
La edad media fue de 84,79±3,99 años y el 50% de los pacientes eran varones. El 56% tenía antecedentes de evento vascular previo, y el índice de Charlson mayor de 8 refleja una elevada comorbilidad.
Análisis de mortalidad y sus factores predictivosFallecieron en el seguimiento 38 pacientes: 26 (68,4%) en el hospital y 12 (31,6%) en domicilio. Las causas de muerte fueron de etiología cardiovascular en 15 pacientes (39,5%), por la propia evolución de la ERCA en 14 pacientes (36,8%), por etiología infecciosa en 4 pacientes (10,5%), neoplasia diseminada en 3 pacientes (7,9%), por traumatismo en un paciente (2,6%) y desconocida en un paciente (2,6%).
Analizamos la diferencia entre los pacientes fallecidos y los que permanecieron vivos tras el periodo de seguimiento. Los pacientes que fallecieron se caracterizaron por tener mayor prevalencia de evento vascular previo, valores más bajos de eFG y albúmina y niveles más altos de NT-proBNP. Asimismo, tenían mayor grado de dependencia y fragilidad, peor puntuación en el componente físico del SF-36 y, en el límite de la significación estadística, peor estado nutricional y mayor puntuación de Charlson.
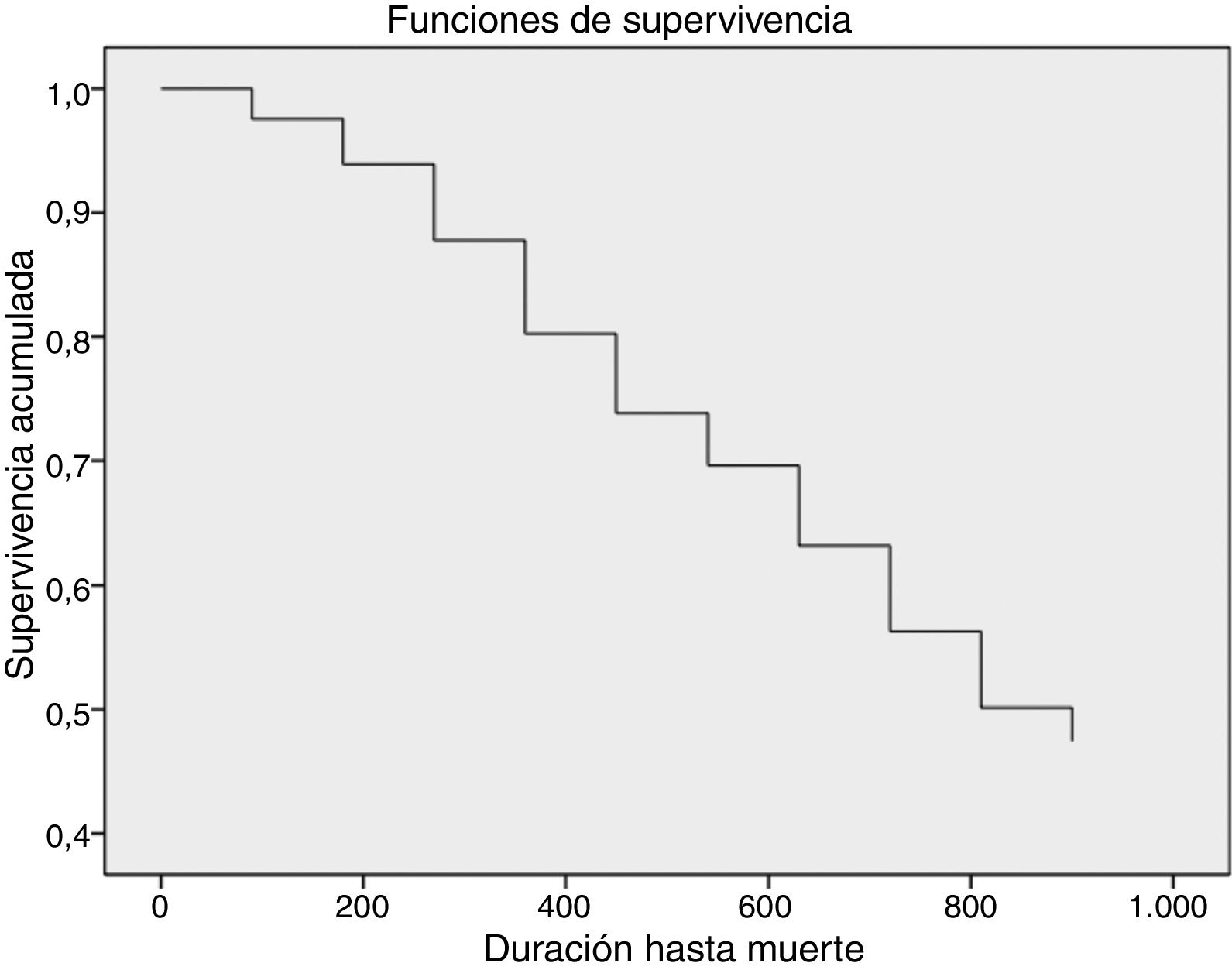
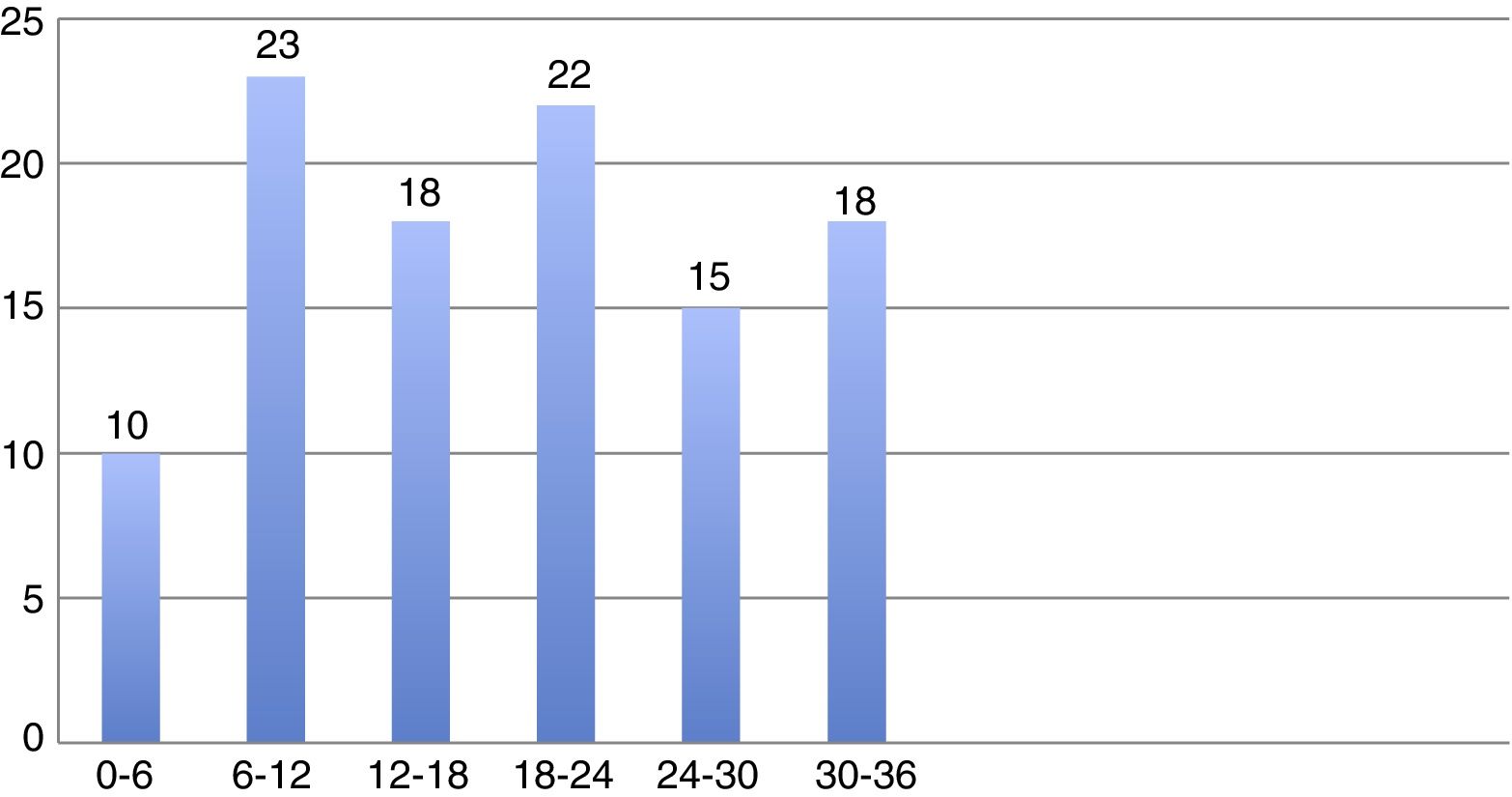
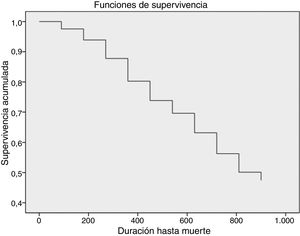
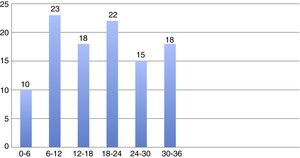
La tasa de mortalidad total fue de 23/1.000 pacientes-mes (fig. 1). En la figura 2 se representa la tasa media de mortalidad mensual por semestres a lo largo del seguimiento, pudiéndose observar que el ritmo de mortalidad a partir de los 6 meses fue homogéneo a lo largo del seguimiento.
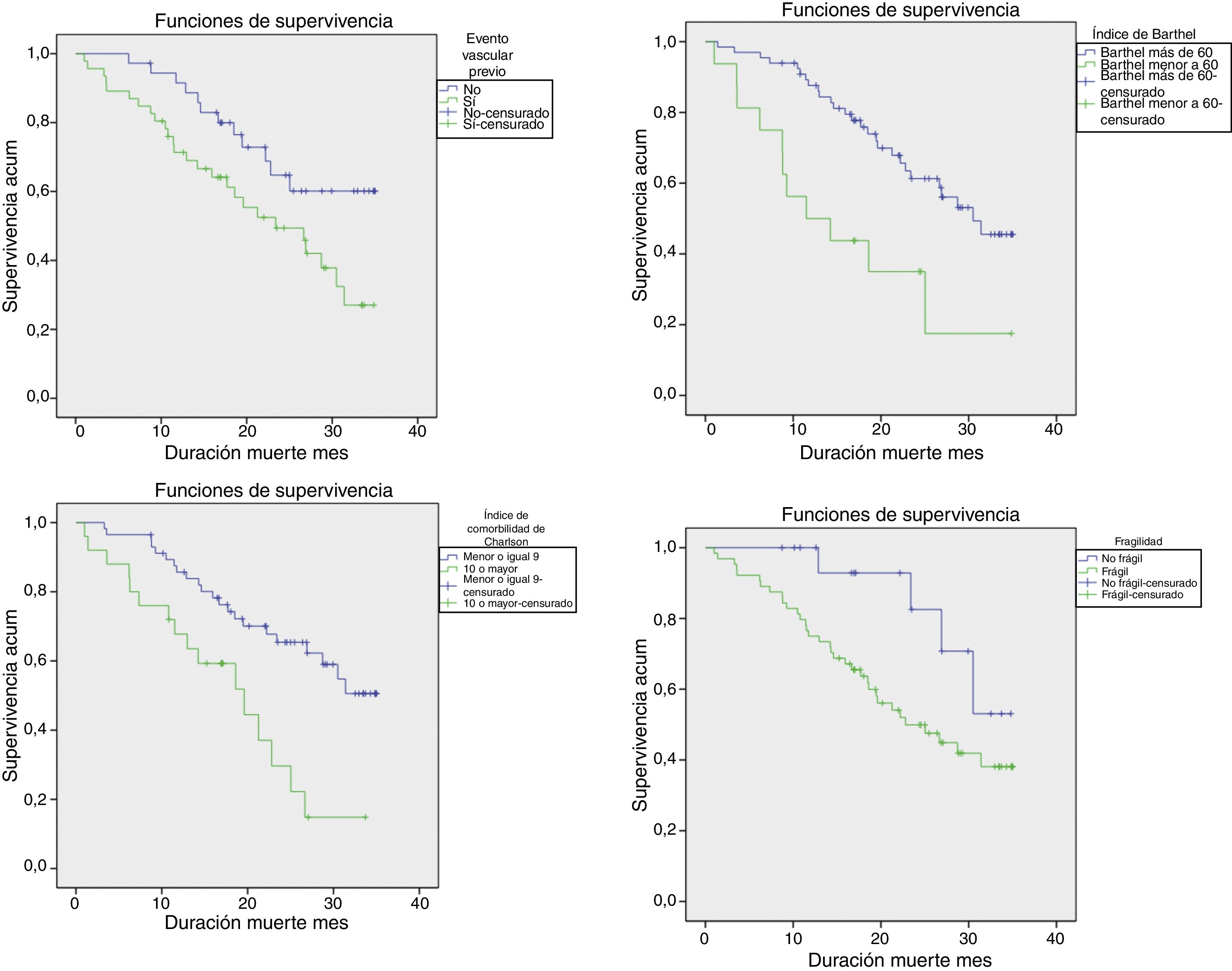
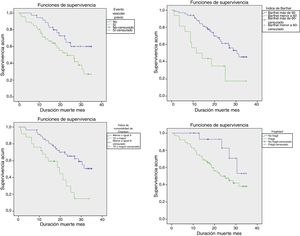
La mediana de supervivencia fue de 26,9 (IC 95%: 19,6-34,2) meses. La supervivencia de los pacientes (fig. 3) difirió significativamente (en dependencia de que presentasen o no evento vascular previo [tasa de mortalidad 36,7 vs. 14,8; p=0,028]), de la puntuación Charlson ≥10 versus <10 [tasa de mortalidad 42 vs. 17; p=0,002], del grado elevado o no de dependencia funcional [tasa de mortalidad 48,4 vs. 19; p=0,002] y de la presencia o no de fragilidad [tasa de mortalidad 27 vs. 10; p=0,05]).
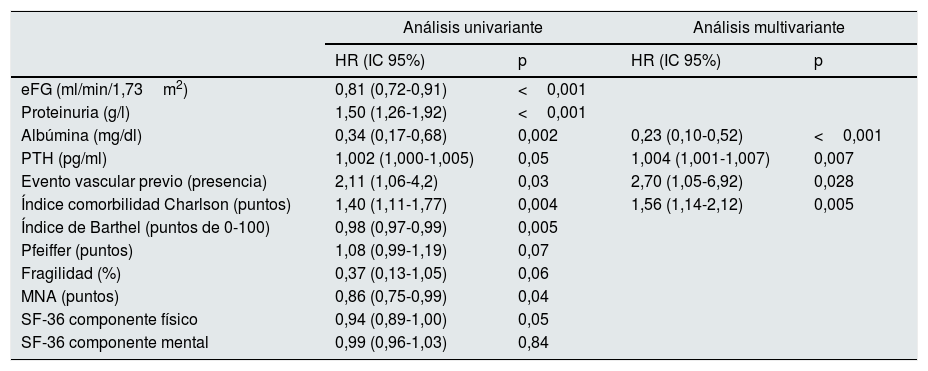
En la tabla 2 se reflejan las variables asociadas de modo significativo con aumento de mortalidad en análisis univariante. Las variables de deterioro cognitivo por el Test de Pfeiffer y de fragilidad quedaron en el límite de la significación estadística. Fueron predictores de mortalidad los parámetros de afectación renal (el FG y la proteinuria), la presencia de evento vascular previo e índice de comorbilidad de Charlson, los parámetros de malnutrición-inflamación (albúmina y puntuación MNA), el grado de dependencia y calidad de vida física y parámetros del metabolismo fosfocálcico (aumento de PTH). En análisis multivariante, la presencia de evento vascular previo, la comorbilidad medida por el índice de Charlson, la albúmina descendida y la elevación de PTH son variables predictivas independientes relacionadas con la mortalidad en pacientes ancianos en TRC.
Variables asociadas con aumento de mortalidad: análisis univariante y multivariante
| Análisis univariante | Análisis multivariante | |||
|---|---|---|---|---|
| HR (IC 95%) | p | HR (IC 95%) | p | |
| eFG (ml/min/1,73m2) | 0,81 (0,72-0,91) | <0,001 | ||
| Proteinuria (g/l) | 1,50 (1,26-1,92) | <0,001 | ||
| Albúmina (mg/dl) | 0,34 (0,17-0,68) | 0,002 | 0,23 (0,10-0,52) | <0,001 |
| PTH (pg/ml) | 1,002 (1,000-1,005) | 0,05 | 1,004 (1,001-1,007) | 0,007 |
| Evento vascular previo (presencia) | 2,11 (1,06-4,2) | 0,03 | 2,70 (1,05-6,92) | 0,028 |
| Índice comorbilidad Charlson (puntos) | 1,40 (1,11-1,77) | 0,004 | 1,56 (1,14-2,12) | 0,005 |
| Índice de Barthel (puntos de 0-100) | 0,98 (0,97-0,99) | 0,005 | ||
| Pfeiffer (puntos) | 1,08 (0,99-1,19) | 0,07 | ||
| Fragilidad (%) | 0,37 (0,13-1,05) | 0,06 | ||
| MNA (puntos) | 0,86 (0,75-0,99) | 0,04 | ||
| SF-36 componente físico | 0,94 (0,89-1,00) | 0,05 | ||
| SF-36 componente mental | 0,99 (0,96-1,03) | 0,84 | ||
No pudieron realizar el test por razones cognitivas o limitación física 16 pacientes (19,5%) en la valoración basal, 26 pacientes (41,2%) a los 12 meses y 12 pacientes (40%) a los 24 meses. De los 64 pacientes a quienes se realizó estudio basal, 37 se valoraron al inicio y 12 meses, y 18 pacientes al inicio, 12 y 24 meses.
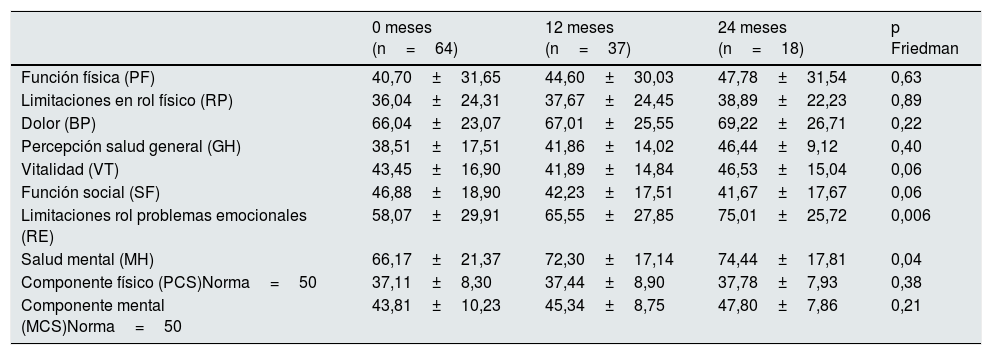
Al inicio del estudio las dimensiones físicas se ven afectadas (función física, limitaciones en el rol físico, dolor y percepción de salud en general) con mejor preservación de la salud mental en las dimensiones rol problemas emocionales y salud mental (tabla 3).
Análisis de la calidad de vida relacionada con la salud a lo largo del tratamiento conservador
| 0 meses (n=64) | 12 meses (n=37) | 24 meses (n=18) | p Friedman | |
|---|---|---|---|---|
| Función física (PF) | 40,70±31,65 | 44,60±30,03 | 47,78±31,54 | 0,63 |
| Limitaciones en rol físico (RP) | 36,04±24,31 | 37,67±24,45 | 38,89±22,23 | 0,89 |
| Dolor (BP) | 66,04±23,07 | 67,01±25,55 | 69,22±26,71 | 0,22 |
| Percepción salud general (GH) | 38,51±17,51 | 41,86±14,02 | 46,44±9,12 | 0,40 |
| Vitalidad (VT) | 43,45±16,90 | 41,89±14,84 | 46,53±15,04 | 0,06 |
| Función social (SF) | 46,88±18,90 | 42,23±17,51 | 41,67±17,67 | 0,06 |
| Limitaciones rol problemas emocionales (RE) | 58,07±29,91 | 65,55±27,85 | 75,01±25,72 | 0,006 |
| Salud mental (MH) | 66,17±21,37 | 72,30±17,14 | 74,44±17,81 | 0,04 |
| Componente físico (PCS)Norma=50 | 37,11±8,30 | 37,44±8,90 | 37,78±7,93 | 0,38 |
| Componente mental (MCS)Norma=50 | 43,81±10,23 | 45,34±8,75 | 47,80±7,86 | 0,21 |
SF-36 v2: puntuaciones 50 (10), la población de referencia tiene una media de 50 con una desviación estándar de 10, por lo que valores superiores o inferiores a 50 indican un mejor o peor estado de salud, respectivamente.
Los pacientes experimentaron como hallazgos significativos sensación de cansancio más acentuado en los primeros 12 meses del tratamiento (VT 0 meses 43,45±16,90 vs. VT 12 meses 41,89±14,84 p=0,03). Además, tuvieron interferencia en sus relaciones sociales habituales a lo largo de los 24 meses de seguimiento (SF 0 meses 46,88±18,90 vs. SF 12 meses 42,23±17,51 p=0,001 y SF 0 meses 46,88±18,90 vs. SF 24 meses 41,67±17,67 p=0,015).
Sin embargo, los pacientes refirieron una menor limitación en las actividades diarias debidas a problemas emocionales durante el tratamiento (RE 0 meses 58,07±29,91 vs. RE 24 meses 75,01±25,72 p=0,05 y RE 12 meses 65,55±27,85 vs. RE 24 meses 75,01±25,72 p=0,05) junto con una mejoría de la percepción en la salud mental, aunque esta última no alcanzó la significación estadística.
Analizamos el cambio de la CVRS en los distintos momentos del seguimiento, mediante el test de Friedman: observamos como la calidad de vida se mantiene estable y como el cambio en el tiempo no es significativo, con mejora en la limitación en las actividades diarias debidas a problemas emocionales y una buena percepción en la salud mental.
DiscusiónEn nuestro estudio hemos constatado que los pacientes en TRC son pacientes con evolución a la cronicidad y pluripatológicos26 por la presencia de comorbilidad asociada (un 56% de los pacientes habían tenido un evento vascular previo, el 38% eran diabéticos y la puntuación media era de 9 en el índice de Charlson). Muchos de estos pacientes son pacientes crónicos complejos, ya que además de tener distintas enfermedades progresivas presentan polifarmacia, dependencia para actividades básicas de la vida diaria y mala situación social (un 13,4% de nuestros pacientes presentaron dependencia moderada, un 2,4% severa y un 9,8% total, y un 20% tenían problemas a nivel sociofamiliar). El TRC no debe conllevar una «ausencia de tratamiento» o una menor asistencia especializada, sino que debe prestar una asistencia integral para intentar retrasar la progresión de la enfermedad renal, manejar los síntomas y, llegado el momento, planificar una atención avanzada paliativa6.
Los resultados en nuestro estudio muestran que la supervivencia mediana en los pacientes en TRC fue de 26 meses. Wong et al.15 objetivaron una supervivencia de 23,4 meses, pero incluían pacientes con FG por debajo de 30ml/min/1,73m2. Chanda et al.27, una media de supervivencia de 21,2 meses; Murtagh et al.5, 18 meses; Ellam et al.14, 21 meses; pero en ellos el FG fue de 15ml/min/1,73m2.
Estos trabajos —heterogéneos en los criterios de inclusión— analizan la supervivencia de los ancianos en TRC frente a TRS: en los resultados de la mayoría de ellos la diálisis aumenta la supervivencia frente al manejo conservador, pero la edad por encima de los 80 años28, la presencia de comorbilidad27,29 y cardiopatía isquémica5 hacen que estas diferencias se reduzcan sustancialmente.
La mortalidad es homogénea a lo largo del seguimiento. El hecho de que no se produzca una mayor mortalidad en un periodo determinado —especialmente en los primeros meses de tratamiento—, y que la causa fundamental de fallecimiento sea la cardiovascular y el deterioro progresivo de la función renal, remarca que estos pacientes se benefician de un seguimiento adecuado y de un cuidado multidisciplinar, sin incidir en otro tipo de actuaciones más cruentas.
La valoración geriátrica30-33 proporciona un abordaje global de la persona anciana mediante valoración clínica (con identificación de enfermedades crónicas y aspectos nutricionales), valoración funcional, valoración cognitiva, valoración psicosocial y fragilidad, cobrando cada vez más importancia en los pacientes con ERC18. En estos pacientes la evaluación y el tratamiento requiere de un abordaje multidisciplinar con estrategias que identifiquen factores de peor pronóstico que ayude en la toma de decisiones.
En nuestro estudio comprobamos que los pacientes con menor supervivencia fueron aquellos con mayor comorbilidad inicial, con evento vascular previo, con mayor grado de dependencia y con fragilidad. También el eFG, la proteinuria, la albúmina, la situación nutricional y el aumento de PTH se relacionaron con mortalidad en el análisis univariante. En el análisis multivariante final mantuvieron la significación estadística la comorbilidad elevada, la presencia de evento vascular previo, el descenso de la albúmina y el aumento de la PTH.
Aunque los valores medios de albúmina y PTH en nuestros pacientes fuesen adecuados, nuestro análisis refleja que cuanto mayores se mantengan los niveles de albúmina y menores los de PTH, mejor será el pronóstico.
Trabajos previos describen la comorbilidad como factor pronóstico de mortalidad15. Ellam et al.14 encontraron que niveles de albúmina superiores a 3,5mg/dl se asociaron a mayor supervivencia. Joly et al.34 realizaron un análisis de pacientes de más de 80 años en TRC y TRS y comprobaron que los octogenarios que no fueron a diálisis diferían de aquellos en TRS en términos de grado de dependencia, comorbilidad y diabetes. En el análisis de Cox, los predictores independientes de muerte en diálisis fueron el estado nutricional, la dependencia funcional y la presencia de macroangiopatía definida por enfermedad vascular periférica.
La prevalencia de calcificación vascular está documentada en pacientes con ERCA35. Es posible que tenga una etiología multifactorial y se deba al envejecimiento, a la comorbilidad y a trastornos en el metabolismo óseo mineral (MOM). Las alteraciones del MOM conllevan además una arquitectura ósea anormal36, desarrollo de fracturas37 y disminución en la movilidad en estos pacientes, las cuales pudieran justificar la relación de niveles elevados de PTH con la mortalidad en nuestros resultados.
La fragilidad no fue un factor predictivo independiente de mortalidad en nuestro trabajo, si bien los resultados estuvieron en el límite de la significación estadística. Una explicación pudiera ser el número limitado de pacientes del trabajo, que resta potencia estadística, y la superposición de comorbilidad y dependencia ya descrita en trabajos anteriores en una cohorte de pacientes en diálisis38.
La mayoría de los trabajos que analizan la calidad de vida en pacientes con ERCA se centran en pacientes en diálisis, especialmente en pacientes que reciben hemodiálisis, y son de tipo observacional trasversal9,10. Nuestros resultados analizan la evolución de la CVRS en pacientes en TRC y muestran que las áreas más afectadas fueron las dimensiones físicas y la dificultad para llevar a cabo sus relaciones sociales. Por otro lado, los pacientes percibieron una menor limitación en las actividades diarias debidas a problemas emocionales y una buena percepción en la salud mental en forma de calma y bienestar.
En un estudio reciente de supervivencia y evolución de CVRS39 realizado con pacientes en TRC y TRS, la calidad de vida física en el manejo conservador se mantuvo o mejoró después de 12 meses de tratamiento en menos de la mitad de los pacientes, mientras que la salud mental se mantuvo o mejoró en algo más de la mitad. Nuestros resultados muestran que los pacientes en TRC perciben las limitaciones físicas consecuencia del paso del tiempo y evolución de su enfermedad, pero a la vez estos pacientes mantienen mayor satisfacción en dimensiones psicológicas con una calidad de vida que no empeora en el tiempo y que se mantiene estable, objetivo primordial del TRC.
Como aportaciones del presente trabajo, cabe resaltar que se trata de un estudio prospectivo que incluye evaluación de parámetros de función renal, situación funcional, fragilidad, estado nutricional y CVRS. El análisis realizado, de supervivencia y calidad de vida, en los pacientes que ya han tomado la decisión de un manejo conservador, puede ser útil como herramienta para informar y orientar al paciente en el proceso de decisión compartida. Además, analiza de una forma integral al paciente anciano, un grupo cada vez más numeroso y poco visible por la ausencia de registros en manejo conservador20.
Dentro de las limitaciones del estudio hay que destacar la ausencia de un grupo comparativo dirigido a diálisis en el que se hubiese analizado supervivencia y calidad de vida y el tamaño muestral reducido, lo que resta potencia estadística a nuestros resultados. Por otra parte, utilizamos la versión 2 del instrumento SF-36, que aporta mejoras en las características métricas de dos dimensiones, unos enunciados más sencillos para facilitar la lectura y cumplimentación y tiene un programa de cálculo que mejora la estimación de las respuestas ausentes. No obstante, aunque está traducida al castellano y su uso permite mayor comparabilidad cultural, no se encuentra validada para población española, por lo que no podemos comparar los resultados obtenidos con la población general española.
En conclusión, en nuestro grupo de pacientes en TRC hemos encontrado una mortalidad elevada y homogénea en el tiempo, cuyos factores predictivos independientes fueron la presencia de evento vascular previo, la comorbilidad medida por el índice de Charlson, la albúmina descendida y la elevación de PTH. Hemos comprobado, además, que la calidad de vida se mantiene estable durante el tratamiento. Por todo ello, un adecuado TRC podría ser una opción terapéutica recomendada en estos pacientes, en el que se llevara a cabo un tratamiento activo del hiperparatiroidismo, prevención y tratamiento de la malnutrición y se fomentara la autonomía y rehabilitación física.
Consideramos necesaria la implantación de equipos multidisciplinares (equipos de cuidados paliativos [médicos y enfermeros], geriatras, nutricionistas, fisioterapeutas y atención primaria) para procurar una mejor asistencia en pacientes en TRC. Igualmente sería necesario una mayor coordinación con equipos de cuidados paliativos y soporte domiciliario, especialmente en las últimas fases de la enfermedad, para mantener o incluso mejorar la CVRS en estos pacientes y sus familias.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.