Antecedentes y objetivos: La arteriolopatía urémica calcificante (CUA) o calcifilaxis es una enfermedad rara pero potencialmente mortal que afecta casi exclusivamente a pacientes con enfermedad renal crónica. Para su tratamiento se han empleado diferentes alternativas con resultados irregulares, siendo los bifosfonatos una de ellas. Desde 2002 iniciamos en nuestra Unidad el tratamiento con bifosfonatos en todos los pacientes con diagnóstico de CUA. Material y métodos: Se recogieron prospectivamente, entre 2002 y 2010, ocho pacientes (cuatro hombres, cinco en diálisis y tres con trasplante renal funcionante) con CUA tratados con bifosfonatos. El diagnóstico se realizó por sospecha clínica y biopsia de confirmación. Cinco pacientes con antecedentes de producto calcio-fósforo elevado, seis con antecedentes de hormona paratiroidea elevada (> 800 pg/ml), cuatro paratiroidectomizados, cinco con elevada dosis acumulada de esteroides y seis recibiendo dicumarínicos. Ningún paciente presentaba obesidad ni diabetes mellitus. Resultados: En todos los casos se constató disminución de sintomatología (dolor) a los pocos días y regresión de las lesiones entre 2 a 4 semanas tras iniciar los bifosfonatos, sin cambios en los valores séricos de calcio y fósforo. La mejoría fue más rápida en los que recibieron ibandronato intravenoso. Todos se mantuvieron en tratamiento con bifosfonatos durante al menos 6 meses, hasta que las heridas se curaron completamente. No se han observado recurrencias tras un seguimiento de entre 1 y 9 años. La función renal se mantuvo estable en los pacientes trasplantados. El tratamiento fue bien tolerado y no se observaron efectos adversos. Conclusiones: Los bifosfonatos podrían constituir una alternativa nueva y atractiva para el tratamiento de la CUA.
Background and objectives: Calcific uraemic arteriolopathy (CUA), also known as calciphylaxis, is a rare but life-threatening condition that almost exclusively affects patients with chronic kidney disease. Several therapies have been employed to treat this disease but with irregular results. We report a prospective case series of eight patients diagnosed with CUA in our unit between 2002 and 2010. Material and method: The series consisted of eight patients with CUA (including 4 men, 5 dialysis patients and 3 with functioning allografts) who were treated with bisphosphonates. The diagnosis was by clinical suspicion and a confirmatory biopsy. Five patients had a previous history of high calcium-phosphorus product, 6 had a history of high parathyroid hormone levels (>800pg/ml), 4 had undergone parathyroidectomy, 5 had a history of high cumulative doses of steroids, and 6 patients were under dicoumarin treatment. None of the patients were obese or had diabetes mellitus. Results: In all patients, progression of skin lesions stopped between 2 to 4 weeks after starting bisphosphonate therapy, with no changes in blood levels of calcium and phosphate. Improvement in pain and lesions was faster in patients receiving intravenous ibandronate. All of these patients remained on bisphosphonate treatment for at least 6 months until the wounds healed completely. No recurrences have been observed after follow-up periods between 1 and 9 years. Renal function remained stable in transplant recipients. The treatment was well tolerated and no adverse effects were observed. Conclusions: Bisphosphonates could be a new and attractive alternative to treat CUA.
INTRODUCCIÓN
La arteriolopatía urémica calcificante (CUA), también llamada calcifilaxis, es un trastorno vascular poco frecuente pero potencialmente mortal que afecta casi exclusivamente a pacientes con enfermedad renal crónica (ERC). La incidencia de la CUA en pacientes en diálisis se ha estimado en el 1% anual, y la prevalencia, en hasta un 4%. La CUA es muy incapacitante, con una tasa de mortalidad del 60-80%, siendo la principal causa de muerte la sepsis1,2. A pesar de que la calcificación de la media de grandes vasos es muy frecuente en los pacientes con ERC, la calcificación de pequeño vaso es excepcional. La vulnerabilidad de la piel para el desarrollo de CUA es probablemente debida a su proximidad a los agentes externos, como pueden ser los cambios de temperatura y presión. La CUA se caracteriza por la progresiva calcificación de los vasos pequeños y el desarrollo de necrosis isquémica de los tejidos blandos y la piel.
Debido a la rareza de la CUA, las intervenciones terapéuticas se basan a menudo en los resultados de casos individuales. Los tratamientos tradicionalmente sugeridos incluyen el desbridamiento de tejido necrótico, el tratamiento con antibióticos para evitar o tratar la infección, el apoyo nutricional, la corrección de los parámetros bioquímicos2, la paratiroidectomía, el cinacalcet, el tiosulfato de sodio (STS) y los bifosfonatos3-13. Los bifosfonatos inhiben los osteoclastos y la resorción ósea, y se utilizan en el tratamiento de la osteoporosis, la enfermedad de Paget, el mieloma múltiple y la hipercalcemia inducida por tumor. En modelos animales, los bifosfonatos han demostrado efectos beneficiosos en la prevención de la calcificación arterial3. A raíz de estas últimas observaciones, los bifosfonatos se han introducido recientemente como tratamiento de la CUA, con resultados exitosos9-13. En base a estudios experimentales previos, desde el año 2002 en nuestra Unidad empezamos a emplear los bifosfonatos como alternativa de tratamiento para todos los pacientes que presentaran CUA. Presentamos nuestra serie de casos de CUA desde 2002, tratados todos ellos exitosamente con bifosfonatos.
MATERIAL Y MÉTODOS
Población de estudio
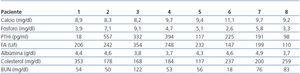
Se recogen prospectivamente los ocho pacientes que se diagnosticaron de CUA en nuestro Servicio entre 2002 y 2010. Se trata de cuatro hombres y cuatro mujeres con una edad media de 61 ± 7 años. Cinco de ellos en hemodiálisis (tres tras pérdida de injerto renal), con un período de diálisis de entre 2 y 20 años. Los otros tres tenían un injerto renal funcionante (entre 1 y 5 años). Las características demográficas y los factores de riesgo se resumen en la tabla 1, y los valores iniciales de laboratorio se resumen en la tabla 2.
Datos relevantes: historia previa de producto calcio-fósforo elevado en cinco pacientes (entre 75-157 mg2/dl2), historia previa de hiperparatiroidismo secundario grave (> 800 pg/ml) en seis pacientes (cuatro de ellos habían sido paratiroidectomizados), historia de alta dosis acumulada de esteroides en cinco pacientes y seis pacientes estaban recibiendo dicumarínicos (Sintrom®) por diversas causas (válvula cardíaca, fibrilación auricular o serios problemas de trombosis del acceso vascular). Sólo un paciente tenía el virus de la hepatitis C (VHC), y ninguno tenía diabetes mellitus o era obeso. Todos presentaron lesiones ulcerosas purpúreas en la piel, con un fondo necrótico, bordes eritematosos y livedo reticularis de toda la zona. Las lesiones se localizaron en el interior de los muslos en seis de los pacientes y en el área tibial en tres pacientes (uno con lesiones en ambos lugares). El diagnóstico se realizó por sospecha clínica con una biopsia de confirmación en seis pacientes.
Tratamiento con bifosfonatos
Todos los pacientes recibieron tratamiento con bifosfonatos: el primer paciente (paciente 1) recibió alendronato oral 70 mg/semana; los próximos cuatro (pacientes 2, 3, 4 y 5) recibieron risedronato oral 35 mg/semana, y los últimos tres (pacientes 6, 7 y 8), ibandronato 6 mg por vía intravenosa (1 dosis), seguido por una segunda dosis de 3 mg a los 15 días y posteriormente ibandronato oral 150 mg/mes durante 6 meses.
En los pacientes que estaban recibiendo dicumarínicos, decidimos mantener la anticoagulación por dos motivos: para evitar problemas de trombosis y para valorar si el efecto sobre la calcifilaxis se debía sólo a los bifosfonatos.
Seguimiento
En todos los pacientes, la terapia con bifosfonatos se mantuvo hasta la total resolución de las lesiones durante al menos 6 meses. Durante el período de seguimiento, se determinaron mensualmente los valores séricos de calcio, fósforo, fosfatasa alcalina y hormona paratiroidea intacta (PTHi) (Diasorin®).
Y en los tres últimos pacientes que recibieron una segunda dosis de ibandronato a los 15 días, también se determinó la calcemia previa a esta segunda administración. En los pacientes con trasplante renal funcionante también se valoró la función renal.
RESULTADOS
En todos los casos, tras la administración de los bifosfonatos se detuvo la progresión de las lesiones cutáneas, iniciándose, a las 2-4 semanas, la cicatrización de los bordes y la reducción del tamaño de la herida. Se constató una progresiva reducción del dolor a los 2-5 días. La mejoría en el dolor y las lesiones fue más rápida en los pacientes tratados con bifosfonatos por vía endovenosa. No se introdujo ninguna otra droga (vitamina D, cinacalcet, captores del fósforo) ni se modificó su tratamiento habitual o esquema de diálisis.
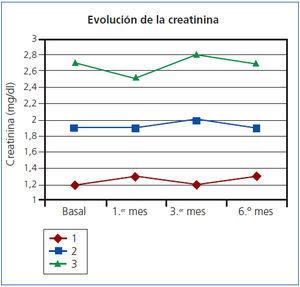
Con un período de seguimiento de entre 1 y 9 años, no se han observado recurrencias en ningún caso ni ha habido ningún éxitus. Tras la administración de los bifosfonatos, no se han observado cambios significativos en los valores sanguíneos de calcio ni fósforo en ninguno de los casos (figura 1), así como tampoco en la PTHi ni fosfatasas alcalinas. En los pacientes con trasplante renal funcionante, la función renal se mantuvo estable (figura 2). El tratamiento fue bien tolerado en todos los casos y no se observaron efectos adversos relevantes.
DISCUSIÓN
La CUA se desarrolla fundamentalmente en pacientes con ERC, tanto estadios 3-4 como diálisis o trasplante renal. La incidencia de la CUA parece haber aumentado en los últimos años por causas desconocidas, aunque también podría deberse a que se recogen mejor los casos, presentándose en hasta un 4% de los pacientes de diálisis1,2.
El diagnóstico de la CUA se debe sospechar ante la presencia de úlceras cutáneas necróticas muy dolorosas en un paciente con ERC de larga evolución. Al principio también se manifiestan otras alteraciones cutáneas, tales como placas induradas o livedo reticularis, a veces con depósitos palpables de calcio subcutáneo. Estas lesiones suelen localizarse en el tronco proximal o en las extremidades, sobre todo en la cara interior de los muslos1.
En radiografías simples con buena sensibilidad se pueden observar calcificaciones de los pequeños vasos, pero el patrón oro diagnóstico sigue siendo la biopsia cutánea de las lesiones, a pesar del riesgo de propagación de la úlcera. Típico de los hallazgos histológicos es la calcificación de los vasos pequeños con proliferación intimal y trombosis intravascular, asociada a veces a paniculitis1, y también se pueden observar depósitos de calcio perivascular con la tinción de von Kossa. Los factores de riesgo de desarrollar CUA incluyen: edad (suelen ser más jóvenes), sexo femenino, alto índice de masa corporal, diabetes mellitus, mayor tiempo en diálisis, valores más elevados de calcemia, fosfatemia, producto calcio-fósforo, fosfatasas alcalinas y PTH. Se ha descrito posible asociación con VHC, siendo otro factor de riesgo importante el estar bajo tratamiento con altas dosis de esteroides o con warfarina (acenocumarol)1,2.
Nuestra serie incluye el mismo número de mujeres que de hombres y un amplio rango de años en diálisis, así como receptores de trasplante renal; sólo hay un paciente con VHC positivo y ningún paciente con obesidad ni con diabetes mellitus. Los actuales valores séricos de calcio, fósforo y PTHi sólo estaban elevados en uno, dos y un paciente, respectivamente, aunque sí es cierto que la mayoría tenían antecedentes de producto calcio-fósforo muy elevado. Por el contrario, la mayoría de nuestros pacientes estaban recibiendo esteroides y acenocumarol.
Cuando se diagnostica una CUA, las alternativas terapéuticas prioritarias incluyen la normalización de calcemia y fosfatemia, evitando el uso de vitamina D y sales de calcio. El tratamiento tópico y el inicio del tratamiento antibiótico empírico también pueden ser de ayuda1,2. En pacientes con valores altos de PTH, la paratiroidectomía se sugirió como una buena alternativa, pero los resultados han sido contradictorios y la mortalidad puede aumentar después de la cirugía1,2. El cinacalcet ha demostrado ser beneficioso en algunos casos de CUA con hiperparatiroidismo secundario, generalmente en combinación con otros tratamientos, tales como el oxígeno hiperbárico y el STS4,8. Se ha descrito algún caso de buena respuesta al tratamiento hiperbárico, aunque siempre en combinación con otras alternativas7.
Recientemente, el STS ha emergido como una interesante opción terapéutica, habiéndose publicado algunos casos aislados y dos series de casos con resultados esperanzadores8. Este compuesto parece jugar un papel en la disolución de los depósitos de calcio en los tejidos mediante la formación de complejos solubles de tiosulfato de calcio, y también puede actuar como un antioxidante mejorando la disfunción endotelial. La serie más reciente, publicada en 2011, describe el uso de STS en seis pacientes; se constató mejoría de dolor o curación de heridas en cuatro de ellos, pero tres pacientes (dos de los cuatro que respondieron) murieron antes del año del diagnóstico8. Además, la mayoría de ellos habían recibido al menos una dosis de pamidronato endovenoso durante o en el mes previo al inicio del STS y dos de ellos recibieron cinacalcet. Sólo un paciente no desarrolló efectos adversos (vómitos o acidosis metabólica).
Otra posible alternativa de tratamiento la constituyen los bifosfonatos, que son análogos del pirofosfato, utilizados ampliamente para el tratamiento de la osteoporosis. El pirofosfato (PPi) es un potente inhibidor de la cristalización de calcio que circula en sangre a concentraciones suficientes para evitar la formación de hidroxiapatita y, por lo tanto, sirve como un inhibidor endógeno de la calcificación14,15. En particular, la producción de PPi por la célula de músculo liso vascular puede ser una defensa importante contra la calcificación vascular de la media. Se ha demostrado que el PPi inhibe la calcificación arterial de la media en ratas intoxicadas con vitamina D16. El efecto de PPi está limitado por su rápida hidrólisis in vivo. Los bifosfonatos son análogos no hidrolizables de los PPi que son capaces de inhibir la calcificación vascular a dosis mucho más bajas15. En los últimos años, los bifosfonatos se han empleado en casos aislados como tratamiento de la CUA con buena respuesta y tolerancia9-13,17.
Farmacológicamente, los bifosfonatos modifican in vitro la cristalización o la reabsorción de la hidroxiapatita dependiendo de su concentración15,18. Se sugiere que el mismo efecto se puede producir in vivo. Estos compuestos también bloquean la transformación de los precursores de osteoclastos en células maduras. Se ha sugerido que la similitud entre la célula muscular lisa y las células de estirpe osteogénica podrían favorecer la unión de los bifosfonatos a la pared vascular y la consecuente prevención de su osificación. Otros estudios también han demostrado que los bifosfonatos reducen la actividad de los macrófagos a nivel local19 y la secreción de citocinas proinflamatorias20.
La administración de difosfonato etano-1-hidroxi-1, 1-difosfonato y difosfonato diclorometileno disminuyó lesiones de CUA en ratas, aunque el mecanismo exacto de acción no está claro21. Por otro lado, en ratas urémicas, el ibandronato, que se sabe que es un potente inhibidor de la calcificación arterial, se ha mostrado eficaz para disminuir y prevenir la calcificación vascular3. Disminuye la concentración de calcio y reduce la capacidad de formación y crecimiento del núcleo mineral en la pared arterial. Todo ello probablemente por la supresión de la producción de citocinas proinflamatorias.
Los bifosfonatos nitrogenados, como el ibandronato, inhiben la producción de isoprenoides de la ruta biosintética del mevalonato, entre ellos, el farnesil pirofosfato22. El farnesil pirofosfato es necesario para la modificación postranslacional de proteínas, como GTP-binding proteins (p. ej. Ras, Rho y Rac)23, posiblemente involucradas en la expresión génica del complejo OPG-RANKL. Ésta podría ser una de las explicaciones del constatado efecto de los bifosfonatos sobre la generación de OPG y su contribución a la mejoría de las calcificaciones extraóseas24.
En nuestros pacientes, hemos observado una rápida mejoría del dolor en las lesiones tras el inicio del tratamiento con bifosfonatos que es independiente del tipo de bifosfonato, aunque más rápido con la administración endovenosa, lo que sugiere un efecto sobre la movilización de las sales de calcio de los tejidos blandos. No se han observado descensos significativos de calcemia en ninguno de nuestros casos. No obstante, ante el potencial riesgo de hipocalcemia con la administración de bifosfonatos, aconsejamos determinación de calcemia entre los 7-15 días posteriores a su administración.
En los últimos años (últimos tres pacientes) hemos decidido utilizar el ibandronato endovenoso basándonos en que parece ser el bifosfonato que, a pesar de poseer un 50% de eliminación renal, se ha mostrado más seguro. No se han descrito efectos negativos sobre la función renal. El ibandronato no afecta a las células tubulares, no interfiere con la reabsorción tubular renal ni afecta a la filtración glomerular25.
Somos conscientes de que existe cierta preocupación en la comunidad científica con el uso de los bifosfonatos en pacientes con ERC avanzada, debido sobre todo al riesgo potencial de provocar o agravar una enfermedad ósea adinámica. No obstante, decidimos emplearlos abiertamente por dos razones fundamentalmente: una de ellas es que se sabe que la capacidad de fijación de los bifosfonatos sobre el hueso está relacionada con la actividad de remodelación, por lo que en la enfermedad ósea adinámica se supone que los bifosfonatos se van a depositar en muy pequeñas cantidades; la otra y más importante es que la calcifilaxis es una patología potencialmente mortal y, por lo tanto, aun a riesgo potencial de agravar una posible enfermedad ósea adinámica, preferimos el beneficio de reducir la morbimortalidad de la CUA.
En conclusión, los bifosfonatos podrían constituir una alternativa nueva y atractiva en el tratamiento de la CUA. Con nuestra experiencia, recomendaríamos la administración inicial de una dosis intravenosa de bifosfonatos, de preferencia el ibandronato, en pacientes con diagnóstico de sospecha de CUA y, en función del diagnóstico definitivo o la evolución, podríamos mantener el tratamiento. No debemos olvidar que la CUA es una condición potencialmente mortal que, en nuestra opinión, debe ser tratada con todas las medidas a nuestro alcance, incluida la supresión de sales cálcicas, vitamina D y análogos, dicumarínicos y factores precipitantes, así como el uso precoz de bifosfonatos o STS.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Figura 2. Valores de creatinina sérica en los pacientes con trasplante renal tras administración de bifosfonatos
Tabla 1. Características demográficas basales y factores de riesgo
Tabla 2. Valores de laboratorio basales
Figura 1. Valores séricos de Ca y P tras la administración de bifosfonatos